Pakkausseloste
BOOSTRIX POLIO injektionsvätska, suspension i förfylld spruta
Tilläggsinformation
Boostrix Polio injektionsvätska, suspension i förfylld spruta
Vaccin mot difteri, stelkramp, kikhosta (acellulärt, komponent) och polio (inaktiverat), adsorberat, med reducerat antigeninnehåll
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du eller ditt barn börjar använda detta vaccin. Den innehåller information som är viktig för dig.
- Spara denna information. Du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
- Detta vaccin har ordinerats enbart åt dig eller ditt barn. Ge det inte till andra.
- Om du eller ditt barn får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad Boostrix Polio är och vad det används för
2. Vad du behöver veta innan du eller ditt barn får Boostrix Polio
3. Hur Boostrix Polio ska användas
4. Eventuella biverkningar
5. Hur Boostrix Polio ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Boostrix Polio är ett vaccin som används som påfyllnadsdos till barn från 3 års ålder, ungdomar och vuxna för att förhindra fyra sjukdomar: difteri, stelkramp (tetanus), kikhosta (pertussis) och polio (poliomyelit). Vaccinet verkar genom att hjälpa kroppen att producera egna antikroppar (skydd) mot dessa sjukdomar.
- Difteri: Difteri påverkar huvudsakligen luftvägarna och ibland huden. Luftvägarna blir vanligtvis inflammerade (svullna) vilket kan orsaka svåra andningsproblem och i värsta fall kvävning. Bakterierna frisläpper också ett gift (toxin) som kan orsaka nervskada, hjärtproblem och i värsta fall dödsfall.
- Stelkramp (tetanus): Stelkrampsbakterier kommer in i kroppen genom skärsår, skrapsår och andra skador i huden. Skador som är särskilt utsatta för infektion är brännskador, frakturer, djupa sår och sår som förorenats med jord, damm, hästgödsel/dynga eller träflisor. Bakterierna frisläpper ett gift (toxin) som kan orsaka muskelstelhet, smärtsamma muskelspasmer, krampanfall och till och med död. Muskelspasmerna kan vara så kraftiga att de orsakar benfrakturer i ryggraden.
- Kikhosta (pertussis): Kikhosta är en mycket smittsam sjukdom som påverkar luftvägarna och orsakar svåra attacker av hosta som kan störa normal andning. Hostan åtföljs ofta av ett ”kiknande” läte, därav namnet kikhosta. Hostan varar 1-2 månader eller längre. Kikhosta kan också orsaka öroninfektioner, luftrörskatarr som kan vara under lång tid, lunginflammation, krampanfall, hjärnskador och i värsta fall dödsfall.
- Polio (poliomyelit): Poliomyelit som förenklat kallas polio är en virusinfektion som kan yttra sig på olika sätt. Det orsakar ofta enbart mild sjukdom men kan även orsaka bestående skador eller i värsta fall dödsfall. I dess svåraste form kan polioinfektion orsaka förlamning av musklerna (musklerna kan inte röra sig), inklusive andningsmuskulaturen och de muskler som behövs för att kunna gå. De kroppsdelar som påverkas av sjukdomen kan bli smärtsamt deformerade.
Inget av innehållsämnena i vaccinet kan orsaka difteri, stelkramp, kikhosta eller polio.
Användning av Boostrix Polio under graviditet bidrar till att skydda ditt barn mot kikhosta under de första levandsmånaderna innan han/hon grundvaccineras.
Vad du behöver veta innan produkten används
Boostrix Polio ska inte ges
- om du eller ditt barn tidigare fått en allergisk reaktion mot Boostrix Polio eller något annat innehållsämne i detta vaccin (anges i avsnitt Förpackningens innehåll och övriga upplysningar) eller neomycin, polymyxin (antibiotika) eller formaldehyd. Tecken på en allergisk reaktion kan inkludera kliande hudutslag, andfåddhet och svullnad av ansikte och tunga.
- om du eller ditt barn tidigare fått en allergisk reaktion mot något vaccin mot difteri, stelkramp, kikhosta eller polio.
- om du eller ditt barn fått en neurologisk sjukdom (encefalopati) inom 7 dagar efter tidigare vaccination med vaccin mot kikhosta.
- om du eller ditt barn fått en tillfällig minskning av antalet blodplättar (vilket ökar risken för blödning eller blåmärken) eller en neurologisk sjukdom efter tidigare vaccination med ett vaccin mot difteri och/eller stelkramp.
- om du eller ditt barn har en kraftig infektion med hög feber (över 38 °C). En lättare infektion såsom en vanlig förkylning är sannolikt inget problem, men tala med läkaren först.
Varningar och försiktighet
Tala med läkare eller apotekspersonal innan du eller ditt barn får Boostrix Polio.
- om du eller ditt barn tidigare har fått något hälsoproblem i anslutning till tidigare vaccination med vaccin mot kikhosta, såsom:
- hög feber (över 40 °C) inom 48 timmar efter vaccination
- kollaps eller chockliknande tillstånd inom 48 timmar efter vaccination
- ihållande, otröstlig gråt som varade 3 timmar eller längre, inom 48 timmar efter vaccination
- kramper med eller utan feber inom 3 dagar efter vaccination
- om ditt barn har en odiagnostiserad eller pågående hjärnsjukdom eller epilepsi som inte är under kontroll. Vaccinet bör ges när sjukdomen är under kontroll.
- om du eller ditt barn har ökad risk för blödningar eller har lätt att få blåmärken
- om du, ditt barn eller någon annan i familjen har tendens att få feberkramper
- om du eller ditt barn har långvariga problem med immunförsvaret (inklusive hiv-infektion). Du eller ditt barn erhåller eventuellt ändå Boostrix Polio men får kanske inte ett lika bra skydd mot infektioner efter vaccinationen som vuxna och barn med fullgott immunförsvar mot infektioner.
Svimning kan förekomma (främst hos ungdomar) efter, eller även före, all nålinjektion. Tala därför om för läkaren eller sjuksköterskan om du eller ditt barn har svimmat vid tidigare injektion.
Som med alla vacciner ger Boostrix Polio eventuellt inte fullt skydd hos alla personer som vaccineras.
Andra läkemedel och Boostrix Polio
Tala om för läkare eller apotekspersonal om du eller ditt barn tar nyligen har tagit eller kan tänkas ta andra läkemedel eller nyligen fått något annat vaccin.
Boostrix Polio kan ges samtidigt med vissa andra vacciner. Injektionsställe ska bytas för varje typ av vaccin.
Boostrix Polio kan ha sämre effekt om du eller ditt barn tar läkemedel som minskar immunförsvarets förmåga att bekämpa infektioner.
Graviditet, amning och fertilitet
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du får detta vaccin.
Det är inte känt om Boostrix Polio passerar över i modersmjölk. Din läkare kommer att tala med dig om möjliga risker och fördelar av vaccination med Boostrix Polio i samband med amning.
Körförmåga och användning av maskiner
Det är inte troligt att Boostrix Polio skulle ha någon effekt på förmågan att framföra fordon och använda maskiner. Du är dock själv ansvarig för att bedöma om du är i kondition att framföra motorfordon eller utföra arbete som kräver skärpt uppmärksamhet. En av faktorerna som kan påverka din förmåga i dessa avseenden är användningen av läkemedel på grund av deras effekter och/eller biverkningar. Beskrivning av dessa effekter och biverkningar finns i andra avsnitt. Läs därför all information i denna bipacksedel för vägledning. Diskutera med läkare eller apotekspersonal om du är osäker.
Boostrix Polio innehåller neomycin och polymyxin
Detta vaccin innehåller neomycin och polymyxin (antibiotika). Tala om för din eller ditt barns läkare om du eller ditt barn har haft en allergisk reaktion mot något av dessa innehållsämnen.
Boostrix Polio innehåller para-aminobensoesyra, fenylalanin, natrium och kalium
Boostrix Polio innehåller para-aminobensoesyra. Det kan orsaka allergiska reaktioner (eventuellt fördröjda) och i undantagsfall bronkospasm.
Vaccinet innehåller 0,0298 mikrogram fenylalanin i varje dos. Fenylalanin kan vara skadligt om du har fenylketonuri (PKU), en sällsynt genetisk störning där fenylalanin byggs upp för att kroppen inte kan avlägsna det ordentligt.
Detta läkemedel innehåller mindre än 1 mmol natrium (23 mg) per dos, d.v.s. är näst intill “natriumfritt”.
Detta läkemedel innehåller kalium, mindre än 1 mmol (39 mg) per dos, d.v.s är näst intill “kaliumfritt”.
Hur produkten används
- Boostrix Polio ges som en injektion i muskeln.
- Vaccinet ska aldrig ges i ett blodkärl.
- Du eller ditt barn kommer att få en injektion med Boostrix Polio.
- Din eller ditt barns läkare kommer att kontrollera om du eller ditt barn tidigare vaccinerats mot difteri, stelkramp, kikhosta och/eller polio.
- Boostrix Polio kan användas vid infektion med misstänkt stelkrampssmitta, men även annan ytterligare behandling såsom noggrann sårrengöring och/eller tillförsel av stelkrampsantikroppar (motverkar stelkrampsbakteriens gift) ges för att minska risken för stelkramp.
- Din eller ditt barns läkare kommer att ge dig råd angående ytterligare vaccinationer.
Eventuella biverkningar
Liksom alla läkemedel kan detta vaccin orsaka biverkningar men alla användare behöver inte få dem.
Som med alla vacciner för injektion kan det mycket sällan (upp till 1 av 10 000 vaccindoser) förekomma allvarliga allergiska reaktioner (anafylaktiska och anafylaktoida reaktioner). Dessa känns igen genom
- hudutslag med blåsor eller klåda
- svullnad av ögon och ansikte
- svårighet att andas eller svälja
- plötsligt blodtrycksfall och medvetslöshet.
Sådana reaktioner inträffar vanligtvis innan man hunnit lämna mottagningen. Om du eller ditt barn får några av dessa symtom ska läkare omedelbart kontaktas.
Biverkningar som förekommit under kliniska studier hos barn 4-8 år
Mycket vanliga (kan förekomma vid fler än 1 av 10 vaccindoser): smärta, rodnad och svullnad vid injektionsstället, sömnighet.
Vanliga (kan förekomma vid upp till 1 av 10 vaccindoser): feber 37,5 °C eller högre (inklusive feber över 39 °C), blödning, klåda och förhårdnad vid injektionsstället, kraftig svullnad av den vaccinerade kroppsdelen, aptitlöshet, irritabilitet, huvudvärk.
Mindre vanliga (kan förekomma vid upp till 1 av 100 vaccindoser): diarré, illamående, kräkning, ont i magen, svullna körtlar i halsen, armhålan eller ljumsken (lymfadenopati), sömnproblem, apati, muntorrhet, trötthet.
Samtidig vaccination mot mässling-påssjuka-röda hund (MPR) eller mässling-påssjuka-röda hund-vattkoppor (MPR/V) hos barn i åldern 3-6 år
I studier där Boostrix Polio gavs samtidigt med MPR- eller MPR/V-vacciner rapporterades övre luftvägsinfektion (däribland snuva och halsont) och hudutslag som vanliga biverkningar. Feber, irritabilitet, trötthet, minskad aptit och magtarmbesvär (däribland diarré och kräkningar) rapporterades med en högre frekvens (mycket vanliga) än i studier där enbart Boostrix Polio gavs.
Biverkningar som förekommit i kliniska studier av vuxna, ungdomar och barn från 10 års ålder
Mycket vanliga (kan förekomma vid fler än 1 av 10 vaccindoser): smärta, rodnad och svullnad vid injektionsstället, trötthet, huvudvärk.
Vanliga (kan förekomma vid upp till 1 av 10 vaccindoser): feber 37,5 °C eller högre, blåmärke, klåda, förhårdnad, domning med värmekänsla vid injektionsstället, ont i magen, illamående, kräkning.
Mindre vanliga (kan förekomma vid upp till 1 av 100 vaccindoser): feber över 39 °C, kraftig svullnad av den vaccinerade kroppsdelen, frossa, smärta, yrsel, ledsmärta, muskelvärk, klåda, oral herpes, svullna körtlar i halsen, armhålan eller ljumsken (lymfadenopati), minskad aptit, stickande känsla eller domningar i händer eller fötter (parestesi), sömnighet, astma.
Följande biverkningar förekom under rutinanvändning av Boostrix Polio och är inte specifika för någon åldersgrupp: kollaps eller perioder av medvetslöshet eller sänkt medvetande, svullnad av ansiktet, läpparna, munnen, tungan eller halsen som kan orsaka svårighet att svälja eller andas (angioödem), kramper eller anfall (med eller utan feber), nässelfeber (urticaria), ovanlig svaghet (asteni).
Dessutom har följande biverkningar rapporterats under kliniska studier med Boostrix (GlaxoSmithKline Biologicals boostervaccin mot difteri, stelkramp och kikhosta):
Biverkningar som förekommit hos barn från 4 till 8 års ålder
Mindre vanliga (kan förekomma vid upp till 1 av 100 vaccindoser): uppmärksamhetsstörningar, utsöndringar från ögonen med klåda och skorpor på ögonlocken (konjunktivit), smärta.
Biverkningar som förekommit hos vuxna, ungdomar och barn från 10 års ålder och uppåt
Mycket vanliga (kan förekomma vid fler än 1 av 10 vaccindoser): allmän sjukdomskänsla.
Vanliga (kan förekomma vid upp till 1 av 10 vaccindoser): hård knöl eller böld vid injektionsstället.
Mindre vanliga (kan förekomma vid upp till 1 av 100 vaccindoser): övre luftvägsinfektion, halsont och obehag vid sväljning (faryngit), svimning (synkope), hosta, diarré, kraftig svettning (hyperhidros), hudutslag, led- och muskelstelhet, influensaliknande symtom, t.ex. feber, halsont, rinnande näsa, hosta och frossa.
Efter administrering av vacciner mot stelkramp har det mycket sällan (upp till 1 av 10 000 vaccindoser) förekommit en tillfällig inflammation i nerverna, vilken ger smärta, svaghet och förlamning av armar och ben som även kan stiga uppåt mot bröstet och ansiktet (Guillain-Barrés syndrom).
Rapportering av biverkningar
Om du eller ditt barn får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
I Sverige:
Läkemedelsverket
Box 26
751 03 Uppsala
I Finland:
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta vaccin utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på kartongen och den förfyllda sprutans etikett, efter Utg.dat /EXP. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras i kylskåp (2 °C – 8 °C).
Får ej frysas. Frysning förstör vaccinet.
Förvaras i originalförpackningen. Ljuskänsligt.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
De aktiva substanserna är:
- Difteritoxoid1 inte mindre än 2 Internationella Enheter (IE) (2,5 Lf)
Tetanustoxoid1 inte mindre än 20 Internationella Enheter (IE) (5 Lf)
Bordetella pertussis-antigen
Pertussistoxoid1 8 mikrogram
Filamentöst hemagglutinin1 8 mikrogram
Pertaktin1 2,5 mikrogram
Inaktiverade poliovirus
typ 1 (Mahoney-stam)2 40 D-antigenenheter
typ 2 (MEF-1-stam)2 8 D-antigenenheter
typ 3 (Saukett-stam)2 32 D-antigenenheter
1adsorberat på hydratiserad aluminiumhydroxid (Al(OH)3) 0,3 milligram Al3+
och aluminiumfosfat (AlPO4) 0,2 milligram Al3+
2odlat på VERO-celler
Aluminiumhydroxid och aluminiumfosfat ingår i detta vaccin som adjuvans. Adjuvans är ämnen som ingår i en del vacciner för att påskynda, förbättra och/eller förlänga vaccinets skyddseffekt.
- Övriga innehållsämnen är: Medium 199 (innehållande aminosyror (inklusive fenylalanin), mineralsalter (inklusive natrium och kalium), vitaminer (inklusive para-aminobensoesyra) och andra ämnen), natriumklorid och vatten för injektionsvätskor.
Läkemedlets utseende och förpackningsstorlekar
Injektionsvätska, suspension i förfylld spruta.
Boostrix Polio är en vit, mjölkaktig vätska som tillhandahålls i förfylld spruta (0,5 ml).
Boostrix Polio tillhandahålls i en förfylld spruta innehållande en dos med eller utan separata nålar i förpackningsstorlekar om 1 och 10 stycken.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning och tillverkare
I Sverige
Innehavare av godkännande för försäljning/Information lämnas av:
GlaxoSmithKline AB
Box 516
169 29 Solna
Tel: 08-638 93 00
E-post: info.produkt@gsk.com
I Finland Innehavare av godkännande för försäljning:
GlaxoSmithKline Biologicals s.a.
Rue de l’Institut 89
B-1330 Rixensart
Belgien
Information lämnas av:
GlaxoSmithKline Oy
Biskopsbro 9A
02230 Esbo
Tel. 010 30 30 30
Tillverkare:
GlaxoSmithKline Biologicals s.a
Rue de l’Institut 89
B-1330 Rixensart
Belgien
Detta läkemedel är godkänt inom Europeiska ekonomiska samarbetsområdet under följande namn:
Boostrix Polio: Belgien, Bulgarien, Danmark, Finland, Grekland, Island, Lettland, Litauen, Luxemburg, Nederländerna, Norge, Polen, Portugal, Slovakien, Slovenien, Spanien, Sverige, Tjeckien, Tyskland, Ungern, Österrike
Boostrix Tetra: Frankrike
IPV-Boostrix: Irland, Malta
Polio Boostrix: Italien
Boostrix-IPV: Rumänien
Denna bipacksedel ändrades senast: 27.6.2023 (i Finland)
Övriga informationskällor
Ytterligare information om detta läkemedel finns på Läkemedelsverkets hemsida: http://www.lakemedelsverket.se
Direktiv för experterna inom hälsovården
Följande uppgifter är endast avsedda för hälso- och sjukvårdspersonal:
Före användning ska vaccinet vara rumstemperat och omskakas väl till en homogen grumlig vit suspension. Före administrering ska vaccinet inspekteras visuellt med avseende på främmande partiklar och/eller fysikaliska förändringar.Administrera inte vaccinet om något avvikande observeras.
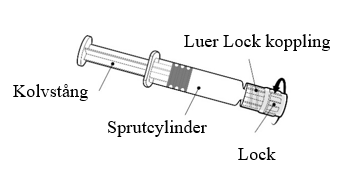
Instruktioner för den förfyllda sprutan
|
|
Håll alltid i sprutcylindern, inte i kolvstången. Skruva av locket på sprutan genom att vrida den motsols. |
|
|
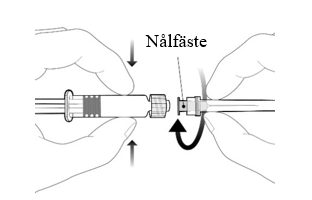
Fäst nålen på sprutan genom att ansluta den till Luer Lock kopplingen och rotera ett kvarts varv medsols tills du känner att den låser sig. Lock Dra inte ut kolvstången ur sprutcylindern, om detta sker ska vaccinet inte administreras. |
Destruktion
Ej använt läkemedel och avfall ska hanteras enligt lokala anvisningar.