HEXVIX pulver och vätska till intravesikal lösning 85 mg
Tilläggsinformation
Hexvix 85 mg pulver och vätska till intravesikal lösning
hexaminolevulinat
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du får detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till din läkare eller sjuksköterska.
- Om du får biverkningar, tala med läkare eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
- Vad Hexvix är och vad det används för
- Vad du behöver veta innan du får Hexvix
- Hur du använder Hexvix
- Eventuella biverkningar
- Hur Hexvix ska förvaras
- Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Detta läkemedel är endast avsett för diagnostik.
Detta läkemedel används som hjälp för att identifiera blåscancer. Det ges till dig innan läkaren använder ett speciellt instrument som kallas cystoskop för att titta inuti din blåsa. Ett cystoskop används som hjälp för att se eventuella tumörer, vilka lyser upp i blått ljus efter administrering av Hexvix. De onormala cellerna kan därmed tas bort.
Vad du behöver veta innan produkten används
Använd inte Hexvix
- om du är allergisk mot den aktiva substansen eller mot något annat innehållsämne i detta läkemedel, inklusive den vätska som används för att lösa upp det i (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
- om du har porfyri (en sällsynt, ärftlig blodsjukdom).
Varningar och försiktighet
Tala med läkare eller sjuksköterska innan du får Hexvix:
- Om du har en urinvägsinfektion eller en brännande känsla när du urinerar.
- Om du nyligen fått en BCG-behandling (försvagade tuberkelbakterier insprutat i urinblåsan).
- Om du nyligen genomgått en operation av blåsan.
Dessa tillstånd kan orsaka lokala reaktioner i urinblåsan, vilket kan försvåra för din läkare att tolka resultatet av undersökningen.
Andra läkemedel och Hexvix
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel.
Graviditet, amning och fertilitet
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare innan du använder detta läkemedel.
Körförmåga och användning av maskiner
Du är själv ansvarig för att bedöma om du är i kondition att framföra motorfordon eller utföra arbete som kräver skärpt uppmärksamhet. En av faktorerna som kan påverka din förmåga i dessa avseenden är användning av läkemedel på grund av deras effekter och/eller biverkningar. Beskrivning av dessa effekter och biverkningar finns i andra avsnitt. Läs därför all information i denna bipacksedel för vägledning. Diskutera med läkare eller apotekspersonal om du är osäker.
Hur produkten används
Hexvix iordningställs och ges till dig av speciellt utbildad och behörig personal.
- Hexvix ges i normala fall på sjukhus eller läkarmottagning.
Din läkare ger det till dig på följande sätt:
- En smal slang kallad kateter placeras i urinblåsan.
- Din blåsa töms genom slangen.
- Hexvix förs in i blåsan genom slangen.
- Hexvix hålls kvar inne i blåsan ungefär 60 minuter.
- Din blåsa töms sedan genom slangen.
- Läkaren använder ett instrument (cystoskop) för att undersöka insidan av din urinblåsa.
Om du fått mer Hexvix än vad du borde
Om Hexvix hålls kvar i blåsan längre än 60 minuter eller om mer Hexvix än vanligt används förväntas inga biverkningar uppstå. Tala med din läkare eller sjuksköterska om du är orolig för detta.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem. Det finns en risk för biverkningar som har att göra med den undersökningsteknik (cystoskopi) som används för att se insidan av urinblåsan. Användningen av Hexvix som en kompletterande procedur till standardcystoskopi för en noggrannare diagnos av din blåscancer tolereras vanligtvis väl. Om biverkningar uppkommer förväntas dessa vara relaterade till undersökningstekniken och är vanligtvis inte allvarliga och varar inte länge. Följande biverkningar kan uppstå efter undersökningsproceduren vid användning av detta läkemedel:
Vanliga (kan förekomma hos upp till 1 av 10 personer):
- Illamående, kräkning.
- Diarré.
- Förstoppning.
- Muskelkramp eller smärta i eller i närheten av magen.
- Smärta vid tömning av blåsan eller svårigheter att kasta vatten.
- Oförmåga att tömma blåsan (urinretention).
- Blod i urinen.
- Smärta efter undersökningen.
- Feber.
Mindre vanliga (kan förekomma hos upp till 1 av 100 personer):
- Huvudvärk.
- Brännande känsla när du kastar vatten (orsakas av inflammation eller infektion i urinblåsan).
- Behov av att kasta vatten oftare
- Blodförgiftning.
- Sömnlöshet eller svårighet att somna.
- Smärta i urinröret.
- Känsla att du behöver kasta vatten omedelbart (urinträngning).
- Ökat antal vita blodkroppar, ökade nivåer av bilirubin (det gula pigmentet i gallan) eller leverenzymer. Dessa biverkningar ses i blodprovssvar.
- Minskat antal röda blodkroppar (anemi).
- Inflammation i ollonet (balanit).
- Ryggsmärta.
- Gikt.
- Hudutslag.
- Klåda.
Ingen känd frekvens (kan inte beräknas från tillgängliga data)
- Anafylaktisk chock (blodtrycksfall, ökad hjärtfrekvens, hudutslag).
Rapportering av biverkningar
Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på yttre förpackningen efter Utg.dat. Utgångsdatum är den sista dagen i angiven månad.
Pulver och vätska: Inga särskilda förvaringsanvisningar.
Lösning (efter blandning): Förvaras i kylskåp (2°C–8°C), lösningen ska användas inom 2 timmar.
Sjukvårdspersonalen ser till att medicinen förvaras och kasseras på rätt sätt och att inte används efter utgångsdatumet på kartongen.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- Den aktiva substansen är hexaminolevulinat.
- Övriga innehållsämnen är dinatriumfosfatdihydrat, kaliumdivätefosfat, natriumklorid, saltsyra, natriumhydroxid och vatten för injektionsvätskor.
Läkemedlets utseende och förpackningsstorlekar:
- Varje förpackning består av en injektionsflaska med vitt till benvitt eller ljusgult pulver innehållande 85 mg av den aktiva substansen hexaminolevulinat och en förfylld spruta med eller utan en Mini-Spike innehållande 50 ml klar färglös vätska för upplösning av pulvret.
- Hexvix pulver löses upp i den vätska på 50 ml, som följer med förpackningen. När pulver och vätska har blandats, erhålls en lösning innehållande hexaminolevulinat 1,7 mg/ml, vilket motsvarar hexaminolevulinat 8 mmol/l lösning.
Innehavare av godkännande för försäljning och tillverkare
Photocure ASA
Hoffsveien 4
NO-0275 Oslo
Norge
Detta läkemedel är godkänt under namnet Hexvix i följande medlemsstater inom Europeiska ekonomiska samarbetsområdet och i Förenade kungariket (Nordirland): Belgien, Danmark, Estland, Finland, Frankrike, Förenade kungariket (Nordirland), Grekland, Irland, Island, Italien, Lettland, Litauen, Nederländerna, Norge, Polen, Portugal, Slovenien, Spanien, Sverige, Tjeckien, Tyskland, Ungern, Österrike.
Denna bipacksedel ändrades senast 01.02.2022.
Direktiv för experterna inom hälsovården
Följande uppgifter är endast avsedda för hälso- och sjukvårdpersonal:
Anvisningar för hantering
Hexaminolevulinat kan orsaka sensibilisering vid hudkontakt.
Alla steg skall utföras med steril utrustning och med aseptiska rutiner.
Instruktioner för rekonstitution A: Hexvix pulver och vätska för Hexvix i förfylld spruta
|
|
1. Fäst kolvstången i gummiproppen i sprutan genom att vrida kolvstången medurs tills det tar stopp. 2. Ta bort locket från sprutan och behåll den för senare användning. Anslut en nål, som är lämplig för beredning, på sprutan. Håll sprutan upprätt och tryck försiktigt kolvstången uppåt för att avlägsna luft. |
|
|
3. Injicera ca 10 ml av vätskan i injektionsflaskan med pulver. Injektionsflaskan bör bli ca ¾ full. |
|
|
4. Håll injektionsflaskan med pulver och sprutan i ett fast grepp, utan att dra ut nålen ur injektionsflaskan, och skaka försiktigt för att säkerställa fullständig upplösning. |
|
|
5. Dra upp all den upplösta beredningen i injektionsflaskan med pulver in i sprutan. |
|
|
6. Koppla bort den tomma injektionsflaskan från sprutan. Koppla bort nålen från sprutspetsen och kassera den. Förslut sprutan med sprutlocket. Blanda försiktigt innehållet i sprutan. |
Hexvix är nu blandad och klar för användning. Utseendet på den färdigblandade lösningen är klar till lätt opalescent och färglös till ljusgul. Lägg till två timmar på den nuvarande tiden och skriv den resulterande utgångstiden och datumet på sprutans etikett.
Instruktioner för rekonstitution B: Hexvix pulver och vätska för Hexvix i förfylld spruta med Mini-Spike
|
1. Fäst kolvstången i gummiproppen i sprutan genom att vrida kolvstången medurs tills det tar stopp. |
|
|
|
2. Penetrera proppen i injektionsflaskan med pulver med Mini-Spike. Ta av locket från sprutan och behåll den för senare användning. Håll sprutan upprätt och tryck försiktigt kolven uppåt för att avlägsna luft. Anslut sprutan till Mini-Spike. |
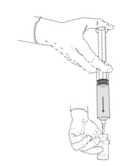 |
3. Injicera ca 10 ml av vätskan ner i injektionsflaskan med pulver. Injektionsflaskan bör bli ca ¾ full. |
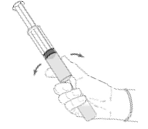 |
4. Utan att dra ut Mini-Spike från injektionsflaskan, håll injektionsflaskan med pulver och sprutan i ett fast grepp och skaka försiktigt för att säkerställa fullständig upplösning. |
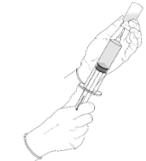 |
5. Vänd injektionsflaskan och sprutan upp och ner och dra upp all den upplösta lösningen, från injektionsflaskan med pulver, i sprutan. |
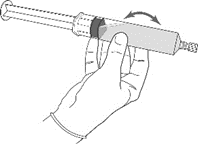 |
6. Koppla bort den tomma injektionsflaskan och Mini-Spike från sprutan, kassera injektionsflaska och Mini-Spike. Förslut sprutan med sprutlocket. Blanda försiktigt innehållet i sprutan. |
Hexvix är nu blandad och klar för användning. Utseendet på den färdigblandade lösningen är klar till lätt opalescent och färglös till ljusgul.
Lägg till två timmar på den nuvarande tiden och skriv den resulterande utgångstiden och datumet på sprutans etikett.
Endast avsedd för engångsbruk. Oanvänd lösning skall kasseras. Inga särskilda anvisningar för destruktion.
Kemisk och fysikalisk stabilitet för lösningen har visats under 2 timmar vid 2°C-8°C. Från mikrobiologisk synpunkt bör produkten användas omedelbart. Om den inte används omedelbart är förvaringstiden och förvaringsvillkoren före administrering användarens ansvar och ska normalt inte vara mer än 2 timmar vid 2°C-8°C.