OSURNIA örongel 10 mg/10 mg/1 mg
DET VETERINÄRMEDICINSKA LÄKEMEDLETS NAMN
OSURNIA örongel för hundar
DEKLARATION AV AKTIVA SUBSTANSER OCH ÖVRIGA SUBSTANSER
Varje dos (1,2 g) innehåller:
Aktiva substanser:
Terbinafin (Terbinafinum): 10 mg
Florfenikol (Florfenicolum): 10 mg
Betametasonacetat (betamethasoni acetas): 1 mg
motsvarande betametasonbas 0,9 mg
Hjälpämnen:
Butylhydroxitoluen (E 321) 1 mg
Gulvit till svagt gul genomskinlig gel.
ANVÄNDNINGSOMRÅDEN
Behandling av akut inflammation i ytterörat och akut försämring av återkommande inflammation i ytterörat orsakad av bakterien Staphylococcus pseudintermedius och svampen Malassezia pachydermatis.
KONTRAINDIKATIONER
Använd inte om trumhinnan är perforerad.
Använd inte till hundar med generaliserad demodikos (hårsäckkvalster).
Använd inte till dräktiga djur eller avelsdjur.
Använd inte vid överkänslighet mot de aktiva substanserna, andra kortikosteroider eller mot något av hjälpämnena.
BIVERKNINGAR
Hund:
Mycket sällsynta (färre än 1 av 10 000 behandlade djur, enstaka rapporterade händelser inkluderade): | Dövheta, nedsatt hörsela Erytem vid appliceringsstället, smärta vid appliceringsstället, klåda vid appliceringsstället, ödem vid appliceringsstället, sår vid appliceringsstället Överkänslighetsreaktioner (t.ex. ansiktsödem, nässelutslag och chock) Ögonsjukdomar (t.ex. neurogen keratokonjunktivit sicca, keratokonjunktivit sicca, sår på hornhinnan, blefarospasm, ögonrodnad och okulär flytning)b Ataxi, ansiktsförlamning, nystagmus Störning i innerörat (huvudsakligen lutande huvud) |
a Oftast övergående och i huvudsakligen hos äldre djur.
b Se även avsnitt ”Särskilda försiktighetsåtgärder för säker användning hos det avsedda djurslaget”.
Det är viktigt att rapportera biverkningar. Det möjliggör fortlöpande säkerhetsövervakning av ett läkemedel. Om du observerar biverkningar, även sådana som inte nämns i denna bipacksedel, eller om du tror att läkemedlet inte har fungerat, meddela i första hand din veterinär. Du kan också rapportera eventuella biverkningar till innehavaren av godkännande för försäljning genom att använda kontaktuppgifterna i slutet av denna bipacksedel, eller via ditt nationella rapporteringssystem:
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
webbplats: https://www.fimea.fi/sv/veterinar.
DJURSLAG
Hund.
DOSERING FÖR VARJE DJURSLAG, ADMINISTRERINGSSÄTT OCH ADMINISTRERINGSVÄGAR
För användning i örat. Använd en tub per infekterat öra. Upprepa behandlingen efter 7 dagar.
Maximalt behandlingssvar uppnås eventuellt inte förrän 21 dagar efter det andra behandlingstillfället.
1. Öppna tuben genom att vrida om den mjuka spetsen.
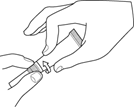
2. För in den flexibla mjuka spetsen i hörselgången.
3. Applicera läkemedlet i hörselgången genom att pressa tuben mellan två fingrar.
4. Efter appliceringen kan örats bas masseras försiktigt under en kort stund så att läkemedlet fördelas jämnt i hörselgången.
ANVISNING FÖR KORREKT ADMINISTRERING
Innan läkemedlet appliceras ska den yttre hörselgången undersökas noga för att säkerställa att
trumhinnan inte är perforerad.
Rengör öronen före det första behandlingstillfället. Rengöringen av örat får inte upprepas förrän 21 dagar efter det andra behandlingstillfället. I kliniska studier rengjordes öronen med enbart natriumkloridlösning.
Om behandling med detta läkemedel avbryts bör hörselgångarna rengöras innan behandling med en annan produkt påbörjas.
KARENSTIDER
Ej relevant.
SÄRSKILDA FÖRVARINGSANVISNINGAR
Förvaras utom syn- och räckhåll för barn.
Förvaras i kylskåp (2 °C-8 °C).
Använd inte detta läkemedel efter utgångsdatumet på etiketten efter Exp. Utgångsdatumet är den sista dagen i angiven månad.
SÄRSKILDA VARNINGAR
Särskilda varningar:
Rengör öronen före det första behandlingstillfället. Rengöringen ska inte upprepas förrän 21 dagar efter det andra behandlingstillfället. I kliniska studier rengjordes öronen med enbart natriumkloridlösning.
Övergående fuktighet i den inre och yttre öronmusslan kan förekomma. Fuktigheten orsakas av
användning av produkten och saknar betydelse.
Öroninflammation som orsakas av bakterier och svamp uppkommer ofta till följd av andra tillstånd.
En korrekt diagnos bör ställas och behandling av bakomliggande orsaker utredas innan behandling med antibiotika övervägs.
Hos djur med tidigare kronisk eller återkommande inflammation i ytterörat kan läkemedlets effektivitet påverkas om de underliggande orsakerna till tillståndet, såsom allergi eller örats anatomiska struktur, inte beaktas.
Särskilda försiktighetsåtgärder för säker användning hos det avsedda djurslaget:
Om överkänslighet mot något av innehållsämnena uppstår ska örat tvättas noggrant.
Säkerheten för detta läkemedel har inte fastställts hos hundar som är yngre än 2 månader eller väger mindre än 1,4 kg.
Användning av läkemedlet ska om möjligt baseras på identifiering av de infekterande organismerna samt på känslighetstest.
Användning av läkemedlet som avviker från instruktionerna i bipacksedeln kan öka förekomsten av bakterier och svamp som är resistenta mot florfenikol respektive terbinafin och kan minska effekten av behandling med andra antibiotika och antimykotika.
Vid öroninflammation som orsakas av parasiter bör lämpligt kvalsterdödande medel sättas in.
Innan läkemedlet appliceras ska den yttre hörselgången undersökas noga för att säkerställa att trumhinnan inte är perforerad.
Långvarig och intensiv användning av topikala kortikosteroidberedningar är känd för att ge systemiska effekter, inklusive hämmad binjurefunktion (se avsnittet ”Överdosering”).
I toleransstudier observerades minskade kortisolnivåer efter administrering av produkten i samband med test för Addisons sjukdom, vilket tyder på att betametason absorberas och upptas i blodcirkulationen. Detta var inte förknippat med några kliniska tecken eller symtom och var övergående.
Ytterligare kortikosteroidbehandlingar bör undvikas.
Används med försiktighet till hundar med misstänkt eller bekräftad endokrin störning (t ex diabetes mellitus, underaktiv eller överaktiv sköldkörtel).
Läkemedlet kan irritera ögonen. Undvik oavsiktlig kontakt med hundens ögon. Vid oavsiktlig exponering av ögonen ska ögonen noga sköljas med vatten i 10–15 minuter. Om kliniska tecken utvecklas, uppsök veterinär.
Ägare rekommenderas att kontrollera hunden med avseende på tecken i ögonen (såsom blinkning, rodnad och sekret från ögonen) under timmarna och dagarna efter applicering av läkemedlet, samt att omedelbart kontakta veterinär om tecken uppstår. Se avsnittet ”Biverkningar” för mer information om ögonbiverkningar hos hundar.
Säkerhet och effekt av läkemedlet hos katter har inte utvärderats. Efter lansering har det visats att användningen av läkemedlet hos katter kan vara förknippad med neurologisk påverkan (inklusive Horners syndrom med framfall av blinkhinnan, små pupiller, olika storlekar på pupillerna och störningar i innerörat som kan ge svårigheter att samordna kroppsrörelser och lutning av huvudet) och systemisk påverkan (aptitlöshet och slöhet). Användning av läkemedlet hos katter bör därför undvikas.
Särskilda försiktighetsåtgärder för personer som ger läkemedlet till djur:
Läkemedlet kan irritera ögonen. Oavsiktlig exponering av ögonen kan inträffa när hunden skakar på huvudet under eller strax efter administrering. För att undvika denna risk för ägare, rekommenderas det att läkemedlet endast administreras av veterinärer eller under noggrann övervakning av veterinär. Lämpliga åtgärder (t.ex. att använda skyddsglasögon under administrering, att noga massera hörselgången efter administrering för att säkerställa jämn fördelning av läkemedlet, att hålla hunden på plats efter administrering) är nödvändiga för att undvika exponering i ögonen.
Vid oavsiktlig exponering av ögonen ska ögonen noga sköljas med vatten i 10–15 minuter. Om symtom utvecklas, uppsök genast läkare och visa bipacksedeln eller etiketten.
Vid oavsiktligt spill på huden, tvätta noga med vatten.
Vid oavsiktligt intag hos människa, uppsök genast läkare och visa bipacksedeln eller etiketten.
Dräktighet och digivning:
Laboratoriestudier har visat belägg för teratogena effekter associerade med betametason på laboratoriedjur.
Säkerheten för detta läkemedel har inte fastställts under dräktighet och digivning hos dräktiga och digivande tikar.
Använd inte under dräktighet och laktation.
Fertilitet:
Använd inte till avelsdjur.
Interaktioner med andra läkemedel och övriga interaktioner:
Kompatibilitet med andra öronrengöringsmedel än natriumkloridlösning har inte påvisats.
Överdosering:
Långvarig eller intensiv användning av läkemedlet kan orsaka blåsbildning på trumhinnans ytvävnad eller slemhinnesår på ytan av mellanörats hålrum. Dessa fynd påverkar inte hörseln och är övergående.
Långvarig och intensiv användning av lokalt applicerade kortikosteroidberedningar är känd för att ge generella effekter i kroppen, inklusive hämmad binjurefunktion.
SÄRSKILDA FÖRSIKTIGHETSÅTGÄRDER FÖR DESTRUKTION AV EJ ANVÄNT LÄKEMEDEL ELLER AVFALL, I FÖREKOMMANDE FALL
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall.
Använd retursystem för kassering av ej använt läkemedel eller avfall från läkemedelsanvändningen i enlighet med lokala bestämmelser. Dessa åtgärder är till för att skydda miljön.
Fråga veterinär eller apotekspersonal hur man gör med läkemedel som inte längre används.
DATUM DÅ BIPACKSEDELN SENAST GODKÄNDES
24.10.2025
Utförlig information om detta läkemedel finns i unionens produktdatabas (https://medicines.health.europa.eu/veterinary).
Detta läkemedel är en fast kombination av tre aktiva substanser: antibiotikum, läkemedel mot svamp och kortikosteroid.
NAMN PÅ OCH ADRESS TILL INNEHAVAREN AV GODKÄNNANDE FÖR FÖRSÄLJNING OCH NAMN PÅ OCH ADRESS TILL INNEHAVAREN AV TILLVERKNINGSTILLSTÅND SOM ANSVARAR FÖR FRISLÄPPANDE AV TILLVERKNINGSSATS, OM OLIKA
Innehavare av godkännande för försäljning och kontaktuppgifter för att rapportera misstänkta biverkningar:
Dechra Regulatory B.V.
Handelsweg 25
5531 AE Bladel
Nederländerna
Tillverkare ansvarig för frisläppande av tillverkningssats:
Argenta Dundee Limited
Kinnoull Road
Dunsinane Industrial Estate
Dundee DD2 3XR
Storbritannien
Genera d.d.
Svetonedeljska cesta 2
Kalinovica
10436 Rakov Potok
Kroatien