Pakkausseloste
EFLUELDA TETRA injektionsvätska, suspension i förfylld spruta 60 mikrog HA/0,7 ml
Tilläggsinformation
Efluelda Tetra, injektionsvätska, suspension i förfylld spruta
Vaccin mot influensa (spjälkat virus), inaktiverat, 60 mikrogram HA/stam
Utökad övervakning
▼Detta läkemedel är föremål för utökad övervakning. Detta kommer att göra det möjligt att snabbt identifiera ny säkerhetsinformation. Du kan hjälpa till genom att rapportera de biverkningar du eventuellt får. Information om hur du rapporterar biverkningar finns i slutet av avsnitt Eventuella biverkningar.
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du vaccineras. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare, apotekspersonal eller sjuksköterska.
- Detta vaccin har ordinerats enbart åt dig. Ge det inte till andra.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
- Vad Efluelda Tetra är och vad det används för
- Vad du behöver veta innan du använder Efluelda Tetra
- Hur du använder Efluelda Tetra
- Eventuella biverkningar
- Hur Efluelda Tetra ska förvaras
- Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Efluelda Tetra är ett vaccin. Detta vaccin hjälper till att skydda personer från 60 års ålder mot influensa. Användning av Efluelda Tetra ska baseras på officiella rekommendationer om vaccination mot influensa.
När en person blir vaccinerad med Efluelda Tetra börjar immunförsvaret (kroppens naturliga försvarssystem) att producera ett eget skydd (antikroppar) mot sjukdomen. Innehållsämnena i vaccinet kan inte orsaka influensa.
Influensa är en smittsam luftvägssjukdom orsakad av influensavirus. Sjukdomen kan variera från lindrig till svår och kan resultera i allvarliga komplikationer, såsom lunginflammation, vilket kan leda till sjukhusinläggning eller till och med döden. Influensa är en sjukdom som kan spridas snabbt och som orsakas av olika virusstammar som kan förändras varje år. Baserat på att dessa cirkulerande virusstammar kan förändras årligen och även på grund av varaktigheten av det skydd som du får av vaccinet rekommenderas vaccination varje år. Störst risk att smittas av influensa föreligger under de kalla månaderna mellan oktober och mars. Om du inte vaccinerades under hösten är det fortfarande klokt att vaccineras ända fram till våren eftersom du fortfarande riskerar att smittas av influensa. Läkaren kan rekommendera den lämpligaste tiden för dig att bli vaccinerad.
Efluelda Tetra är avsett att skydda dig mot de fyra virusstammar som ingår i vaccinet och börjar verka ungefär två till tre veckor efter injektionen. Om du utsätts för influensavirus precis innan eller efter vaccinationen, skulle du fortfarande kunna utveckla sjukdomen, eftersom inkubationsperioden (perioden från smittotillfället till dess att du uppvisar symtom) för influensa är några dagar.
Vaccinet skyddar dig inte mot vanlig förkylning, trots att vissa symtom påminner om influensa.
Vad du behöver veta innan produkten används
För att säkerställa att Efluelda Tetra är lämpligt för dig är det viktigt att informera läkare eller apotekspersonal om någon av nedanstående punkter gäller för dig. Om det är något du inte förstår, be läkare eller apotekspersonal att förklara.
Använd inte Efluelda Tetra
- om du är allergisk mot
- aktiva substanser eller
- något annat innehållsämne i detta vaccin (anges i avsnitt Förpackningens innehåll och övriga upplysningar), eller
- någon beståndsdel som kan finnas i mycket liten mängd, såsom ägg (ovalbumin, hönsprotein) och formaldehyd.
Varningar och försiktighet
Tala med läkare, apotekspersonal eller sjuksköterska innan du använder Efluelda Tetra.
Tala om för läkare före vaccinationen om du har:
- nedsatt immunförsvar (har en immunbrist eller tar läkemedel som påverkar immunförsvaret)
- problem med blödning eller lätt får blåmärken
- fått Guillain-Barrés syndrom (svår muskelsvaghet) efter att du vaccinerats mot influensa
- en sjukdom med hög eller måttlig feber eller en akut sjukdom; vaccinationen ska skjutas upp tills du blivit frisk igen.
Läkaren kommer att avgöra om du ska få vaccinet.
Svimning kan förekomma efter, eller till och med före, nålsticket. Tala därför om för läkare eller sjuksköterska om du tidigare har svimmat i samband med nålstick.
Liksom för alla vacciner finns risken att Efluelda Tetra kanske inte ger fullt skydd hos alla som vaccineras.
Tala om för din läkare om du av någon anledning lämnar blodprov inom några dagar efter en influensavaccination. Detta ska göras eftersom falskt positivt blodprov har observerats hos ett fåtal patienter som nyligen blivit vaccinerade.
Barn
Detta vaccin ska inte användas för barn. Det ska endast användas för vuxna från 60 års ålder.
Andra läkemedel och Efluelda Tetra
Tala om för läkaren eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra vacciner eller andra läkemedel.
- Om Efluelda Tetra ges vid samma tillfälle som andra vacciner, ska vaccinerna alltid ges i olika armar eller ben.
- Det ska noteras att biverkningarna kan förstärkas vid samtidig administrering.
- Immunsvaret kan bli sämre vid behandling med läkemedel som hämmar immunförsvaret, till exempel kortikosteroider (kortison), cellgifter eller strålbehandling.
Graviditet och amning
Efluelda Tetra är enbart avsett för vuxna från 60 års ålder.
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du använder detta vaccin. Läkare eller apotekspersonal kan avgöra om du ska få Efluelda Tetra.
Körförmåga och användning av maskiner
Efluelda Tetra har ingen eller försumbar effekt på förmågan att framföra fordon eller använda maskiner.
Du bör dock inte framföra fordon om du känner dig sjuk eller yr.
Du är själv ansvarig för att bedöma om du är i kondition att framföra motorfordon eller utföra arbeten som kräver skärpt uppmärksamhet. En av faktorerna som kan påverka din förmåga i dessa avseenden är användning av läkemedel på grund av deras effekter och/eller biverkningar. Beskrivning av dessa effekter och biverkningar finns i andra avsnitt. Läs därför all information i denna bipacksedel för vägledning. Diskutera med läkare eller apotekspersonal om du är osäker.
Efluelda Tetra innehåller natrium
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per dos, d.v.s. är näst intill ”natriumfritt’.
Hur produkten används
Vuxna från 60 års ålder får en dos på 0,7 ml.
Hur Efluelda Tetra ges
Läkaren, apotekspersonalen eller sjuksköterskan ger rekommenderad dos av vaccinet som en injektion i en muskel eller under huden.
Om du har ytterligare frågor om detta läkemedel, kontakta läkare eller apotekspersonal.
Eventuella biverkningar
Liksom alla läkemedel kan detta vaccin orsaka biverkningar, men alla användare behöver inte få dem.
Allergiska reaktioner
Uppsök OMEDELBART läkare om du upplever följande:
- Allvarliga allergiska reaktioner:
- som kan leda till akuta besvär med lågt blodtryck, andnöd, väsande andning eller andningssvårigheter, snabb hjärtrytm och svag puls, kall och fuktig hud, yrsel som kan leda till kollaps (anafylaxi [inklusive angioödem, dvs. svullnad som främst uppstår på huvudet och i halsen, inkluderat ansikte, läppar, tunga, svalg eller andra delar av kroppen och som kan leda till svårigheter att svälja eller andas]).
Uppsök läkare om du upplever följande:
- Allergiska reaktioner såsom hudreaktioner som kan sprida sig över kroppen med klåda, nässelutslag, hudutslag.
Dessa biverkningar är sällsynta (kan förekomma hos upp till 1 av 1 000 personer).
Andra rapporterade biverkningar
Biverkningarna nedan rapporterades hos vuxna från 60 års ålder.
Mycket vanliga (kan förekomma hos fler än 1 av 10 personer)
- reaktioner vid injektionsstället: smärta, rodnad (erytem)
- allmän sjukdomskänsla, huvudvärk, muskelvärk (myalgi).
Vanliga (kan förekomma hos upp till 1 av 10 personer):
- reaktioner vid injektionsstället: svullnad, blåmärken, förhårdnad (induration)
- feber, frossa.
Mindre vanliga (kan förekomma hos upp till 1 av 100 personer):
- reaktioner vid injektionsstället: klåda
- trötthet, matthet (letargi), illamående, kräkningar, diarré
- hosta, muskelsvaghet, matsmältningsbesvär (dyspepsi), inflammation i halsen (orofaryngeal smärta).
Sällsynta (kan förekomma hos upp till 1 av 1 000 personer):
- onormal brist på energi (asteni), rodnad, ledsmärta (artralgi), yrsel, nattlig svettning, hudutslag, domningar eller stickningar (parestesi), inflammation i näsan (rinorré), svindel (vertigo), ökad mängd blod i ögonvitan (okulär hyperemi)
- smärta i armar och ben.
Har rapporterats (förekommer hos ett okänt antal användare):
- minskat antal av en viss sorts blodkroppar s.k. blodplättar; ett lågt antal av dessa kan orsaka en ökad tendens att få blåmärken eller blödningar (trombocytopeni)
- svullna körtlar i hals, armhåla eller ljumske (lymfadenopati)
- neurologiska störningar som kan orsaka nackstelhet, förvirring, domningar, smärta och svaghet i armar och ben, försämrad balans, försämrade reflexer, förlamning i delar av eller hela kroppen (encefalomyelit, transversell myelit, brakial neurit, Guillain-Barrés syndrom), ansiktsförlamning (Bells pares), synstörningar på grund av störning i synnerverna (optikusneurit/neuropati), kramper (inklusive feberkramper), svimning (synkope) kort efter vaccinationen
- kärlinflammation i blodkärlen (vaskulit), som kan leda till hudutslag och i mycket sällsynta fall övergående njurproblem, kärlutvidgning (vasodilatation)
- bröstsmärta
- väsande andning, trånghetskänsla i halsen, andningssvårigheter (dyspné).
De flesta biverkningarna uppstod vanligtvis inom tre dagar efter vaccinationen och försvann av sig själva inom tre dagar. Biverkningarna var lindriga till måttliga.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta vaccin utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på etiketten och kartongen efter "EXP". Utgångsdatumet är den sista dagen i angiven månad.
Förvaras i kylskåp (2 °C – 8 °C). Får ej frysas. Förvara sprutan i ytterkartongen. Ljuskänsligt.
Vacciner ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar vacciner som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- De aktiva substanserna är: Influensavirus (inaktiverat, spjälkat) av följande stammar*:
A/Victoria/4897/2022 (H1N1)pdm09 - liknande stam (A/Victoria/4897/2022, IVR-238)............................................................60 mikrogram HA**
A/Thailand/8/2022 (H3N2) - liknande stam (A/California/122/2022, SAN-022).....................................................................................60 mikrogram HA**
B/Austria/1359417/2021 - liknande stam (B/Michigan/01/2021, vildtyp) ..................................................................................60 mikrogram HA**
B/Phuket/3073/2013 - liknande stam (B/Phuket/3073/2013, vildtyp) ........................................................................................60 mikrogram HA**
Per 0,7 ml dos
* framställda ur befruktade hönsägg
** hemagglutinin
Detta vaccin överensstämmer med rekommendationer från WHO (Världshälsoorganisationen, norra hemisfären) och beslut inom EU för säsongen 2024/2025.
Övriga innehållsämnen: en buffertlösning innehållande natriumklorid, natriumdivätefosfat, dinatriumfosfat, vatten för injektionsvätskor och oktoxinol-9.
Vissa beståndsdelar såsom ägg (ovalbumin, hönsprotein) eller formaldehyd kan förekomma i mycket små mängder (se avsnitt Vad du behöver veta innan produkten används).
Läkemedlets utseende och förpackningsstorlekar
Efter försiktig omskakning är vaccinet en färglös och opaliserande vätska.
Efluelda Tetra är en 0,7 ml injektionsvätska, suspension i en förfylld spruta med eller utan nål (i en kartong om 1, 5 eller 10) eller med en nål med nålskydd (i en kartong om 1 eller 10).
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning och tillverkare
Innehavare av godkännande för försäljning:
Sanofi Winthrop Industrie
82 avenue Raspail
94250 Gentilly
Frankrike
Tillverkare:
Sanofi Winthrop Industrie
Voie de l’Institut - Parc Industriel d’Incarville
B.P 101
27100 Val de Reuil
Frankrike
Lokal representant:
Sanofi Oy
Norrskensgränden 1
02100 Esbo
Tel: +358 (0) 201 200 300
Denna bipacksedel ändrades senast 10.03.2025
Övriga informationskällor
Den senaste godkända informationen om detta läkemedel finns tillgänglig genom att skanna QR-koden på den yttre förpackningen med en smarttelefon eller på adressen https://efluelda-nh.info.sanofi
Direktiv för experterna inom hälsovården
Följande uppgifter är endast avsedda för hälso- och sjukvårdspersonal:
Liksom med alla injicerbara vacciner ska lämplig medicinsk behandling och övervakning alltid finnas lätt tillgänglig om en anafylaktisk reaktion skulle inträffa efter administrering av vaccinet.
Vaccinet ska anta rumstemperatur före användning.
Omskakas före användning. Kontrolleras visuellt före användning.
Vaccinet ska inte användas om det finns främmande partiklar i suspensionen.
Vaccinet ska inte blandas med andra läkemedel i samma spruta.
Vaccinet får inte injiceras rakt in i ett blodkärl.
Se även avsnitt Hur produkten används. Hur du använder Efluelda Tetra
<Förberedelse för administrering
Bruksanvisning för användning av förfylld Luer Lock-spruta med nålskydd:
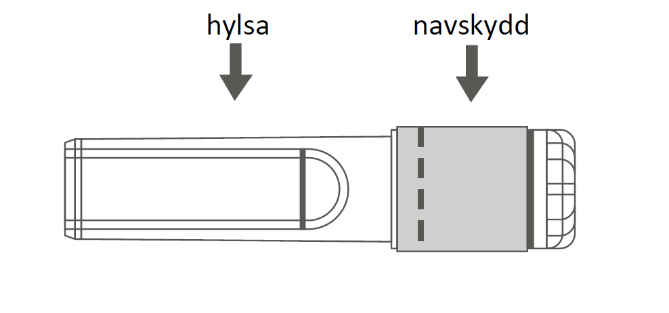
| Bild A: Nål med nålskydd (inuti hylsa) | Bild B: Delar av nål med nålskydd (förberett för användning) |
 |
|
| Steg 1: Fäst nålen vid sprutan genom att ta bort navskyddet så att du ser nålens nav och vrid sedan försiktigt fast nålen i Luer Lock-kopplingen på sprutan, tills du känner ett litet motstånd. | ||
| Steg 2: Dra av nålskyddets hylsa rakt av. Nålen täcks av nålskyddet och skyddsdelen. | ||
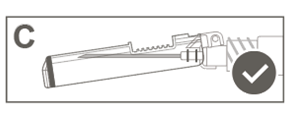
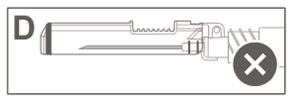
Steg 3: A: Lyft nålskyddet bort från nålen och bakåt mot sprutcylindern till den vinkel som visas i bilden. B: Dra av skyddsdelen rakt från nålen. | 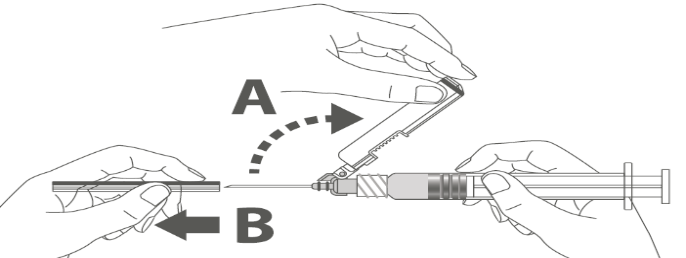 | |
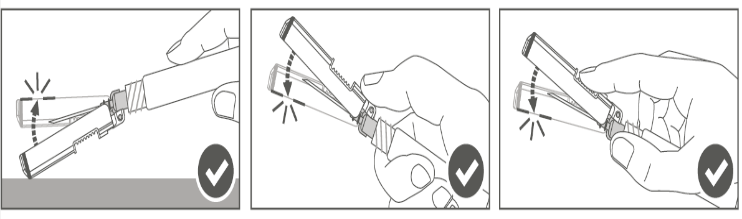
Steg 4: Efter injektionen ska nålskyddet låsas (aktiveras) genom att använda en av de tre (3) enhandsteknikerna som visas i bilden: aktivering mot en yta, med tummen eller med fingret. Observera: Aktiveringen har lyckats när du hör och/eller känner ett ”klick”.
|  | |
Steg 5: Kontrollera visuellt att nålskyddet har aktiverats. Nålskyddet ska vara helt låst (aktiverat) såsom visas i bild C
I bild D visas ett nålskydd som INTE är helt låst (inte aktiverat).
|
| |
| Varning: Försök inte låsa upp (avaktivera) skyddsmekanismen genom att tvinga ut nålen från nålskyddet. | ||
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar. ˃