Pakkausseloste
EFLUELDA TETRA injektioneste, suspensio, esitäytetty ruisku 60 mikrog HA/0,7 ml
Efluelda Tetra, injektioneste, suspensio, esitäytetty ruisku
Influenssarokote (virusfragmentit, inaktivoitu), 60 mikrogrammaa HA / kanta
Lisäseuranta
▼Tähän lääkkeeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti turvallisuutta koskevaa uutta tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista. Ks. kohdan Mahdolliset haittavaikutukset lopusta, miten haittavaikutuksista ilmoitetaan.
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin sinulle annetaan tämä rokote, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
- Tämä rokote on määrätty vain sinulle, eikä sitä tule antaa muiden käyttöön.
- Jos havaitset haittavaikutuksia, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
- Mitä Efluelda Tetra on ja mihin sitä käytetään
- Mitä sinun on tiedettävä, ennen kuin sinulle annetaan Efluelda Tetra -rokote
- Miten Efluelda Tetra -rokotetta käytetään
- Mahdolliset haittavaikutukset
- Efluelda Tetra -rokotteen säilyttäminen
- Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Efluelda Tetra on rokote. Tämä rokote suojaa vähintään 60-vuotiaita henkilöitä influenssalta. Efluelda Tetra -rokotteen käytön pitää perustua influenssarokotuksia koskeviin virallisiin suosituksiin.
Kun henkilölle annetaan Efluelda Tetra -rokote, immuunijärjestelmä (elimistön luonnollinen puolustusjärjestelmä) tuottaa itse suojan (vasta-aineita) tautia vastaan. Mikään rokotteen sisältämistä aineista ei voi aiheuttaa influenssaa.
Influenssa on influenssavirusten aiheuttama tarttuva hengityselinsairaus, joka voi olla lievä tai vaikea tauti. Influenssa saattaa aiheuttaa sairaalahoitoa vaativia tai jopa kuolemaan johtavia vakavia komplikaatioita, kuten keuhkokuumetta. Influenssa on sairaus, joka voi levitä nopeasti ja sitä aiheuttaa eri viruskannat, jotka voivat muuttua joka vuosi. Tämän kiertävien kantojen mahdollisen vuosittaisen muuttumisen sekä rokotteen tarjoaman suojan keston vuoksi rokote on suositeltavaa ottaa joka vuosi. Influenssaan sairastumisen riski on suurimmillaan kylminä kuukausina, lokakuusta maaliskuuhun. Jos sinua ei ole rokotettu syksyllä, rokotuksen ottaminen on silti järkevää kevääseen saakka, koska influenssatartunnan mahdollisuus on olemassa siihen asti. Lääkäri pystyy suosittelemaan sinulle parhaan rokotusajankohdan.
Efluelda Tetra on tarkoitettu suojaamaan sinua neljää rokotteen sisältämää viruskantaa vastaan ja sen antama suoja alkaa noin 2–3 viikon kuluttua rokotuksesta. Jos altistut kuitenkin influenssalle välittömästi ennen rokotusta tai sen jälkeen, sinulle voi kehittyä influenssasairaus, koska influenssan itämisaika on muutamia päiviä.
Rokote ei suojaa sinua tavalliselta nuhakuumeelta, vaikka jotkin sen oireista ovat hyvin samankaltaisia kuin influenssan oireet.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Efluelda Tetra -rokotteen sopivuuden varmistamiseksi on tärkeää, että kerrot lääkärille tai apteekkihenkilökunnalle, jos jokin seuraavista kohdista koskee sinua. Jos et ymmärrä jotakin asiaa, pyydä lääkäriä tai apteekkihenkilökuntaa selittämään se.
Älä käytä Efluelda Tetra -rokotetta:
- jos olet allerginen:
- vaikuttaville aineille tai
- tämän rokotteen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa) tai
- jollekin aineelle, jota rokotteessa voi olla hyvin pieniä määriä, kuten kananmunalle (ovalbumiinille tai kanan proteiineille) tai formaldehydille.
Varoitukset ja varotoimet
Keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen Efluelda Tetra -rokotteen ottamista.
Sinun on kerrottava lääkärille ennen rokotusta:
- jos sinulla on heikko immuunivaste (sinulla on immuunivajavuustila tai käytät immuunijärjestelmään vaikuttavia lääkkeitä)
- jos sinulla on verenvuotohäiriö tai saat helposti mustelmia
- jos sinulla on ilmennyt Guillain-Barrén oireyhtymä (vaikea lihasheikkous) influenssarokotteen saamisen jälkeen
- jos sinulla on sairaus, johon liittyy korkea tai kohtalainen kuume, tai akuutti sairaus; rokotusta on lykättävä, kunnes olet toipunut.
Lääkäri päättää, voitko saada rokotteen.
Pyörtymistä voi ilmetä minkä tahansa neulalla annetun pistoksen jälkeen tai jopa sitä ennen. Siksi sinun on kerrottava lääkärille tai hoitajalle, jos olet pyörtynyt aiemmin pistoksen saamisen yhteydessä.
Kaikkien muiden rokotteiden tavoin Efluelda Tetra ei välttämättä anna täydellistä suojaa kaikille rokotetuille henkilöille.
Kerro lääkärille, jos sinulta otetaan jostakin syystä verinäyte muutaman päivän kuluessa influenssarokotteen saamisen jälkeen. Tämä on tarpeen, sillä joillakin harvoilla potilailla verikokeiden tuloksissa on havaittu vääriä positiivisia tuloksia, kun näyte on otettu pian rokotuksen jälkeen.
Lapset
Tätä rokotetta ei pidä käyttää lapsille. Se on tarkoitettu ainoastaan vähintään 60‑vuotiaille aikuisille.
Muut lääkevalmisteet ja Efluelda Tetra
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät tai olet äskettäin käyttänyt tai saatat käyttää muita rokotteita tai muita lääkkeitä.
- Jos Efluelda Tetra -rokote annetaan samanaikaisesti muiden rokotteiden kanssa, pistokset on aina annettava eri raajoihin.
- On otettava huomioon, että haittavaikutukset saattavat olla voimakkaampia samanaikaisen annon yhteydessä.
- Immunologinen vaste saattaa heikentyä, jos potilas saa immuunivastetta heikentävää hoitoa, kuten kortikosteroideja, solunsalpaajia tai sädehoitoa.
Raskaus ja imetys
Efluelda Tetra on tarkoitettu vain vähintään 60‑vuotiaille aikuisille.
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän rokotteen käyttöä. Lääkäri/apteekkihenkilökunta auttaa sinua päättämään, kannattaako sinun ottaa Efluelda Tetra -rokote.
Ajaminen ja koneiden käyttö
Efluelda Tetra -rokotteella ei ole haitallista vaikutusta ajokykyyn tai koneidenkäyttökykyyn. Ei kuitenkaan ole järkevää ajaa, jos sinulla ilmenee huonovointisuutta tai huimausta.
Olet itse vastuussa sen arvioimisesta, kykenetkö ajamaan autoa tai suorittamaan erityistä tarkkuutta vaativia tehtäviä. Lääkkeiden vaikutukset ja/tai haittavaikutukset voivat vaikuttaa toimintakykyysi. Tämän lääkkeen vaikutuksista ja haittavaikutuksista on kerrottu tämän pakkausselosteen muissa kohdissa. Lue koko pakkausseloste huolellisesti saadaksesi tietoa mahdollisista toimintakykyysi vaikuttavista tekijöistä. Keskustele lääkärin tai apteekkihenkilökunnan kanssa, jos olet epävarma.
Efluelda Tetra sisältää natriumia
Tämä lääkevalmiste sisältää alle 1 mmol (23 mg) natriumia per annos eli sen voidaan sanoa olevan ”natriumiton”.
Miten valmistetta käytetään
Vähintään 60‑vuotiaat aikuiset saavat yhden 0,7 ml:n annoksen.
Miten Efluelda Tetra annetaan
Lääkäri, apteekkihenkilökunta tai hoitaja antaa suositellun annoksen rokotetta pistoksena lihakseen tai ihon alle.
Jos sinulla on kysymyksiä tämän valmisteen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin rokote voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Allergiset reaktiot
Käänny VÄLITTÖMÄSTI lääkärin puoleen, jos sinulla ilmenee:
- vaikea allerginen reaktio:
- vaikeat allergiset reaktiot saattavat aiheuttaa lääketieteellisen hätätilanteen, johon liittyy matala verenpaine, hengenahdistus, hengityksen vinkuminen tai hengitysvaikeus, nopea sydämen syke ja heikko syke, kylmänhikinen iho tai heitehuimaus, joka saattaa johtaa pyörtymiseen (anafylaktinen reaktio [mukaan lukien angioedeema eli tila, johon liittyy turvotusta, joka on selvimmin havaittavissa pään ja kaulan alueella, kuten kasvoissa, huulissa, kielessä tai nielussa, tai muualla kehossa ja joka saattaa aiheuttaa nielemis- tai hengitysvaikeuksia]).
Käänny lääkärin puoleen, jos sinulla ilmenee:
- allerginen reaktio, kuten ihoreaktio, joka saattaa levitä koko kehoon, kutina, nokkosihottuma ja ihottuma mukaan lukien.
Nämä haittavaikutukset ovat harvinaisia (niitä saattaa ilmetä enintään 1 henkilöllä tuhannesta).
Muita ilmoitettuja haittavaikutuksia
Seuraavia haittavaikutuksia on ilmoitettu vähintään 60‑vuotiailla aikuisilla.
Hyvin yleiset (yli 1 henkilöllä kymmenestä):
- reaktiot pistoskohdassa: kipu, punoitus
- yleinen huono olo (huonovointisuus), päänsärky, lihaskipu
Yleiset (enintään 1 henkilöllä kymmenestä)
- reaktiot pistoskohdassa: turvotus, mustelma, kovettuma
- kuume, vilunväristykset
Melko harvinaiset (enintään 1 henkilöllä sadasta)
- reaktiot pistoskohdassa: kutina
- väsymys, uneliaisuus (letargia), pahoinvointi, oksentelu, ripuli
- yskä, lihasheikkous, ruuansulatushäiriö (dyspepsia), nielutulehdus (kipu suun ja nielun alueella)
Harvinaiset (enintään 1 henkilöllä tuhannesta):
- epätavallinen voimattomuus (astenia), punoitus, nivelkipu (artralgia), heitehuimaus, yöhikoilu, ihottuma, puutuminen tai pistelyn tunne (parestesia), nenän tulehdus (voimakas nuha), huimaus, silmänvalkuaisen lisääntynyt verekkyys (silmän hyperemia)
- kipu raajoissa
Tuntematon: saatavissa oleva tieto ei riitä esiintyvyyden arviointiin
- tietyn tyyppisten, verihiutaleiksi kutsuttujen verihiukkasten väheneminen: niiden vähäinen määrä voi johtaa mustelmien tai verenvuodon lisääntymiseen (trombosytopenia)
- kaulassa, kainaloissa tai nivusissa olevien rauhasten turpoaminen (lymfadenopatia)
- hermoston häiriöt, jotka saattavat aiheuttaa niskan jäykkyyttä, sekavuutta, puutumista, kipua ja heikkoutta raajoissa, tasapainohäiriöitä, refleksien häviämistä, kehon osan tai koko kehon halvaantumista (enkefalomyeliitti, transversaalimyeliitti, hartiapunoksen neuriitti, Guillain-Barrén oireyhtymä), kasvohalvausta (Bellin pareesi), näköhermojen toimintahäiriöstä johtuvia näköhäiriöitä (näköhermotulehdus/neuropatia), kouristuskohtauksia (kuumekouristukset mukaan lukien), pyörtymistä pian rokottamisen jälkeen
- verisuonitulehdus (vaskuliitti), joka saattaa aiheuttaa ihottumaa ja hyvin harvinaisissa tapauksissa tilapäisiä munuaisvaivoja, verisuonten laajeneminen (vasodilataatio)
- rintakipu
- hengityksen vinkuminen, kuristava tunne kurkussa, hengitysvaikeudet (hengenahdistus)
Useimmat haittavaikutukset ilmenivät yleensä ensimmäisten kolmen vuorokauden sisällä rokotuksen jälkeen ja hävisivät 3 vuorokauden kuluessa. Nämä haittavaikutukset olivat voimakkuudeltaan lieviä tai kohtalaisia.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä rokotetta etiketissä ja kotelossa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Säilytä jääkaapissa (2 °C – 8 °C). Ei saa jäätyä. Pidä ruisku ulkopakkauksessa. Herkkä valolle.
Rokotteita ei tule heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien rokotteiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä Efluelda Tetra sisältää
- Vaikuttavat aineet ovat: Influenssavirus (inaktivoitu, fragmentoitu) seuraavista kannoista*:
Kannan A/Victoria/4897/2022 (H1N1) pdm09 kaltainen virus (A/Victoria/4897/2022, IVR-238)
............................................................................................................................60 mikrogrammaa HA**
Kannan A/Thailand/8/2022 (H3N2) kaltainen virus (A/California/122/2022, SAN-022)
............................................................................................................................60 mikrogrammaa HA**
Kannan B/Austria/1359417/2021 kaltainen virus (B/Michigan/01/2021, villityyppi)
............................................................................................................................60 mikrogrammaa HA**
Kannan B/Phuket/3073/2013 kaltainen virus (B/Phuket/3073/2013, villityyppi)
...........................................................................................................................60 mikrogrammaa HA**
0,7 ml:n annoksessa
* kasvatettu hedelmöitetyissä kananmunissa
** hemagglutiniini
Rokote on WHO:n (Maailman terveysjärjestön) suositusten (pohjoinen pallonpuolisko) ja EU:n päätöksen mukainen kaudelle 2024/2025.
Muut aineet ovat: puskuriliuos, joka sisältää natriumkloridia, yksiemäksistä natriumfosfaattia, kaksiemäksistä natriumfosfaattia, injektionesteisiin käytettävää vettä ja oktoksinoli-9:ää.
Rokotteessa saattaa olla hyvin pieniä määriä joitakin aineita, kuten kananmunaa (ovalbumiinia tai kanan proteiineja) tai formaldehydiä (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä).
Lääkevalmisteen kuvaus ja pakkauskoot
Rokote on kevyen ravistamisen jälkeen väritön opaalinhohtoinen neste.
Efluelda Tetra: 0,7 ml injektionestettä, suspensiota, esitäytetyssä ruiskussa neulan kanssa tai ilman neulaa (pakkauskoot: 1, 5 tai 10) tai turvaneulan kanssa (pakkauskoot: 1 tai 10).
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija ja valmistaja
Myyntiluvan haltija:
Sanofi Winthrop Industrie
82 avenue Raspail
94250 Gentilly
Ranska
Valmistaja:
Sanofi Winthrop Industrie
Voie de l’Institut - Parc Industriel d’Incarville
B.P 101
27100 Val de Reuil
Ranska
Paikallinen edustaja:
Sanofi Oy
Revontulenkuja 1
02100 Espoo
Puh.: +358 (0) 201 200 300
Tämä pakkausseloste on tarkistettu viimeksi 10.03.2025
Muut tiedonlähteet
Viimeisimmät hyväksytyt tiedot tästä valmisteesta ovat saatavilla ulkopakkauksessa olevan QR-koodin kautta älypuhelimella tai osoitteessa https://efluelda-nh.info.sanofi
Ohjeet terveydenhuollon ammattilaiselle
Seuraavat tiedot on tarkoitettu vain terveydenhuollon ammattilaisille:
Kuten aina injektoitavia rokotteita annettaessa, pitää asianmukaisen hoidon ja valvonnan olla helposti saatavilla rokotuksen jälkeen mahdollisesti ilmenevän anafylaktisen reaktion varalta.
Rokotteen on annettava lämmetä huoneenlämpöön ennen käyttöä.
Ravista ennen käyttöä. Tarkasta silmämääräisesti ennen antoa.
Rokotetta ei saa käyttää, jos suspensiossa on vierashiukkasia.
Rokotetta ei saa sekoittaa samassa ruiskussa muiden lääkevalmisteiden kanssa.
Tätä rokotetta ei saa antaa verisuoneen.
Ks. myös kohta Miten valmistetta käytetään. Miten Efluelda Tetra -rokotetta käytetään
<Valmistelut ennen antamista
Ohjeet turvaneulan käytölle esitäytetyn Luer Lock ‑ruiskun kanssa:
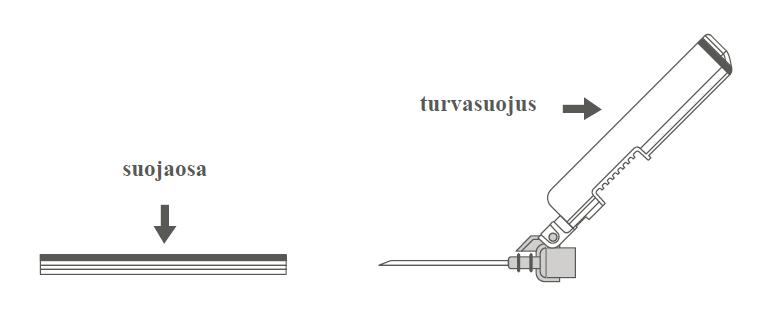
| Kuva A: Turvaneula (kotelossa) | Kuva B: Turvaneulan osat (valmisteltuna käyttöä varten) |
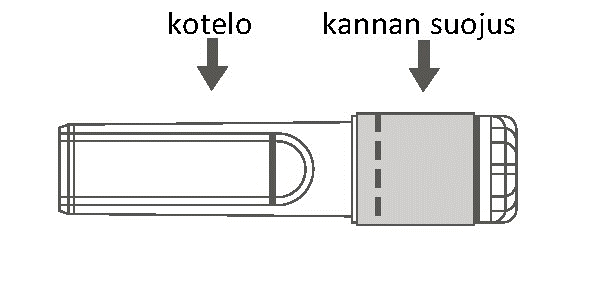 |  |
| Vaihe 1: Kiinnitä neula ruiskuun seuraavasti: Poista kannan suojus, niin että neulan kanta tulee näkyviin, ja kierrä neulaa varovasti ruiskun Luer Lock ‑liittimeen, kunnes tunnet vähäisen vastuksen. | ||
| Vaihe 2: Poista turvaneulan kotelo vetämällä kohtisuoraan. Neula on turvasuojuksen ja suojaosan sisällä. | ||
Vaihe 3: A: Käännä turvasuojusta poispäin neulasta, kohti ruiskun sylinteriä kuvassa esitettyyn asentoon. B: Poista suojaosa vetämällä kohtisuoraan. | 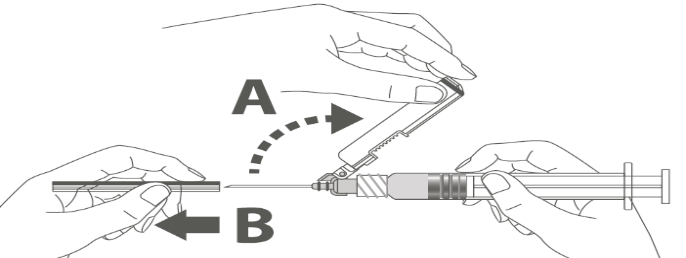 | |
Vaihe 4: Kun pistos on annettu, lukitse (aktivoi) turvasuojus käyttämällä jotakin kolmesta (3) yhden käden tekniikasta, jotka on esitetty kuvassa, eli aktivoinnilla pintaa vasten, peukalolla tai sormella. Huomaa: Aktivointi on onnistunut, kun kuulet ja/tai tunnet naksahduksen. | 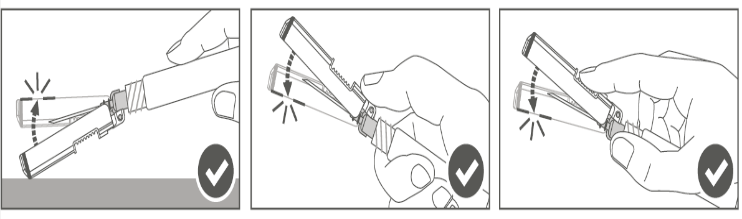 | |
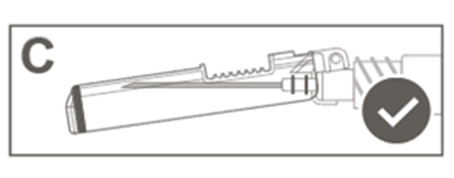
Vaihe 5: Tarkasta turvasuojuksen aktivoituminen silmämääräisesti. Turvasuojuksen on oltava täysin lukkiutunut (aktivoitunut), kuten kuvassa C on esitetty.
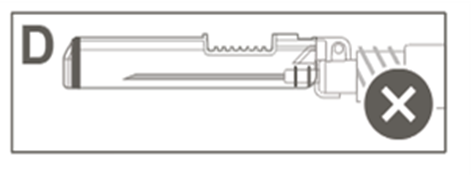
Kuvassa D on turvasuojus, joka EI ole täysin lukkiutunut (ei ole aktivoitunut).
|
| |
| Varoitus: Älä yritä poistaa turvalaitteen lukitusta (peruuttaa turvalaitteen aktivointia) ottamalla neula väkisin pois turvasuojuksesta. | ||
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.˃