LUMIGAN silmätipat, liuos, kerta-annospakkaus 0,3 mg/ml
LUMIGAN 0,3 mg/ml, silmätipat, liuos kerta-annospakkauksessa
bimatoprosti
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti, ennen kuin aloitat tämän lääkkeen käyttämisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
- Tämä lääke on määrätty vain sinulle eikä sitä tule antaa muiden käyttöön. Se voi aiheuttaa haittaa muille, vaikka heillä olisikin samanlaiset oireet kuin sinulla.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
1. Mitä LUMIGAN‑kerta-annosvalmiste on ja mihin sitä käytetään
2. Mitä sinun on tiedettävä, ennen kuin käytät LUMIGAN-kerta-annosvalmistetta
3. Miten LUMIGAN-kerta-annosvalmistetta käytetään
4. Mahdolliset haittavaikutukset
5. LUMIGAN-kerta-annosvalmisteen säilyttäminen
6. Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
LUMIGAN‑kerta-annosvalmiste on glaukoomalääke, ja se kuuluu prostamideiksi kutsuttujen lääkeaineiden ryhmään.
LUMIGAN‑kerta-annossilmätippoja käytetään silmänsisäisen paineen alentamiseen. Sitä voidaan käyttää yksin tai yhdessä toisten silmänsisäistä painetta alentavien tippojen, beetasalpaajien, kanssa.
Silmissä on kirkasta ja vetistä nestettä, joka ruokkii silmän sisäosia. Tätä nestettä virtaa jatkuvasti ulos silmästä ja uutta nestettä valmistuu sen tilalle. Jos neste ei pääse virtaamaan ulos tarpeeksi nopeasti, silmänsisäinen paine nousee. Tämä lääke lisää ulosvirtaavan nesteen määrää, mikä alentaa silmänsisäistä painetta. Jos painetta ei alenneta, se saattaa johtaa glaukooma-nimiseen sairauteen ja mahdollisesti heikentää näköä.
Tämä lääkevalmiste ei sisällä säilytysainetta.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä käytä LUMIGAN-kerta-annosvalmistetta:
- jos olet allerginen bimatoprostille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa).
Varoitukset ja varotoimet
Keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin käytät LUMIGAN-kerta-annosvalmistetta, jos:
- sinulla on hengitysvaikeuksia.
- maksasi tai munuaisesi toimii huonosti.
- sinulle on aiemmin tehty kaihileikkaus.
- sinulla on tai on aiemmin ollut matala verenpaine tai alhainen syke.
- sinulla on ollut silmässä virusinfektio tai tulehdus.
Hoidon aikana LUMIGAN saattaa aiheuttaa silmän ympärillä olevan rasvatyynyn ohenemista, minkä vuoksi luomivako saattaa syventyä, silmä voi painua kuoppaansa (enoftalmia), yläluomi voi riippua (ptoosi), silmänympärysiho voi kiristyä (velton ihon surkastuminen) tai silmän valkuaisen alaosa voi tulla selvemmin esiin (kovakalvon alaosan näkyminen). Muutokset ovat tyypillisesti lieviä, mutta näkyvämmät muutokset voivat vaikuttaa näkökenttään. Muutokset voivat hävitä, jos lopetat LUMIGAN-valmisteen ottamisen. LUMIGAN‑kerta-annosvalmiste saattaa myös aiheuttaa ripsien kasvua ja värin tummumista sekä silmäluomen ympärillä olevan ihon tummumista. Myös silmän värikalvo saattaa tummua. Nämä muutokset saattavat olla pysyviä. Muutokset saattavat olla näkyvämpiä, jos hoidat vain toista silmää.
Lapset ja nuoret
LUMIGAN‑kerta-annosvalmistetta ei ole testattu alle 18-vuotiailla lapsilla ja nuorilla. Sen vuoksi alle 18-vuotiaat eivät saa käyttää tätä valmistetta.
Muut lääkevalmisteet ja LUMIGAN-kerta-annosvalmiste
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan otat, olet äskettäin ottanut tai saatat ottaa muita lääkkeitä.
Raskaus, imetys ja hedelmällisyys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käyttöä.
LUMIGAN-kerta-annosvalmiste saattaa erittyä äidinmaitoon. Imettämistä ei suositella tämän lääkkeen käytön aikana.
Ajaminen ja koneiden käyttö
Näkösi saattaa sumentua tilapäisesti, juuri kun olet käyttänyt LUMIGAN‑kerta-annosvalmistetta. Ennen ajamista tai koneiden käyttöä on odotettava näön selkenemistä.
Miten valmistetta käytetään
Käytä tätä lääkettä juuri siten kuin lääkäri on määrännyt tai apteekkihenkilökunta on neuvonut. Tarkista ohjeet lääkäriltä tai apteekista, jos olet epävarma.
Suositeltu annos on yksi tippa illalla kumpaankin hoidettavaan silmään kerran vuorokaudessa. LUMIGAN‑kerta-annosvalmiste tiputetaan ainoastaan silmään.
Jos käytät LUMIGAN‑kerta-annosvalmistetta muiden silmälääkkeiden kanssa, odota eri silmälääkkeiden annostelun välillä vähintään 5 minuuttia.
Älä käytä useammin kuin kerran vuorokaudessa, sillä hoidon teho voi heikentyä.
Pese kädet ennen valmisteen käyttöä. Tarkista, että kerta-annospakkaus on ehjä ennen käyttöä. Liuos on käytettävä heti avaamisen jälkeen. Kontaminaation välttämiseksi älä anna kerta-annospakkauksen avatun kärjen koskea silmään tai muuhun pintaan.
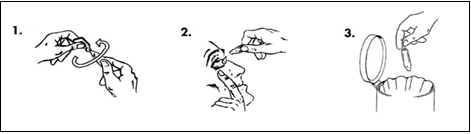
- Irrota yksi kerta-annospakkaus pussista, japidä kerta-annospakkausta pystyssä (repäisykorkki ylöspäin) ja kierrä repäisykorkki irti.
- Vedä alaluomea varovasti alaspäin, kunnes siihen muodostuu pieni tasku. Käännä kerta-annospakkaus ylösalaisin ja purista 1 tippa hoidettavaan silmään (hoidettaviin silmiin).
- Hävitä avattu kerta-annospakkaus käytön jälkeen, vaikka liuosta olisikin vielä jäljellä.
Pyyhi pois mahdollinen poskelle valuva ylimääräinen liuos.
Jos käytät piilolinssejä, poista piilolinssit ennen tämän lääkkeen käyttöä. Odota 15 minuuttia tippojen laittamisen jälkeen, ennen kuin laitat piilolinssit takaisin silmiin.
Jos käytät enemmän LUMIGAN-kerta-annosvalmistetta kuin sinun pitäisi
Jos käytät tätä lääkettä enemmän kuin pitäisi, on epätodennäköistä, että siitä koituisi sinulle mitään vakavaa haittaa. Tiputa seuraava annos normaaliin aikaan. Jos olet asiasta huolestunut, neuvottele siitä lääkärisi tai apteekin kanssa.
Jos unohdat käyttää LUMIGAN-kerta-annosvalmistetta
Jos unohdat käyttää tätä lääkettä, laita yksi tippa silmään heti kun muistat ja palaa sitten normaaliin annosteluun. Älä tiputa kaksinkertaista annosta korvataksesi unohtamasi annoksen.
Jos lopetat LUMIGAN-kerta-annosvalmisteen käytön
LUMIGAN‑kerta-annosvalmistetta on käytettävä joka päivä, jotta se vaikuttaisi asianmukaisella tavalla. Jos lopetat LUMIGAN‑kerta-annosvalmisteen käytön, silmänpaineesi saattaa nousta. Keskustele sen vuoksi lääkärin kanssa ennen tämän hoidon lopettamista.
Jos sinulla on kysymyksiä tämän valmisteen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Hyvin yleiset (voi esiintyä useammalla kuin 1 henkilöllä 10:stä)
Silmät
- Lievä punoitus (enintään 24 %:lla potilaista)
- Silmän alueen rasvatyynyn oheneminen, mistä voi seurata luomivaon syventyminen, silmän painuminen kuoppaansa (enoftalmia), riippuva yläluomi (ptoosi), silmänympärysihon kiristyminen (velton ihon surkastuminen) tai silmän valkuaisen alaosan tuleminen selvemmin esiin (kovakalvon alaosan näkyminen)
Yleiset (voi esiintyä enintään 1 henkilöllä 10:stä)
Silmät
- Pienet silmän pinnan rikkoumat, joihin voi liittyä tulehdusta
- Silmien ärsytys
- Silmien kutina
- Kipu
- Silmien kuivuus
- Roskantunne silmässä
- Silmäripsien pidentyminen
- Silmää ympäröivän ihon tummuminen
- Silmäluomien punoitus
Melko harvinaiset (voi esiintyä enintään 1 henkilöllä 100:sta)
Silmät
- Väsyneet silmät
- Valoherkkyys
- Värikalvon tummuminen
- Silmäluomien kutina ja turvotus
- Kyynelvuoto
- Silmän sidekalvon turvotus
- Näön sumeneminen
Elimistö
- Päänsärky
- Karvojen kasvu silmien ympärillä
Tuntemattomat (saatavissa oleva tieto ei riitä esiintyvyyden arviointiin)
Silmät
- Silmien rähmäisyys
- Epämiellyttävä tunne silmässä
Elimistö
- Astma
- Astman paheneminen
- Keuhkoahtaumataudin (COPD) paheneminen
- Hengenahdistus
- Allergisen reaktion oireet (turvotus, silmien punoitus ja ihottuma)
- Heitehuimaus
- Kohonnut verenpaine
- Ihon värimuutokset (silmänympärysihon)
LUMIGAN 0,3 mg/ml ‑kerta-annosvalmisteen käyttöön liittyvien haittavaikutusten lisäksi on havaittu seuraavia haittavaikutuksia säilytysainetta sisältävän LUMIGAN 0,3 mg/ml -moniannosvalmisteen käytön yhteydessä, ja niitä saattaa esiintyä LUMIGAN 0,3 mg/ml ‑kerta-annosvalmistetta käyttävillä potilailla:
- Silmien kirvely
- Silmän allerginen reaktio
- Silmäluomien tulehdus
- Näkövaikeudet
- Näön heikentyminen
- Silmäripsien tummuminen
- Verkkokalvon verenvuoto
- Silmänsisäinen tulehdus
- Kystoidi makulaedeema (silmän verkkokalvon turpoaminen, joka johtaa näön heikentymiseen)
- Värikalvotulehdus
- Silmäluomen nykiminen
- Silmäluomen kutistuminen, siirtyminen poispäin silmän pinnasta
- Pahoinvointi
- Silmää ympäröivän ihon punoitus
- Heikotus
- Arvojen suureneminen maksan toimintaa mittaavissa verikokeissa.
Muita fosfaattia sisältävien silmätippojen käytön yhteydessä raportoituja haittavaikutuksia
Jos sinulla on vakava vaurio silmän etuosan läpinäkyvässä kerroksessa (sarveiskalvossa), fosfaatit voivat hyvin harvinaisissa tapauksissa aiheuttaa sameita laikkuja sarveiskalvoon johtuen kalsiumin kertymisestä hoidon aikana.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös kaikkia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Tämä lääke on tarkoitettu vain kertakäyttöön eikä se sisällä säilytysaineita. Hävitä käyttämättä jäänyt liuos.
Älä käytä tätä lääkettä kerta-annospakkauksessa ja pahvikotelossa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Tämä lääkevalmiste ei vaadi erityisiä säilytysolosuhteita. Avatun pussin sisältö on kuitenkin käytettävä 30 vuorokauden kuluessa.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä LUMIGAN-kerta-annosvalmiste sisältää
- Vaikuttava aine on bimatoprosti. Yksi millilitra liuosta sisältää 0,3 mg bimatoprostia.
- Muut aineet ovat natriumkloridi, dinatriumfosfaattiheptahydraatti, sitruunahappomonohydraatti ja puhdistettu vesi. Liuokseen on voitu lisätä pieniä määriä suolahappoa tai natriumhydroksidia happamuuden (pH-arvon) pitämiseksi normaalina (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä).
LUMIGAN-kerta-annosvalmisteen kuvaus ja pakkauskoot
LUMIGAN 0,3 mg/ml -kerta-annosvalmiste on kirkas, väritön liuos, joka toimitetaan muovisissa kerta-annospakkauksissa, joista kukin sisältää 0,4 ml liuosta.
Pakkaus sisältää 5 kerta-annospakkausta pahvikotelossa.
Pakkaus sisältää 3 tai 9 alumiinifoliopussia, joista jokainen sisältää 10 kerta-annospakkausta, yhteensä 30 tai 90 kerta-annospakkausta pahvikotelossa.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija
AbbVie Deutschland GmbH & Co. KG
Knollstrasse
67061 Ludwigshafen
Saksa
Valmistaja
Allergan Pharmaceuticals Ireland
Castlebar Road
Westport
Co. Mayo
Irlanti
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
Suomi AbbVie Oy Puh: +358 (0)10 2411 200 |
Tämä pakkausseloste on tarkistettu viimeksi 11/2024
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla https://www.ema.europa.eu.
Jos haluat kuunnella tämän pakkausselosteen tai pyytää siitä kopion isotekstisenä, ota yhteys myyntiluvan haltijan paikalliseen edustajaan.