SHINGRIX injektiokuiva-aine ja suspensio, suspensiota varten
Shingrix injektiokuiva-aine ja suspensio suspensiota varten
Vyöruusurokote (rekombinantti, adjuvanttia sisältävä)
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin saat tätä rokotetta, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
- Tämä lääke on määrätty vain sinulle eikä sitä pidä antaa muiden käyttöön.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
1. Mitä Shingrix on ja mihin sitä käytetään
2. Mitä sinun on tiedettävä, ennen kuin saat Shingrix-rokotetta
3. Miten Shingrix annetaan
4. Mahdolliset haittavaikutukset
5. Shingrix-rokotteen säilyttäminen
6. Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Mihin Shingrix-rokotetta käytetään
Shingrix on rokote, jolla suojataan aikuisia vyöruusulta ja vyöruusun jälkeiseltä pitkäkestoiselta hermosäryltä eli postherpeettiseltä neuralgialta.
Shingrix-rokotetta annetaan:
- 50 vuotta täyttäneille aikuisille;
- 18 vuotta täyttäneille aikuisille, joilla vyöruusun riski on suurentunut.
Shingrix ei sovi vesirokon ehkäisyyn.
Mikä vyöruusu on
- Vyöruusu on rakkulainen ja usein kivulias ihottuma. Sitä esiintyy yleensä yhdellä kehon alueella, ja se voi kestää useita viikkoja.
- Vyöruusun aiheuttaja on vesirokkovirus.
- Kun ihminen sairastaa vesirokon, vesirokkovirus jää taudin jälkeen elimistön hermosoluihin.
- Joskus virus voi aiheuttaa vyöruusun useiden vuosien jälkeen, kun immuunijärjestelmän (elimistön oman puolustusjärjestelmän) toiminta heikkenee (iän, sairauden tai lääkityksen vuoksi).
Vyöruusun komplikaatiot
Vyöruusu voi aiheuttaa komplikaatioita.
Vyöruusun yleisin komplikaatio on:
- pitkäkestoinen hermokipu – vyöruusun jälkeinen hermosärky eli ns. postherpeettinen neuralgia. Vyöruusurakkuloiden paranemisen jälkeen voi esiintyä kipua, joka saattaa kestää kuukausia tai vuosia ja voi olla vaikeaa.
Vyöruusun muita komplikaatioita ovat:
- arvet rakkulakohdissa.
- ihotulehdukset, heikkous, lihasten halvausoire ja kuulon tai näön menetys – nämä komplikaatiot ovat harvinaisempia.
Miten Shingrix vaikuttaa
Shingrix muistuttaa elimistöä vyöruusua aiheuttavasta viruksesta. Näin immuunijärjestelmä (elimistön oma puolustusjärjestelmä) valmistautuu torjumaan virusta ja suojaamaan sinua vyöruusulta ja sen komplikaatioilta.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Sinulle ei saa antaa Shingrix-rokotetta
- jos olet allerginen vaikuttaville aineille tai tämän rokotteen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa). Allergisen reaktion merkkejä voivat olla kutiava ihottuma, hengenahdistus ja kasvojen tai kielen turvotus.
Sinulle ei saa antaa Shingrix-rokotetta, jos jokin näistä koskee sinua. Keskustele lääkärin tai apteekkihenkilökunnan kanssa, jos olet epävarma.
Varoitukset ja varotoimet
Keskustele lääkärin tai apteekkihenkilökunnan kanssa ennen kuin sinulle annetaan Shingrix-rokotetta
- jos sinulla on vaikea tulehdus, johon liittyy kuumetta (lämmönnousua). Näissä tilanteissa rokotusta täytyy ehkä siirtää, kunnes olet toipunut. Vähäinen tulehdus kuten nuhakuume ei luultavasti ole ongelma, mutta keskustele asiasta ensin lääkärin kanssa;
- jos sinulla on verenvuotohäiriö tai saat herkästi mustelmia.
Jos jokin edellä mainituista koskee sinua (tai olet epävarma asiasta), ota yhteys lääkäriin tai apteekkihenkilökuntaan ennen kuin sinulle annetaan Shingrix-rokotetta.
Pyörtyminen on mahdollista ennen mitä tahansa neulanpistoa tai minkä tahansa neulanpiston jälkeen. Kerro siis lääkärille tai hoitajalle, jos olet aiemmin pyörtynyt pistoksen jälkeen.
Shingrix ei sovi jo kehittyneen vyöruusun tai vyöruusukomplikaation hoitoon.
Kuten muutkaan rokotteet, Shingrix ei välttämättä tuota kaikille rokotetuille täydellistä suojaa.
Muut lääkevalmisteet ja Shingrix
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä. Tämä koskee myös itsehoitolääkkeitä sekä muita äskettäin saamiasi rokotteita.
Shingrix voidaan antaa samanaikaisesti muiden rokotteiden, kuten kausi-influenssarokotteen (inaktivoitu, adjuvantiton), 23-valenttisen pneumokokkipolysakkaridirokotteen (PPV23), 13-valenttisen pneumokokkikonjugaattirokotteen (PCV13), kurkkumätä-jäykkäkouristus-soluton hinkuyskä-rokotteen (matala antigeenipitoisuus) (dTap), COVID-19 mRNA -rokotteen tai RSV-rokotteen (respiratory syncytial virus; rekombinantti, adjuvanttia sisältävä) kanssa. Kukin rokote annetaan eri pistoskohtaan.
Kuumetta ja/tai vilunväristyksiä voi esiintyä yleisemmin, kun 23-valenttinen pneumokokkipolysakkaridirokote annetaan samanaikaisesti Shingrix-rokotteen kanssa.
Vilunväristyksiä, väsymystä, kuumetta, vatsa- ja ruoansulatusvaivoja (kuten pahoinvointia, oksentelua, ripulia ja/tai vatsakipua), päänsärkyä, lihaskipua tai nivelkipua voi esiintyä yleisemmin, kun COVID-19 mRNA -rokote annetaan samanaikaisesti Shingrix-rokotteen kanssa.
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen kuin sinulle annetaan tätä rokotetta.
Ajaminen ja koneiden käyttö
Osa alla mainituista haittavaikutuksista (kohta Mahdolliset haittavaikutukset) saattaa väliaikaisesti vaikuttaa ajokykyyn tai koneiden käyttökykyyn. Älä aja ajoneuvoja äläkä käytä koneita, jos vointisi on huono.
Shingrix sisältää polysorbaatti 80:tä, natriumia ja kaliumia
Tämä lääkevalmiste sisältää 0,08 mg polysorbaatti 80:tä per annos. Polysorbaatit saattavat aiheuttaa allergisia reaktioita. Jos sinulla on allergioita, kerro asiasta lääkärille.
Tämä lääkevalmiste sisältää alle 1 mmol natriumia (23 mg) per annos eli sen voidaan sanoa olevan ”natriumiton”.
Tämä lääkevalmiste sisältää kaliumia alle 1 mmol (39 mg) per annos, eli sen voidaan sanoa olevan ”kaliumiton”.
Miten valmistetta käytetään
- Shingrix annetaan pistoksena lihakseen (yleensä olkavarteen).
- Saat yhteensä 2 pistosta, jotka annetaan 2 kuukauden välein. Jos rokotussarjaan on välttämätöntä saada joustavuutta, toinen annos voidaan antaa 2–6 kuukauden kuluttua ensimmäisestä annoksesta.
Terveystilanteesi perusteella lääkäri voi myös suositella, että toinen pistos annetaan 1 kuukauden kuluttua ensimmäisestä pistoksesta. - Sinulle kerrotaan, milloin toinen Shingrix-annos tulee antaa.
Muista ottaa rokotussarjan molemmat rokotteet. Näin Shingrix tarjoaa mahdollisimman tehokkaan suojan.
Shingrix voidaan antaa, vaikka olisit jo aiemmin saanut rokotuksen elävällä heikennetyllä herpes zoster -rokotteella. Keskustele lääkärin kanssa lisätietojen saamiseksi.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin rokote voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Haittavaikutuksia, joita on raportoitu Shingrix-rokotteen kliinisissä tutkimuksissa ja markkinoille tulon jälkeen:
Hyvin yleiset (voi esiintyä yli 1 rokoteannoksen yhteydessä 10:stä):
- päänsärky
- maha- ja ruoansulatusvaivat (mm. pahoinvointi, oksentelu, ripuli ja/tai mahakipu)
- lihaskipu
- pistoskohdan kipu, punoitus ja turvotus
- uupumus
- vilunväristykset
- kuume.
Yleiset (voi esiintyä enintään 1 rokoteannoksen yhteydessä 10:stä):
- kutina pistoskohdassa
- yleinen sairaudentunne.
Melko harvinaiset (voi esiintyä enintään 1 rokoteannoksen yhteydessä 100:sta):
- imusolmukkeiden turvotus kaulan, kainaloiden tai nivusten alueella
- nivelkipu
- ihon kovettuminen injektiokohdassa.
Harvinaiset (voi esiintyä enintään 1 rokoteannoksen yhteydessä 1 000:sta):
- allergiset reaktiot mukaan lukien ihottuma, nokkosihottuma ja kasvojen, kielen tai nielun turvotus, joka voi aiheuttaa nielemis- tai hengitysvaikeuksia (angioedeema).
Hyvin harvinaiset (voi esiintyä enintään 1 rokoteannoksen yhteydessä 10 000:sta):
- hermoston häiriö, joka alkaa yleensä pistelystä ja raajojen heikkoudesta ja voi edetä osan tai koko kehon halvaantumiseen (Guillain–Barrén oireyhtymä).
Useimmiten nämä haittavaikutukset ovat lieviä tai kohtalaisia eivätkä kestä pitkään.
18–49-vuotiailla immuunipuutteisilla aikuisilla voi esiintyä enemmän haittavaikutuksia kuin 50 vuotta täyttäneillä immuunipuutteisilla aikuisilla.
50–69-vuotiailla aikuisilla voi esiintyä enemmän haittavaikutuksia kuin 70 vuotta täyttäneillä aikuisilla.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan kansallisen ilmoitusjärjestelmän kautta. Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Valmisteen säilyttäminen
- Ei lasten ulottuville eikä näkyville.
- Älä käytä tätä lääkettä etiketissä ja kotelossa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
- Säilytä jääkaapissa (2 °C – 8 °C).
- Ei saa jäätyä.
- Säilytä alkuperäispakkauksessa. Herkkä valolle.
- Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä Shingrix sisältää
- Vaikuttavat aineet ovat:
Käyttökuntoon saattamisen jälkeen yksi annos (0,5 ml) sisältää:
Varicella zoster ‑viruksen1 glykoproteiini E ‑antigeenia2 50 mikrogrammaa
1 Varicella zoster ‑virus = VZV
2 Mukana oleva AS01B-adjuvantti sisältää seuraavia aineita:
Quillaja saponaria Molina ‑kasviuute, fraktio 21 (QS-21) 50 mikrogrammaa
3-O-desasyyli-4’-monofosforyylilipidi A (MPL) Salmonella minnesota ‑mikrobista 50 mikrogrammaa
Glykoproteiini E on varicella zoster ‑viruksessa eli vesirokkoviruksessa esiintyvä proteiini. Tämä proteiini ei ole tartuntaa aiheuttava.
Adjuvantilla (AS01B) tehostetaan elimistön reagointia rokotteeseen. - Muut aineet ovat:
- Kuiva-aine: Sakkaroosi, polysorbaatti 80 (E 433), natriumdivetyfosfaattidihydraatti (E 339), dikaliumfosfaatti (E 340).
- Suspensio: Dioleoyylifosfatidyylikoliini (E 322), kolesteroli, natriumkloridi, vedetön dinatriumfosfaatti (E 339), kaliumdivetyfosfaatti (E 340) ja injektionesteisiin käytettävä vesi.
Ks kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä. ”Shingrix sisältää polysorbaatti 80:tä, natriumia ja kaliumia”.
Lääkevalmisteen kuvaus ja pakkauskoko (- koot)
- Injektiokuiva-aine ja suspensio suspensiota varten.
- Kuiva-aine on valkoista.
- Suspensio on opalisoivaa, väritöntä tai vaalean rusehtavaa nestettä.
Yhdessä Shingrix-pakkauksessa on:
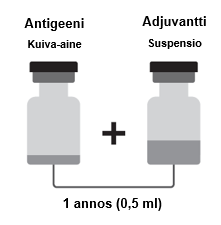
- Kuiva-aine (antigeeni) 1 annosta varten injektiopullossa
- Suspensio (adjuvantti) 1 annosta varten injektiopullossa
Shingrix on saatavilla pakkauksessa, jossa on 1 injektiopullo kuiva-ainetta ja 1 injektiopullo suspensiota, sekä pakkauksessa, jossa on 10 injektiopulloa kuiva-ainetta ja 10 injektiopulloa suspensiota.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija ja valmistaja
GlaxoSmithKline Biologicals SA
Rue de l’Institut 89
1330 Rixensart
Belgia
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
Suomi/Finland
GlaxoSmithKline Oy
Puh/Tel: + 358 10 30 30 30
Tämä pakkausseloste on tarkistettu viimeksi 12.2.2026
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla https://www.ema.europa.eu.
Ohjeet terveydenhuollon ammattilaiselle
Shingrix on pakattu kuiva-ainetta (antigeenia) sisältävään injektiopulloon, jossa on ruskea irti napsautettava (flip-off) korkki, ja suspensiota (adjuvanttia) sisältävään injektiopulloon, jossa on sinivihreä irti napsautettava (flip-off) korkki.
Kuiva-aine ja suspensio on saatettava käyttökuntoon ennen antoa.
Kuiva-aine ja suspensio on tarkastettava silmämääräisesti vieraiden hiukkasten ja/tai ulkonäkömuutosten varalta. Jos jompaakumpaa näistä todetaan, rokotetta ei saa saattaa käyttökuntoon.
Shingrix-rokotteen valmistelu:
Shingrix saatetaan käyttökuntoon ennen antoa.
- Suspensiota sisältävän injektiopullon koko sisältö vedetään ruiskuun sopivan kokoisella neulalla (21G–25G).
- Ruiskun koko sisältö lisätään injektiopulloon, jossa kuiva-aine on.
- Ravistellaan varovasti, kunnes kuiva-aine on liuennut täysin.
Käyttökuntoon saatettu rokote on opalisoivaa, väritöntä tai vaalean rusehtavaa nestettä.
Käyttökuntoon saatettu rokote on tarkastettava silmämääräisesti vieraiden hiukkasten ja/tai ulkonäkömuutosten varalta. Jos jompaakumpaa näistä todetaan, rokotetta ei saa antaa.
Käyttökuntoon saattamisen jälkeen rokote tulee antaa heti; mikäli tämä ei ole mahdollista, rokote säilytetään jääkaapissa (2 °C – 8 °C). Jos sitä ei käytetä 6 tunnissa, se on hävitettävä.
Ennen antoa:
- Käyttökuntoon saatettua rokotetta sisältävän injektiopullon koko sisältö vedetään ruiskuun.
- Neula vaihdetaan eli rokotteen antoon käytetään uutta neulaa.
Hävittäminen
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.