BRAVECTO paikallisvaleluliuos kissoille 112,5 mg, 250 mg, 500 mg
ELÄINLÄÄKEVALMISTEEN NIMI
Bravecto 112,5 mg paikallisvaleluliuos pienille kissoille (1,2–2,8 kg)
Bravecto 250 mg paikallisvaleluliuos keskikokoisille kissoille (>2,8–6,25 kg)
Bravecto 500 mg paikallisvaleluliuos suurille kissoille (>6,25–12,5 kg)
VAIKUTTAVAT JA MUUT AINEET
1 ml sisältää 280 mg fluralaneeria.
Yksi annospipetti sisältää:
|
Bravecto paikallisvaleluliuos |
Pipetin sisältö (ml) |
Fluralaneeria (mg)
|
|
pienille kissoille 1,2–2,8 kg |
0,4 |
112,5 |
|
keskikokoisille kissoille >2,8–6,25 kg |
0,89 |
250 |
|
suurille kissoille >6,25–12,5 kg |
1,79 |
500 |
Kirkas, väritön tai keltainen liuos.
KÄYTTÖAIHEET
Puutiais- ja kirpputartuntojen hoito kissoilla.
Tämä eläinlääke on systeemisesti vaikuttava insektisidinen ja akarisidinen aine, jolla on välitön ja pitkäkestoinen kirppuja (Ctenocephalides felis) ja puutiaisia (Ixodes ricinus) tappava vaikutus 12 viikon ajan.
Kirppujen ja puutiaisten täytyy kiinnittyä kissaan ja aloittaa imeminen, jotta ne altistuvat vaikuttavalle aineelle.
Eläinlääkettä voidaan käyttää osana kirppuallergian (flea allergy dermatitis, FAD) hoitoa.
Korvapunkin (Otodectes cynotis) aiheuttaman tartunnan hoito.
VASTA-AIHEET
Ei saa käyttää tapauksissa, joissa esiintyy yliherkkyyttä vaikuttavalle aineelle tai apuaineille.
HAITTAVAIKUTUKSET
Kissa:
Yleinen (1–10 eläintä 100 hoidetusta eläimestä): | Ihoreaktiot antokohdassa (kuten punoitus, kutina tai karvanlähtö)# |
Melko harvinainen 1–10 eläintä 1 000 hoidetusta eläimestä): | Lihasvapina; Apatia, ruokahaluttomuus; Oksentaminen, kuolaaminen. |
Hyvin harvinainen (< 1 eläin 10 000 hoidetusta eläimestä, yksittäiset ilmoitukset mukaan luettuina): | Kutina; Ataksia (vaikeus koordinoida liikkeitä), kouristukset. |
# lieviä ja ohimeneviä
Haittatapahtumista ilmoittaminen on tärkeää. Se mahdollistaa eläinlääkkeen turvallisuuden jatkuvan seurannan. Jos havaitset haittavaikutuksia, myös sellaisia, joita ei ole mainittu tässä pakkausselosteessa, tai olet sitä mieltä, että lääke ei ole tehonnut, ilmoita ensisijaisesti asiasta eläinlääkärillesi. Voit ilmoittaa kaikista haittavaikutuksista myös myyntiluvan haltijalle käyttämällä tämän pakkausselosteen lopussa olevia yhteystietoja tai kansallisen ilmoitusjärjestelmän kautta: Lääkealan turvallisuus- ja kehittämiskeskus Fimea, www-sivusto: https://fimea.fi/elainlaakkeet.
KOHDE-ELÄINLAJI
Kissa
ANNOSTUS, ANTOREITIT JA ANTOTAVAT KOHDE-ELÄINLAJEITTAIN
Bravecto annostellaan seuraavan taulukon mukaan (annos vastaa 40–94 mg fluralaneeria/kissan paino kg:ssa).
|
Kissan paino (kg) |
Annosteltavien pipettien vahvuus ja määrä |
||
|
Bravecto 112,5 mg |
Bravecto 250 mg |
Bravecto 500 mg |
|
|
1,2–2,8 |
1 |
|
|
|
>2,8–6,25 |
|
1 |
|
|
>6,25–12,5 |
|
|
1 |
Kissoille, jotka painavat yli 12,5 kg, annetaan 2 pipettiä yhdistelemällä eri vahvuuksia siten, että saadaan parhaiten kissan todellista painoa vastaava annos.
Aliannostelu voi johtaa tehottomaan käyttöön ja edistää resistenssin kehittymistä.
ANNOSTUSOHJEET
Antotapa
Vaihe 1: Avaa pussi ja poista pipetti juuri ennen käyttöä. Pue suojakäsineet. Pidä kiinni pipetin tyvestä tai ylempää pipetin jäykän osan kohdalla. Pidä pipetti pystyasennossa (kärki ylöspäin) kun avaat. Käännä korkkia myötä- tai vastapäivään yksi täysi kierros. Korkki jää pipettiin kiinni, sitä ei voi irrottaa. Pipetti on auki ja valmis käytettäväksi, kun tunnet sinetin rikkoutuvan.

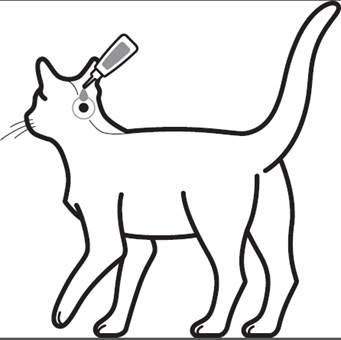
Vaihe 2: Kissan tulee seisoa tai maata selkä ylöspäin annostelun ajan. Aseta pipetin kärki kissan kallon tyveen.
Vaihe 3: Purista pipettiä varovasti jatyhjennä koko pipetin sisältö suoraan kissan iholle. Tyhjennä pipetti yhteen kohtaan kallon tyveen kissoille, jotka painavat 6,25 kg tai vähemmän ja kahteen kohtaan kissoille, jotka painavat enemmän kuin 6,25 kg.
Hoito-ohjelma
Kirppu- ja puutiaistartuntojen osalta uusintahoidon tarpeen ja tiheyden olisi perustuttava ammattilaisen neuvoihin ja siinä tulisi huomioida paikallinen epidemiologinen tilanne ja eläimen elinolosuhteet.
Puutiaisten ja kirppujen optimaalisen häädön ja torjunnan varmistamiseksi eläinlääkettä tulisi käyttää 12 viikon välein.
Korvapunkkitartunnan (Otodectes cynotis) hoitoon annetaan yksi kerta-annos eläinlääkettä. Jotkut eläimet voivat vaatia hoitoa myös toisella eläinlääkkeellä. Tämän vuoksi suositellaan eläinlääkärin tarkastusta 28 vuorokauden jälkeen hoidon aloituksesta
VAROAIKA
Ei oleellinen.
SÄILYTYSOLOSUHTEET
Ei lasten näkyville eikä ulottuville.
Tämä eläinlääke ei vaadi lämpötilan suhteen erityisiä säilytysolosuhteita. Säilytä pipetit alkuperäispakkauksessa suojassa kosteudelta ja liuottimen haihtumiselta. Avaa pipettiä suojaava pussi vasta juuri ennen käyttöä.
Älä käytä tätä eläinlääkettä viimeisen käyttöpäivämäärän jälkeen, joka on ilmoitettu pakkauksessa merkinnän Exp. jälkeen. Viimeisellä käyttöpäivämäärällä tarkoitetaan kuukauden viimeistä päivää.
ERITYISVAROITUKSET
Erityisvaroitukset:
Ulkoloisten täytyy kiinnittyä kissaan ja aloittaa imeminen, jotta ne altistuvat fluralaneerille. Tämän vuoksi ulkoloisvälitteisten tautien tartuntariskiä ei voida sulkea kokonaan pois.
Loislääkkeiden tarpeeton tai valmisteyhteenvedon ohjeista poikkeava käyttö voi lisätä resistenssin valintapainetta ja johtaa tehon heikkenemiseen. Eläinlääkkeen käyttöä koskevan päätöksen tulisi kunkin yksittäisen eläimen osalta perustua loislajin ja loistaakan tai epidemiologisen tilanteen mukaisen tartuntariskin varmistamiseen.
On otettava huomioon mahdollisuus, että saman kotitalouden muut eläimet voivat olla ulkoloisten uudelleentartunnan lähde, ja muut eläimet on hoidettava tarpeen mukaan asianmukaisella eläinlääkkeellä.
Erityiset varotoimet, jotka liittyvät turvalliseen käyttöön kohde-eläinlajilla:
Huolellisuutta on noudatettava, jotta valmistetta ei joudu eläimen silmiin. Älä käytä suoraan vaurioituneelle iholle. Koska tietoja ei ole saatavilla, eläinlääkettä ei pidä käyttää alle 9 viikon ikäisille kissanpennuille ja/tai alle 1,2 kg painaville kissoille.
Eläinlääkettä ei pidä käyttää useammin kuin 8 viikon välein, koska tiheämmän annosvälin turvallisuutta ei ole tutkittu.
Tämä eläinlääke annetaan iholle; sitä ei pidä antaa suun kautta.
Älä anna vastakäsiteltyjen eläinten nuolla toisiaan.
Erityiset varotoimenpiteet, joita eläinlääkettä eläimille antavan henkilön on noudatettava:
Vältä kosketusta eläinlääkkeeseen ja käytä eläinlääkkeen myynnin yhteydessä saatuja kertakäyttöisiä suojakäsineitä eläinlääkettä käsitellessäsi seuraavista syistä:
Yliherkkyysreaktioita, jotka voivat olla vakavia, on raportoitu pienellä määrällä ihmisiä.
Henkilöiden, jotka ovat yliherkkiä fluralaneerille tai jollekin valmisteen, tulee välttää kosketusta eläinlääkkeen kanssa.
Eläinlääke tarttuu ihoon ja voi tarttua myös pintoihin, jos sitä roiskuu pinnoille. Ihottumaa, kihelmöintiä tai tunnottomuutta on raportoitu pienellä määrällä henkilöitä, kun valmistetta on joutunut iholle.
Jos valmistetta joutuu vahingossa ihollesi, pese altistunut iho välittömästi vedellä ja saippualla. Joissakin tapauksissa vesi ja saippua ei poista roiskeita sormista.
Eläinlääkettä voi joutua iholle myös valmisteella käsitellystä eläimestä.
Antopaikkaa ei tule koskea, ennen kuin antopaikka on muuttunut huomaamattomaksi. Tämä tarkoittaa myös lemmikin hyväilemistä ja samassa sängyssä nukkumista. Lääkkeen antopaikka kuivuu 48 tunnissa, mutta lääke voi näkyä antopaikassa kauemmin.
Jos saat iho-oireita, kysy neuvoa lääkäriltä ja näytä hänelle valmisteen pakkausta.
Herkkäihoisten ja allergisten henkilöiden (esim. vastaavan tyyppisille eläinlääkkeille) yleisestikin tulee käsitellä varoen tätä eläinlääkettä sekä eläinlääkkeellä hoidettuja eläimiä.
Tämä eläinlääke voi ärsyttää silmiä. Jos valmistetta joutuu silmiin, huuhtele silmät heti runsaalla vedellä.
Tämä eläinlääke on haitallista nieltynä. Pidä eläinlääke alkuperäispakkauksessa käyttöhetkeen saakka, jotta lapset eivät pääse käsiksi eläinlääkkeeseen. Hävitä käytetty pipetti välittömästi käytön jälkeen. Jos vahingossa nielet valmistetta, käänny välittömästi lääkärin puoleen ja näytä hänelle pakkausseloste tai myyntipäällys.
Tämä eläinlääke on helposti syttyvää. Pidä valmiste kaukana lämmönlähteistä, kipinöistä, avotulesta ja muista sytytyslähteistä.
Jos valmistetta roiskuu annosteltaessa esimerkiksi pöydälle tai lattialle, poista roiskeet paperilla ja puhdista alue puhdistusaineella.
Tiineys, imetys ja hedelmällisyys:
Tämän eläinlääkkeen turvallisuutta tiineyden ja imetyksen aikana ei ole selvitetty. Käytetään tiineille tai imettäville kissoille ainoastaan hoidosta vastaavan eläinlääkärin tekemän hyöty-riskiarvion perusteella.
Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset:
Ei tunneta.
Fluralaneeri sitoutuu voimakkaasti plasman proteiineihin ja voi kilpailla muiden voimakkaasti sitoutuvien lääkeaineiden kanssa, kuten steroideihin kuulumattomat tulehduskipulääkkeet (NSAID) tai kumariinijohdannainen varfariini. Fluralaneerin inkubointi oletetulla maksimikonsentraatiolla plasmassa karprofeenin tai varfariinin kanssa ei vähentänyt fluralaneerin, karprofeenin tai varfariinin sitoutumista plasman proteiineihin.
Laboratorio- ja kliinisten kenttäkokeiden aikana ei havaittu yhteisvaikutuksia tämän eläinlääkkeen ja muiden yleisesti käytettävien eläinlääkkeiden kanssa.
Yliannostus:
Haittavaikutuksia ei havaittu 9–13 viikon ikäisillä ja 0,9–1,9 kg painoisilla kissanpennuilla käytettäessä jopa viisinkertaisia suositeltuja enimmäisannoksia (93 mg, 279 mg ja 465 mg fluralaneeria / paino kg) kolmena annostelukertana käyttäen lyhempiä kuin suositeltuja annosvälejä (8 viikon välein).
Fluralaneeri oli hyvin siedetty kissoilla suun kautta annetuilla enimmäisannoksilla, lukuun ottamatta itsestään rajoittuvaa lisääntynyttä syljen eritystä, yskimistä tai oksentelua annostelun jälkeen.
Merkittävät yhteensopimattomuudet:
Ei tunneta.
ERITYISET VAROTOIMET KÄYTTÄMÄTTÖMÄN VALMISTEEN TAI JÄTEMATERIAALIN HÄVITTÄMISEKSI
Lääkkeitä ei saa kaataa viemäriin eikä hävittää talousjätteiden mukana.
Eläinlääkettä ei saa joutua vesistöihin, sillä fluralaneeri saattaa olla vaarallista selkärangattomille vesieliöille.
Eläinlääkkeiden tai niiden käytöstä syntyvien jätemateriaalien hävittämisessä käytetään paikallisia palauttamisjärjestelyjä sekä kyseessä olevaan eläinlääkkeeseen sovellettavia kansallisia keräysjärjestelmiä. Näiden toimenpiteiden avulla voidaan suojella ympäristöä.
Kysy käyttämättömien lääkkeiden hävittämisestä eläinlääkäriltäsi tai apteekista.
PÄIVÄMÄÄRÄ, JOLLOIN PAKKAUSSELOSTE ON VIIMEKSI HYVÄKSYTTY
24.7.2025
Tätä eläinlääkettä koskevaa yksityiskohtaista tietoa on saatavilla unionin valmistetietokannassa (https://medicines.health.europa.eu/veterinary).
MUUT TIEDOT
Valmiste vaikuttaa kissan ympäristön kirppupopulaatioihin kissan elinalueella.
Valmiste saavuttaa tehonsa kirppuja (C. felis) vastaan 12 tunnin kuluessa ja puutiaisia (I. ricinus) vastaan 48 tunnin kuluessa.
MYYNTILUVAN HALTIJAN NIMI JA OSOITE SEKÄ ERÄN VAPAUTTAMISESTA VASTAAVAN VALMISTAJAN NIMI JA OSOITE EUROOPAN TALOUSALUEELLA, JOS ERI
Myyntiluvan haltija ja yhteystiedot epäillyistä haittatapahtumista ilmoittamista varten:
Intervet International B. V.
Wim de Körverstraat 35
5831 AN Boxmeer
Alankomaat
Suomi
Puh: + 358 10 2310 750
Erän vapauttamisesta vastaava valmistaja:
Intervet Productions S.A.
Rue de Lyons
27460 Igoville
Ranska