DUOTRAV ögondroppar, lösning 40 mikrog/ml + 5 mg/ml
Tilläggsinformation
DuoTrav 40 mikrogram/ml + 5 mg/ml ögondroppar, lösning
travoprost/timolol
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
- Vad DuoTrav är och vad det används för
- Vad du behöver veta innan du använder DuoTrav
- Hur du använder DuoTrav
- Eventuella biverkningar
- Hur DuoTrav ska förvaras
- Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
DuoTrav ögondroppar, lösning är en kombination av två aktiva substanser (travoprost och timolol). Travoprost är en prostaglandinanalog, som verkar genom att öka utflödet av vätska i ögat, vilket sänker trycket i ögat. Timolol är en betablockerare, som verkar genom att produktionen av vätska i ögat minskar. De två substanserna fungerar tillsammans för att minska ögontrycket.
DuoTrav används för att behandla högt tryck i ögat hos vuxna, inklusive äldre. För högt tryck kan leda till en sjukdom som kallas glaukom.
Vad du behöver veta innan produkten används
Använd inte DuoTrav
- om du är allergisk mot travoprost, prostaglandiner, timolol, betablockerare eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
- om du för närvarande har eller tidigare har haft andningsproblem såsom astma, svår kronisk obstruktiv bronkit (svår lungsjukdom som kan orsaka pipande andning, svårigheter att andas och/eller ihållande hosta) eller andra typer av andningsproblem
- om du har allvarlig hösnuva
- om du har långsam hjärtfrekvens, hjärtsvikt eller ett tillstånd som påverkar hjärtats rytm (oregelbundna hjärtslag)
- om ytan på ditt öga är grumlig
Fråga din läkare om råd om något av detta berör dig.
Varningar och försiktighet
Tala med läkare innan du använder DuoTrav om du för närvarande har eller tidigare har haft:
- kranskärlssjukdom (symtomen kan omfatta smärta eller trånghet i bröstet, andfåddhet eller kvävning), hjärtsvikt, lågt blodtryck.
- störningar av hjärtfrekvensen som t.ex. långsamma hjärtslag.
- andningsproblem, astma eller kronisk obstruktiv lungsjukdom.
- sjukdom med nedsatt blodcirkulation (t.ex. Raynauds sjukdom eller Raynauds syndrom).
- diabetes (eftersom timolol kan dölja tecken och symtom på lågt blodsocker).
- överaktiv sköldkörtel (eftersom timolol kan dölja tecken och symtom).
- myasthenia gravis (kronisk neuromuskulär svaghet).
- opererats för grå starr.
- ögoninflammation.
Om du ska genomgå någon slags operation, tala om för läkaren att du använder DuoTrav eftersom timolol kan ändra effekterna av vissa läkemedel som används under anestesi.
Om du får en allvarlig allergisk reaktion (hudutslag, rodnad eller klåda i ögat) när du använder DuoTrav, oavsett orsak, så är det möjligt att adrenalinbehandling inte hjälper som vanligt. När du erhåller någon annan behandling bör du informera läkaren om att du behandlas med DuoTrav.
DuoTrav kan ändra färgen på iris (den färgade delen av ditt öga). Denna förändring kan vara bestående.
DuoTrav kan öka längden, tjockleken, färgen och/eller antalet på dina ögonfransar och kan orsaka ovanlig hårväxt på dina ögonlock.
Travoprost kan tas upp genom huden och ska därför inte användas av kvinnor som är gravida eller försöker bli gravida. Om läkemedlet kommer i kontakt med huden ska man tvätta bort den genast.
Barn
DuoTrav är inte avsett att användas av barn och ungdomar under 18 år.
Andra läkemedel och DuoTrav
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel, inklusive receptfria läkemedel.
DuoTrav kan påverka eller påverkas av andra läkemedel som du använder, även andra ögondroppar för behandling av glaukom. Tala om för din läkare om du använder eller tänker använda läkemedel mot högt blodtryck, hjärtläkemedel som t.ex. kinidin (används för att behandla hjärttillstånd och vissa typer av malaria), läkemedel mot diabetes eller antidepressiva medlen fluoxetin eller paroxetin.
Graviditet, amning och fertilitet
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare innan du använder detta läkemedel.
Använd inte DuoTrav om du är gravid såvida inte din läkare anser att det är nödvändigt. Om du kan tänkas bli gravid, så måste du använda säkra preventivmedel när du använder detta läkemedel.
Använd inte DuoTrav om du ammar. DuoTrav kan gå ut i bröstmjölken.
Körförmåga och användning av maskiner
Du kan uppleva att din syn blir dimmig direkt efter du tagit DuoTrav. DuoTrav kan också ge hallucinationer, yrsel, nervositet eller trötthet hos vissa patienter.
Kör inte bil och använd inte verktyg eller maskiner förrän dessa symtom försvunnit.
DuoTrav innehåller makrogolglycerolhydroxistearat (hydrerad ricinolja) och propylenglykol, vilka kan orsaka hudreaktioner och hudirritation.
Hur produkten används
Använd alltid detta läkemedel enligt läkarens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
Rekommenderad dos är en droppe i det påverkade ögat eller ögonen, en gång dagligen på morgonen eller kvällen. Ta DuoTrav vid samma tidpunkt varje dag.
Använd DuoTrav i båda ögonen endast om din läkare har ordinerat det.
DuoTrav ska endast användas som ögondroppar.
| |
|
|
|
| 1 |
2 |
3 |
4 |
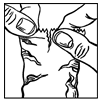
- Direkt innan du använder en flaska för första gången ska du öppna skyddspåsen (bild 1) och ta ut flaskan och anteckna datumet då du öppnade flaskan i det tomma utrymmet på etiketten.
- Se till att du har en spegel tillgänglig.
- Tvätta dina händer.
- Skruva av flaskans lock.
- Håll flaskan upp och ner mellan tummen och fingrarna.
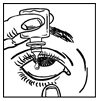
- Luta huvudet bakåt. Dra ner det nedre ögonlocket med ett rent finger så att det bildas en ”ficka” mellan ögonlocket och ögat. Droppen skall hamna här (bild 2).
- Håll droppspetsen nära ögat. Använd spegeln om det hjälper till.
- Vidrör inte ögat eller ögonlocket, omgivande områden eller andra ytor med droppspetsen. Det kan förorena dropparna.
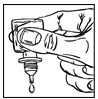
- Tryck försiktigt på flaskan för att frigöra en droppe DuoTrav i taget (bild 3). Om en droppe missar ögat så försök igen.
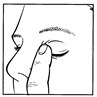
- När du tagit DuoTrav ska du trycka med ditt finger i ögonvrån intill din näsa i 2 minuter (bild 4). Det förhindrar att DuoTrav kommer ut i resten av kroppen.
- Om du ska använda DuoTrav i båda ögonen, upprepa ovanståendemoment för ditt andra öga.
- Skruva på locket ordentligt direkt efter användning.
- Använd endast en flaska i taget. Öppna inte skyddspåsen förrän du behöver använda flaskan.
Använd DuoTrav så länge din läkare har sagt till dig att göra det.
Om du har använt för stor mängd av DuoTrav
Om du har använt för stor mängd av DuoTrav, så skölj ut allt med varmt vatten. Tag inga fler droppar förrän det är tid för din nästa ordinarie dos.
Om du har glömt att använda DuoTrav
Om du har glömt att använda DuoTrav, fortsätt med nästa dos som planerat. Ta inte dubbel dos för att kompensera för glömd dos. Dosen ska inte överstiga en droppe i varje påverkat öga per dag.
Om du slutar att använda DuoTrav
Om du slutar att använda DuoTrav utan att tala med din läkare, så kan inte trycket i ditt öga kontrolleras och detta kan leda till synförlust.
Om du använder andra ögondroppar utöver DuoTrav så vänta minst 5 minuter mellan det att du tar DuoTrav och de andra dropparna.
Om du använder mjuka kontaktlinser ska du inte använda dropparna med kontaktlinserna kvar i ögonen. Vänta i 15 minuter när du har droppat i ögondropparna, innan du sätter tillbaka linserna i ögonen.
Om du har ytterligare frågor om detta läkemedel kontakta läkare eller apotekspersonal.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem.
Du kan vanligtvis fortsätta använda dropparna om inte biverkningarna är allvarliga. Om du är orolig så tala med en läkare eller apotekspersonal. Sluta inte att använda DuoTrav utan att ha talat med din läkare.
Mycket vanliga biverkningar (kan förekomma hos fler än 1 av 10 användare)
Effekter i ögonen
Ögonrodnad.
Vanliga biverkningar (kan förekomma hos upp till 1 av 10 användare)
Effekter i ögonen
Inflammation i ögats yta med ytskador, ögonsmärta, dimsyn, onormal syn, torra ögon, klåda i ögonen, obehag i ögonen, tecken och symtom på ögonirritation (t.ex. sveda, smärta).
Mindre vanliga biverkningar (kan förekomma hos upp till 1 av 100 användare)
Effekter i ögonen
Inflammation i ögats yta, inflammation i ögonlocket, svullen bindhinna, ökad tillväxt av ögonfransarna, irisinflammation, ögoninflammation, ljuskänslighet, nedsatt syn, trötta ögon, ögonallergi, ögonsvullnad, ökad tårproduktion, ögonlocksrodnad, förändring av ögonlockets färg, mörkare hud (runt ögat).
Allmänna effekter
Allergisk reaktion mot aktiv substans, yrsel, huvudvärk, förhöjt eller sänkt blodtryck, andfåddhet, ökad hårväxt, dropp längst bak i svalget, hudinflammation och klåda, långsammare hjärtslag.
Sällsynta biverkningar (kan förekomma hos upp till 1 av 1000 användare)
Effekter i ögonen
Förtunning av ögats yta, inflammation i ögonlockskörtlarna, brustet blodkärl i ögat, krustabildning på ögonlocken, onormalt placerade ögonfransar, onormalt ökad tillväxt av ögonfransarna.
Allmänna effekter
Nervositet, oregelbundna hjärtslag, håravfall, röstproblem, andningssvårigheter, hosta, halsirritation, nässelfeber, onormala levervärden, hudmissfärgning, törst, trötthet, obehag inuti näsan, färgad urin, smärta i händer och fötter.
Har rapporterats (förekommer hos okänt antal användare)
Effekter i ögonen
Hängande ögonlock (gör att ögat hålls halvslutet), insjunkna ögon , ändrad färg på iris (färgade delen av ögat).
Allmänna effekter
Utslag, hjärtsvikt, bröstsmärta, stroke, svimning, depression, astma, ökad hjärtfrekvens, domningar eller stickande känsla, hjärtklappning, svullnad i underbenen, dålig smak i munnen.
Dessutom:
DuoTrav är en kombination av två aktiva ämnen, travoprost och timolol. Liksom andra läkemedel som administreras (ges) i ögonen absorberas travoprost och timolol (en betablockerare) i blodet. Detta kan ge liknande biverkningar som iakttas när betablockerande läkemedel administreras genom munnen eller via injektion. Förekomsten av biverkningar efter administrering i ögonen är lägre än efter administrering genom munnen eller via injektion.
Nedan angivna biverkningar har inte rapporterats för DuoTrav men omfattar reaktioner som ses i klassen betablockerare när de används för behandling av ögontillstånd eller reaktioner som setts med enbart travoprost:
Ögoneffekter
Inflammation i ögonlocket, inflammation i hornhinnan, avlossning av det skikt under näthinnan som innehåller blodkärl efter filtreringskirurgi, vilket kan orsaka synstörningar, minskad känslighet i hornhinnan, erosion av hornhinnan (skada på ögonglobens främre skikt), dubbelseende,, rinnande öga, svullnad runt ögat, klåda på ögonlocken, ögonlocket vänds utåt med rodnad, irritation och ökad tårbildning, dimsyn (tecken på grumling av ögats lins), svullnad av en del av ögat (uvea), eksem på ögonlocken, haloeffekt (ljusringar runt en ljuspunkt), nedsatt känsel i ögat, pigmentering inne i ögat, utvidgade (dilaterade) pupiller, färgförändrade ögonfransar, förändrad textur hos ögonfransarna, onormalt synfält.
Allmänna effekter
Öron och balansorgan: yrsel tillsammans med en känsla av att det snurrar, ringningar i öronen.
Hjärta och blodcirkulation: långsamma hjärtslag, hjärtklappning, ödem (vätskeansamling), ändrad rytm eller hastighet på hjärtslagen, kronisk hjärtinsufficiens (hjärtsjukdom med andfåddhet och svullnad av fötter och ben på grund av vätskansamling), en typ av hjärtrytmsrubbning, hjärtinfarkt, lågt blodtryck, Raynauds fenomen, kalla händer och fötter, minskad blodförsörjning till hjärnan.
Andningsvägarna: sammandragning av luftvägarna i lungorna (framför allt hos patienter med redan befintlig sjukdom), rinnande näsa eller nästäppa, nysningar (på grund av allergi), svårighet att andas, näsblod, torrhet i näsan.
Nervsystemet och allmänna symtom: sömnsvårigheter (insomni), mardrömmar, minnesförlust, hallucinationer, förlust av styrka och energi, ångest (överdriven känslomässig oro).
Mage-tarm: smakförändringar, illamående, magbesvär, diarré, muntorrhet, buksmärta, kräkning och förstoppning.
Allergi: ökade allergiska symtom, generaliserade allergiska reaktioner, bland annat svullnad under huden som kan förekomma på ställen som t.ex. ansiktet och armar och ben och kan hindra luftvägarna vilket kan orsaka svårighet att svälja eller andas, begränsat och generaliserat utslag, klåda, allvarlig, plötslig livshotande allergisk reaktion.
Hud: hudutslag med vitt silveraktigt färgat utseende (psoriasisliknande utslag) eller förvärrande av psoriasis, fjällande hud, onormal hårkvalitet, inflammation i huden med kliande utslag och rodnad, förändrad hårfärg, förlust av ögonfransar, klåda, onormal hårväxt, hudrodnad.
Muskler: ökade tecken och symtom på myasthenia gravis (muskelrubbning), ovanliga förnimmelser som t.ex. stickningar i huden. Muskelsvaghet/muskeltrötthet, muskelsmärta ej orsakad av träning, ledsmärta.
Njurar och urinvägar: svårighet och smärta vid urinering, ofrivilligt urinläckage.
Reproduktionsorganen: Nedsatt sexuell förmåga, minskad sexuell lust.
Metabolism: låga blodsockernivåer, förhöjt prostataspecifikt antigen.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet. Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på flaskan och ytterkartongen efter EXP. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras vid högst 30 °C.
Du måste kassera flaskan 4 veckor efter att du öppnat den, för att förhindra risken för infektioner, och ta en ny flaska. Varje gång du påbörjar en ny flaska, skriv upp det datum som du öppnat den på avsett utrymme på flaska och kartong.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- De aktiva substanserna är travoprost och timolol. En ml lösning innehåller 40 mikrogram travoprost och 5 mg timolol (som timololmaleat).
- Övriga innehållsämnen är polyquaternium‑1, mannitol (E421), propylenglykol (E1520), makrogolglycerolhydroxistearat (hydrerad ricinolja), borsyra, natriumklorid, natriumhydroxid eller saltsyra (för att justera pH‑värdet) och renat vatten. Små mängder natriumhydroxid eller saltsyra tillsätts för att hålla surhetsgraden (pH-värdet) normal.
Läkemedlets utseende och förpackningsstorlekar
DuoTrav är en vätska (en klar, färglös lösning) som tillhandahålls i en 2,5 ml plastflaska med skruvkork. Varje flaska är förpackad i en skyddspåse.
Förpackningar om 1, 3 eller 6 flaskor.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublin 4
Irland
Tillverkare
Novartis Manufacturing NV
Rijksweg 14
2870 Puurs-Sint-Amands
Belgien
Novartis Farmacéutica, S.A.
Gran Via de les Corts Catalanes, 764
08013 Barcelona
Spanien
Novartis Pharma GmbH
Sophie-Germain-Strasse 10
90443 Nürnberg
Tyskland
Kontakta ombudet för innehavaren av godkännandet för försäljning om du vill veta mer om detta läkemedel:
Suomi/Finland
Novartis Finland Oy
Puh/Tel: +358 (0)10 6133 200
Denna bipacksedel ändrades senast 3.2.2026
Övriga informationskällor
Ytterligare information om detta läkemedel finns på Europeiska läkemedelsmyndighetens webbplats http://www.ema.europa.eu/.