TAKHZYRO injektioneste, liuos, esitäytetty ruisku 300 mg
TAKHZYRO 300 mg injektioneste, liuos, esitäytetty ruisku
lanadelumabi
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin aloitat tämän lääkkeen käyttämisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
- Tämä lääke on määrätty vain sinulle eikä sitä tule antaa muiden käyttöön. Se voi aiheuttaa haittaa muille, vaikka heillä olisikin samanlaiset oireet kuin sinulla.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
1. Mitä TAKHZYRO on ja mihin sitä käytetään
2. Mitä sinun on tiedettävä, ennen kuin käytät TAKHZYROA
3. Miten TAKHZYROA käytetään
4. Mahdolliset haittavaikutukset
5. TAKHZYRON säilyttäminen
6. Pakkauksen sisältö ja muuta tietoa
7. Käyttöohjeet
Mitä valmiste on ja mihin sitä käytetään
TAKHZYRO sisältää vaikuttavana aineena lanadelumabia.
Mihin TAKHZYROA käytetään
TAKHZYRO on angioedeemakohtausten ehkäisyyn tarkoitettu lääke perinnöllistä angioedeemaa (HAE) sairastaville vähintään 2‑vuotiaille potilaille.
Mikä on perinnöllinen angioedeema (HAE)
HAE on tauti, joka esiintyy suvuittain. Tautia sairastavilla ei ole veressä tarpeeksi C1-estäjäproteiinia tai C1-estäjä ei toimi kunnolla. Tämän seurauksena plasman kertyy liikaa kallikreiinia, joka puolestaan tuottaa lisää bradykiniiniä verenkiertoon. Liian suuri määrä bradykiniiniä aiheuttaa HAE:n oireita, kuten turvotusta ja kipua
- käsissä ja jaloissa
- kasvoissa, silmäluomissa, huulissa tai kielessä
- kurkunpäässä, mikä voi vaikeuttaa hengitystä
- sukuelimissä.
Miten TAKHZYRO toimii
TAKHZYRO on proteiini, joka estää plasman kallikreiinin toimintaa. Sen ansiosta bradykiniinin määrä verenkierrossa vähenee ja HAE-oireet estyvät.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä käytä TAKHZYROA
Jos olet allerginen lanadelumabille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa).
Varoitukset ja varotoimet
- Keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen kuin käytät TAKHZYROA.
- Jos TAKHZYRO aiheuttaa sinulle vaikean allergisen reaktion, jonka oireita ovat esimerkiksi ihottuma, rinnanahdistus, hengityksen vinkuminen tai sydämentykytys, kerro siitä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle välittömästi.
Muistiinpanojen teko
On erittäin suositeltavaa, että kirjoitat lääkkeen nimen ja eränumeron muistiin joka kerta ottaessasi TAKHZYRO-annoksen. Sillä tavoin pidät kirjaa käytetyistä lääke-eristä.
Laboratoriotutkimukset
Kerro lääkärille TAKHZYRON käytöstä ennen veren hyytymistä mittaavia laboratoriotutkimuksia, sillä veressä oleva TAKHZYRO saattaa häiritä joitain laboratoriotutkimuksia ja aiheuttaa virheellisiä mittaustuloksia.
Lapset ja nuoret
TAKHZYROA ei suositella käytettäväksi alle 2‑vuotiaille lapsille. Syynä tähän on se, että lääkettä ei ole tutkittu kyseisessä ikäryhmässä.
Muut lääkevalmisteet ja TAKHZYRO
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan otat, olet äskettäin ottanut tai saatat ottaa muita lääkkeitä.
TAKHZYRO-valmisteen ei tiedetä vaikuttavan muihin lääkkeisiin, eikä muiden lääkkeiden tiedetä vaikuttavan TAKHZYRO-valmisteeseen.
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen tämän lääkkeen käytön aloittamista. TAKHZYRO-valmisteen käytön turvallisuudesta raskauden ja imetyksen aikana on rajoitetusti tietoa. Varotoimena lanadelumabin käyttöä on suositeltavaa välttää raskauden ja imetyksen aikana. Lääkäri keskustelee kanssasi tämän lääkkeen ottamisen riskeistä ja eduista.
Ajaminen ja koneiden käyttö
Tällä lääkkeellä ei ole haitallista vaikutusta tai sillä on vähäinen vaikutus ajokykyyn ja koneidenkäyttökykyyn.
TAKHZYRO sisältää natriumia
Tämä lääke sisältää alle 1 mmol natriumia (23 mg) per esitäytetty ruisku eli sen voidaan sanoa olevan ”natriumiton”.
Miten valmistetta käytetään
TAKHZYRO toimitetaan kertakäyttöisissä esitäytetyissä ruiskuissa käyttövalmiina liuoksena. Hoito aloitetaan ja sitä seurataan HAE-potilaiden hoitoon perehtyneen lääkärin valvonnassa.
Käytä tätä lääkettä juuri siten kuin tässä pakkausselosteessa kuvataan tai kuten lääkäri on määrännyt tai apteekkihenkilökunta tai sairaanhoitaja on neuvonut. Tarkista ohjeet lääkäriltä, apteekista tai sairaanhoitajalta, jos olet epävarma tai jos sinulla on kysymyksiä tämän lääkkeen käytöstä.
Kuinka paljon TAKHZYROA käytetään
Aikuisille ja 12 – < 18 vuoden ikäisille nuorille:
- Suositeltu aloitusannos on 300 mg lanadelumabia 2 viikon välein. Jos et ole saanut kohtausta pitkään aikaan, lääkäri saattaa muuttaa annostuksen 300 mg:aan lanadelumabia 4 viikon välein, etenkin, jos painosi on alhainen.
- Alle 40 kg painaville potilaille voidaan myös harkita aloitusannosta 150 mg lanadelumabia 2 viikon välein. Jos et ole saanut kohtausta pitkään aikaan, lääkäri saattaa muuttaa annostuksen 150 mg:aan lanadelumabia 4 viikon välein.
Lapsille, jotka ovat 2 – < 12 vuoden ikäisiä, suositeltu annos perustuu ruumiinpainoon:
| Paino (kg) |
Suositeltu aloitusannos |
Annoksen muuttaminen |
| 10 – < 20 kg |
150 mg lanadelumabia 4 viikon välein |
Niille potilaille, joiden kohtauksia ei saada hallintaan, voidaan harkita annoksen suurentamista annokseen 150 mg lanadelumabia 3 viikon välein |
| 20 – < 40 kg |
150 mg lanadelumabia 2 viikon välein |
Niille potilaille, joiden tila on vakaa ja kohtaukseton hoidon aikana, voidaan harkita annoksen pienentämistä annokseen 150 mg lanadelumabia 4 viikon välein |
| Vähintään 40 kg |
300 mg lanadelumabia 2 viikon välein |
Niille potilaille, joiden tila on vakaa ja kohtaukseton hoidon aikana, voidaan harkita annoksen pienentämistä annokseen 300 mg lanadelumabia 4 viikon välein |
- Jos lapsesi tai hoidossasi oleva lapsi painaa 20 – < 40 kg eikä hän ole saanut kohtausta pitkään aikaan, lääkäri voi mahdollisesti antaa hänen jatkaa samalla annoksella myös sen jälkeen, kun hän on täyttänyt 12 vuotta.
Miten TAKHZYRO pistetään
Jos pistät itse tai sinua hoitava henkilö pistää TAKHZYRON, sinun tai sinua hoitavan henkilön pitää lukea huolellisesti ohjeet kohdassa 7, "Käyttöohjeet", ja noudattaa niitä.
- TAKHZYRO annetaan pistoksena ihon alle (ihonalainen pistos).
- Pistoksen voit antaa joko sinä itse tai sen voi antaa sinua hoitava henkilö, jos olet vähintään 12 vuoden ikäinen.
- Pistoksen voi antaa joko terveydenhuollon ammattilainen tai potilasta hoitava henkilö, jos potilas on 2 – < 12 vuoden ikäinen.
- Lääkärin, apteekkihenkilökunnan tai sairaanhoitajan on näytettävä sinulle, miten TAKHZYRO valmistellaan ja pistetään oikein, ennen kuin käytät sitä ensimmäistä kertaa. Älä pistä itse tai anna kenenkään muun pistää, ennen kuin olet saanut opastuksen lääkkeen pistämisestä.
- Pistä neula vatsan, reiden tai olkavarren rasvakudokseen.
- Pistä lääke joka kerta eri kohtaan.
- Jokainen esitäytetty TAKHZYRO-ruisku on kertakäyttöinen.
Jos käytät enemmän TAKHZYROA kuin sinun pitäisi
Kerro lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle, jos otat liikaa TAKHZYROA.
Jos unohdat ottaa TAKHZYROA
Jos unohdat ottaa TAKHZYRO-annoksen, pistä annos mahdollisimman pian. Antoaikataulua voi olla tarpeen muuttaa halutun antovälin mukaan, jotta varmistetaan, että
- antoväli on vähintään 10 vuorokautta, jos potilas saa hoitoa 2 viikon välein
- antoväli on vähintään 17 vuorokautta, jos potilas saa hoitoa 3 viikon välein
- antoväli on vähintään 24 vuorokautta, jos potilas saa hoitoa 4 viikon välein.
Ellet ole varma siitä, milloin sinun pitää pistää TAKHZYRO unohtuneen annoksen jälkeen, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
Jos lopetat TAKHZYRON käytön
On tärkeää, että jatkat TAKHZYRON pistämistä lääkärin ohjeiden mukaan, vaikka tuntisit olosi paremmaksi. Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Jos TAKHZYRO aiheuttaa sinulle vaikean allergisen reaktion, jonka oireita ovat esimerkiksi ihottuma, rinnanahdistus, hengityksen vinkuminen tai sydämentykytys, kerro siitä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle välittömästi.
Kerro lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle, jos sinulle ilmenee mikä tahansa seuraavista haittavaikutuksista.
Hyvin yleiset haittavaikutukset (voi ilmetä yli 1 henkilöllä kymmenestä):
- Reaktiot pistoskohdassa – oireita ovat esimerkiksi kipu, ihon punoitus, mustelmat, epämukava tunne, turvotus, verenvuoto, kutina, ihon kovettuminen, pistely, lämmön tunne ja ihottuma.
Yleiset haittavaikutukset (voi ilmetä enintään 1 henkilöllä kymmenestä)
- Allergiset reaktiot, kuten kutina, epämiellyttävä tunne ja pistelyä kielessä
- Huimaus, pyörrytys
- Koholla oleva ihottuma
- Lihaskipu
- Maksa-arvojen muutokset verikokeissa
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
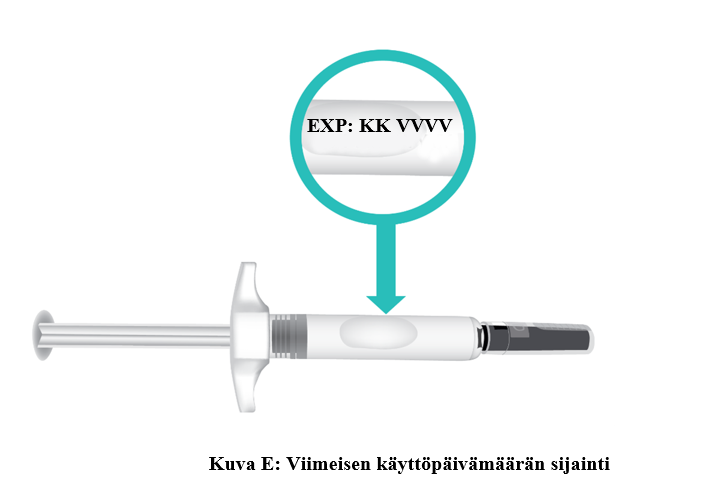
Älä käytä tätä lääkettä etiketissä ja pakkauksessa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
TAKHZYRO 300 mg injektioneste, liuos, esitäytetty ruisku
Säilytä jääkaapissa (2 °C–8 °C). Ei saa jäätyä. Pidä injektiopullo ulkopakkauksessa. Herkkä valolle.
Esitäytettyjä ruiskuja voi säilyttää alle 25 °C:n lämpötilassa yhden 14 vuorokautta kestävän jakson ajan, muttei viimeistä käyttöpäivämäärää kauemmin.
Älä siirrä huoneenlämmössä säilytettyä TAKHZYROA takaisin jääkaappiin.
Kun yksi esitäytetty ruisku on otettu jääkaapissa säilytettävästä monipakkauksesta, palauta monipakkaukseen jääneet esitäytetyt ruiskut jääkaappiin seuraavaa käyttöä varten.
Älä käytä tätä lääkettä, jos huomaat näkyviä muutoksia lääkevalmisteen ulkonäössä, kuten hiukkasia esitäytetyssä ruiskussa tai injektionesteen muuttunut väri.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä TAKHZYRO sisältää
- Vaikuttava aine on lanadelumabi. Jokainen esitäytetty ruisku sisältää 300 mg lanadelumabia 2 ml:ssa liuosta.
- Muut aineet ovat dinatriumfosfaattidihydraatti, sitruunahappomonohydraatti, histidiini, natriumkloridi, polysorbaatti 80 ja injektionesteisiin käytettävä vesi – ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä "TAKHZYRO sisältää natriumia".
Lääkevalmisteen kuvaus ja pakkauskoot
TAKHZYRO on kirkas ja väritön tai hieman kellertävä injektioliuos esitäytetyssä ruiskussa.
TAKHZYRO on saatavissa:
- yksittäispakkauksessa, jossa on yksi 2 ml:n esitäytetty ruisku kotelossa
- yksittäispakkauksessa, jossa on kaksi 2 ml:n esitäytettyä ruiskua kotelossa
- monipakkauksessa, jossa on kolme pakkausta ja niistä kussakin kaksi 2 ml:n esitäytettyä ruiskua.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija ja valmistaja
Myyntiluvan haltija
Takeda Pharmaceuticals International AG Ireland Branch
Block 2 Miesian Plaza
50-58 Baggot Street Lower
Dublin 2
D02 HW68
Irlanti
Valmistaja
Takeda Pharmaceuticals International AG Ireland Branch
Block 2 Miesian Plaza
50-58 Baggot Street Lower
Dublin 2
D02 HW68
Irlanti
Shire Pharmaceuticals Ireland Limited
Blocks 2 & 3 Miesian Plaza
50-58 Baggot Street Lower
Dublin 2
Irlanti
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
Takeda Oy
Puh/Tel: 0800 774 051
Tämä pakkausseloste on tarkistettu viimeksi 03/2024.
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla: http://www.ema.europa.eu . Siellä on myös linkkejä muille harvinaisia sairauksia ja niiden hoitoja käsitteleville verkkosivuille.
Ohjeet käyttäjälle
7. Käyttöohjeet
Varmista, että olet lukenut ja ymmärtänyt nämä TAKHZYRON pistämisen käyttöohjeet ja pystyt noudattamaan niitä. Jos sinulla on kysyttävää, käänny hoidostasi vastaavan terveydenhuollon ammattilaisen puoleen.
Käyttötarkoitus
Esitäytetty TAKHZYRO-ruisku on kiinteäannoksinen (300 mg/2 ml), käyttövalmis, kertakäyttöinen, neulapohjainen injektiolaite, joka on tarkoitettu lääkevalmisteen antamiseen ihon alle terveydenhuollon ammattilaisen, hoitohenkilökunnan tai potilaan itsensä pistämänä (vähintään 12 vuoden ikäiset potilaat).
TAKHZYRON säilyttäminen
- Säilytä esitäytetty TAKHZYRO-ruisku jääkaapissa (2 °C–8 °C). Ei saa jäätyä.
- Jääkaapista otettu esitäytetty ruisku on säilytettävä alle 25 °C:n lämpötilassa ja käytettävä 14 vuorokauden kuluessa. Älä siirrä huoneenlämmössä säilytettyä TAKHZYROA takaisin jääkaappiin.
- Kun yksi esitäytetty ruisku on otettu jääkaapissa säilytettävästä monipakkauksesta, palauta monipakkaukseen jääneet esitäytetyt ruiskut jääkaappiin seuraavaa käyttöä varten.
- TAKHZYRO on säilytettävä alkuperäisessä pakkauksessaan esitäytetyn ruiskun suojaamiseksi valolta.
- Hävitä esitäytetty TAKHZYRO-ruisku, jos sitä on säilytetty jääkaapin ulkopuolella, se on päässyt jäätymään tai sitä ei ole säilytetty alkuperäispakkauksessa valolta suojattuna.
- Älä ravista TAKHZYROA.
- Pidä TAKHZYRO ja kaikki muut lääkkeet poissa lasten ulottuvilta.
Esitäytetyn TAKHZYRO-ruiskun osat ennen käyttöä (kuva A).
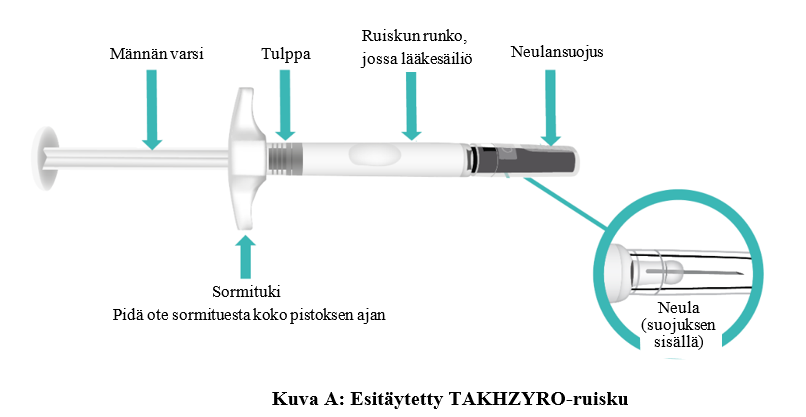
VAIHE 1: Valmistele injektio
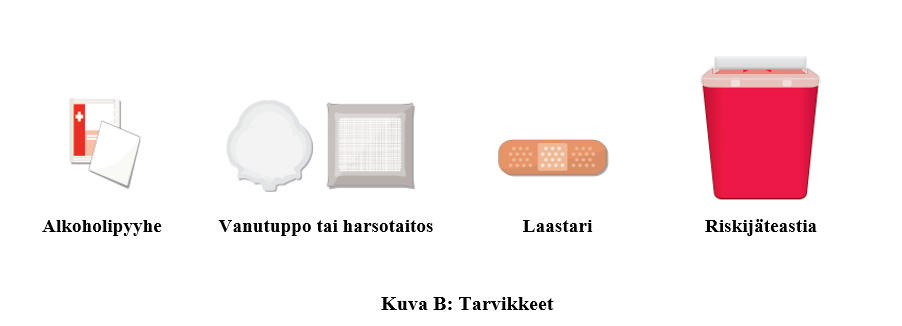
a. Kerää alkoholipyyhe, vanutuppo tai harsotaitos, laastari ja riskijäteastia (kuva A), ja aseta ne puhtaalle, tasaiselle pinnalle hyvin valaistulle alueelle. Nämä tarvikkeet eivät sisälly TAKHZYRO-pakkaukseen.
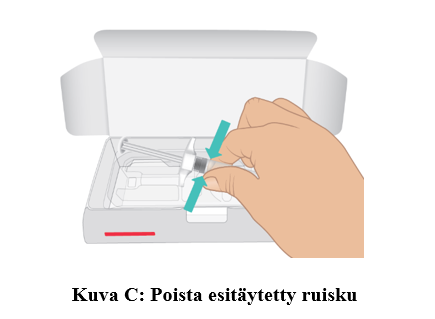
b. Ota esitäytetty TAKHZYRO-ruisku jääkaapista.
- Älä käytä esitäytettyä TAKHZYRO-ruiskua, jos pakkauksen sinetti on avattu tai rikki.
- Ennen kuin valmistelet injektion, anna esitäytetyn ruiskun lämmetä vähintään 15 minuutin ajan huoneenlämpöiseksi.
- Lääkkeesi on herkkä korkeille lämpötiloille. Älä lämmitä esitäytettyä TAKHZYRO-ruiskua lämmönlähteillä, kuten mikroaaltouunilla tai kuumalla vedellä.
- Älä irrota neulansuojusta, ennen kuin olet valmis pistämään.

c. Avaa pakkaus. Tartu esitäytettyyn TAKHZYRO-ruiskuun sen rungosta ja poista ruisku alustalta (kuva C).
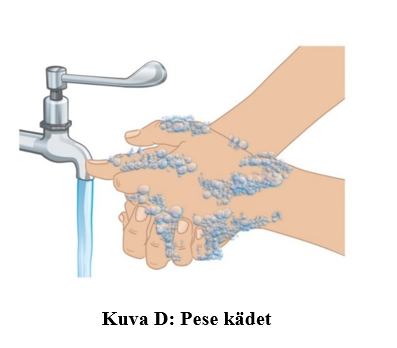
d. Pese kädet saippualla ja vedellä (kuva D). Kuivaa kädet huolellisesti.
- Kädet pestyäsi älä koske mihinkään pintaan tai kehon osaan ennen pistoksen antamista.
e. Tarkista viimeinen käyttöpäivämäärä (EXP) ruiskun rungosta (kuva E).
- Älä käytä esitäytettyä TAKHZYRO-ruiskua, jos viimeinen käyttöpäivämäärä on mennyt. Jos esitäytetyn TAKHZYRO-ruiskun viimeinen käyttöpäivä on mennyt, hävitä ruisku riskijäteastiaan ja ota yhteys hoidostasi vastaavaan terveydenhuollon ammattilaiseen.
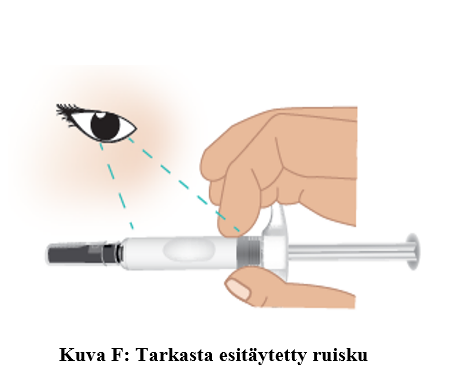
f. Tarkasta esitäytetty TAKHZYRO-ruisku vaurioiden varalta ja varmista, että lääke on väritöntä tai hieman kellertävää (kuva F).
- Älä käytä valmistetta, jos ruisku on vaurioitunut – esim. ruiskuosa on murtunut.
- Älä käytä esitäytettyä TAKHZYRO-ruiskua, jos lääkkeen väri on muuttunut, lääke on sameaa tai siinä on hiutaleita tai hiukkasia.
- Esitäytetyssä TAKHZYRO-ruiskussa saattaa näkyä ilmakuplia. Tämä on normaalia eikä vaikuta annokseesi.
Jos et voi käyttää esitäytettyä ruiskua, ota yhteys hoidostasi vastaavaan terveydenhuollon ammattilaiseen.
VAIHE 2: Valitse ja valmistele pistoskohta
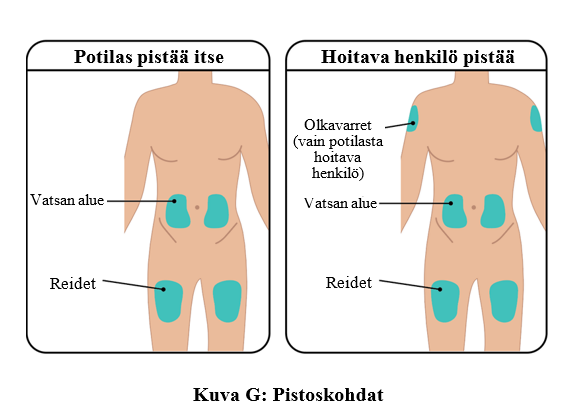
a. Esitäytetty TAKHZYRO-ruisku on pistettävä ainoastaan seuraaviin kohtiin (kuva G):
- vatsan alue
- reidet
- olkavarret (vain, jos pistoksen antaa terveydenhuollon ammattilainen tai potilasta hoitava henkilö).
- Älä valitse pistoskohtaa ihoalueelta, joka on ärtynyt, punoittava, mustelmilla tai infektoitunut.
- Valitsemasi pistoskohdan on oltava vähintään 5 cm:n etäisyydellä arvista tai navasta.
Tärkeää:
Vaihtele pistoskohtia, jotta iho pysyy terveenä. Uuden pistoskohdan on oltava aina vähintään 3 cm:n etäisyydellä edellisestä pistoskohdasta.
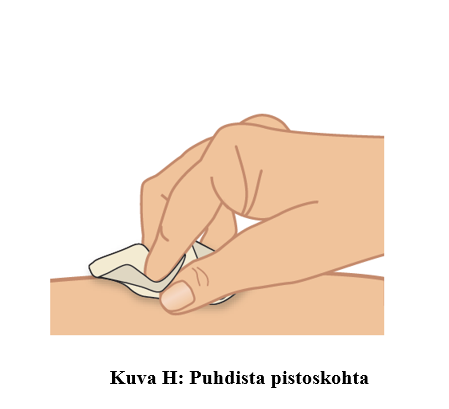
b. Puhdista pistoskohta alkoholipyyhkeellä ja anna sen kuivua kunnolla (kuva H).
- Älä tuuleta tai puhalla puhdasta kohtaa.
- Älä kosketa tätä kohtaa, ennen kuin suoritat pistoksen.
Pitele toisella kädellä esitäytettyä TAKHZYRO-ruiskua tukevasti ruiskun keskeltä ja vedä neulansuojus varovasti suoraan irti toisella kädellä. Hävitä neulansuojus roska-astiaan tai riskijäteastiaan (kuva I).
- Älä kosketa tai työnnä mäntää, ennen kuin olet valmis pistämään.
- Jotta vältät neulanpistovammat, älä aseta esitäytetyn TAKHZYRO-ruiskun neulansuojusta takaisin paikalleen.
- Älä käytä esitäytettyä TAKHZYRO-ruiskua, jos se on pudonnut ilman neulansuojusta.
- Älä käytä esitäytettyä TAKHZYRO-ruiskua, jos neula näyttää vaurioituneelta tai taipuneelta.
- Älä kosketa neulaa äläkä päästä sitä koskettamaan mihinkään.
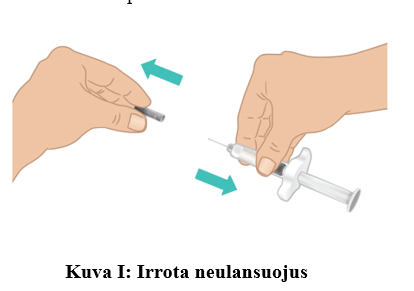
VAIHE 3: Suorita TAKHZYRO-pistos
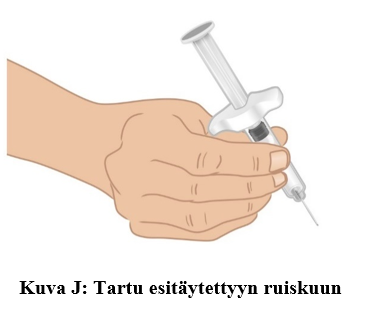
a. Tartu esitäytettyyn TAKHZYRO-ruiskuun toisella kädellä kuin kynään (kuva J). Vältä neulan koskettamista tai männän työntämistä.
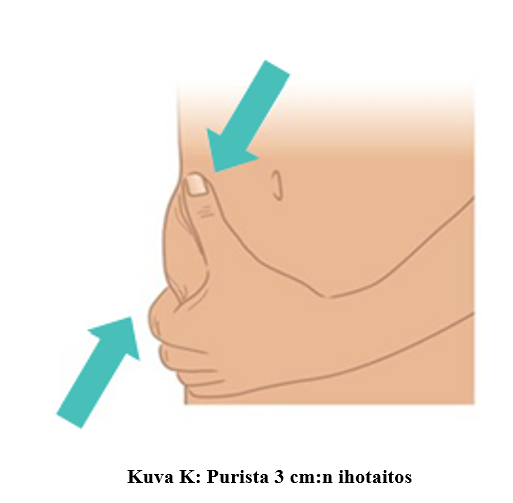
b. Purista toisella kädellä kevyesti noin 3 cm:n ihotaitos puhdistetusta pistoskohdasta.
- Jatka puristamista, kunnes pistos on annettu ja neula poistettu ihosta (kuva K).
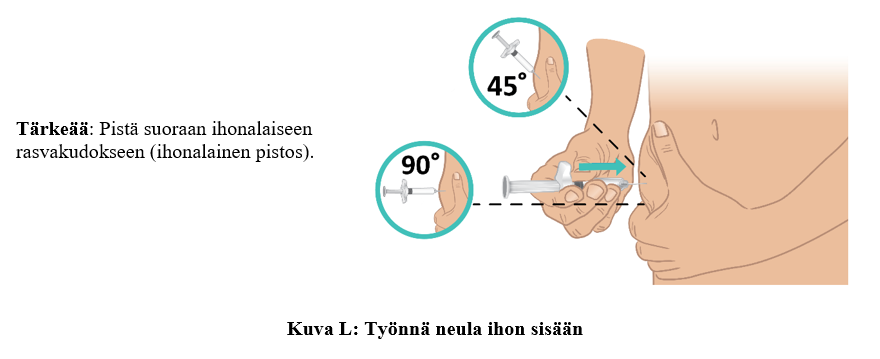
c. Työnnä neula kokonaan ihon sisään 45–90 asteen kulmassa yhdellä nopealla, lyhyellä liikkeellä. Varmista, että neula pysyy paikallaan (kuva L).
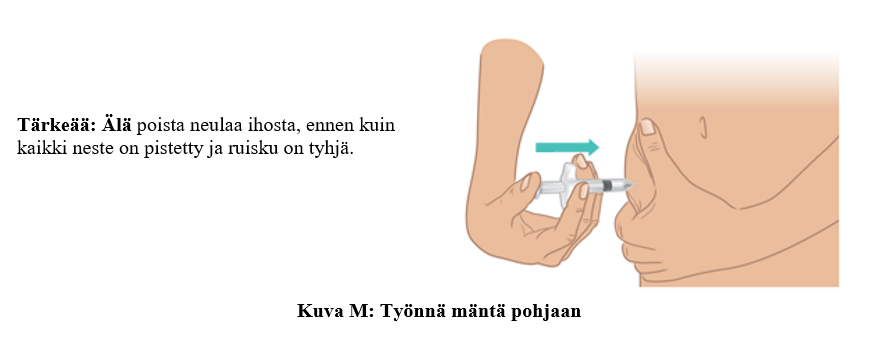
d. Työnnä mäntä hitaasti pohjaan, kunnes se ei enää mene pidemmälle (kuva M).
e. Vedä neula hitaasti irti ihosta niin, että ruisku pysyy samassa kulmassa. Päästä ote ihosta varovasti.

f. Paina vanutuppo tai harsotaitos tarvittaessa pistoskohdan päälle ja pidä se paikallaan 10 sekunnin ajan.
- Älä hankaa pistoskohtaa. Pistoskohdasta saattaa vuotaa hieman verta. Tämä on normaalia.
- Peitä pistoskohta tarvittaessa laastarilla.
g. Hävitä käytetty esitäytetty TAKHZYRO-ruisku.
- Laita käytetty esitäytetty TAKHZYRO-riskijäteastiaan heti käytön jälkeen (kuva O).
- Jotta vältät neulanpistovammat, älä aseta neulansuojusta takaisin neulan päälle.
- Älä käytä esitäytettyä TAKHZYRO-ruiskua tai mitään injektiotarvikkeita uudelleen.
- Älä kosketa neulaa.
Tärkeää: Pidä riskijäteastia aina poissa lasten ulottuvilta.
