VOLIBRIS filmdragerad tablett 5 mg, 10 mg
Tilläggsinformation
Volibris 2,5 mg filmdragerade tabletter
Volibris 5 mg filmdragerade tabletter
Volibris 10 mg filmdragerade tabletter
ambrisentan
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare, apotekspersonal eller sjuksköterska.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad Volibris är och vad det används för
2. Vad du behöver veta innan du tar Volibris
3. Hur du tar Volibris
4. Eventuella biverkningar
5. Hur Volibris ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Volibris innehåller den aktiva substansen ambrisentan. Det hör till en grupp läkemedel som kallas övriga antihypertensiva medel (används för att behandla högt blodtryck).
Det används för att behandla pulmonell arteriell hypertension (PAH) hos vuxna, ungdomar och barn från 8 års ålder. PAH är högt blodtryck i de blodkärl (lungartärerna) som transporterar blod från hjärtat till lungorna. Hos personer med PAH blir dessa artärer trängre så att hjärtat måste arbeta hårdare för att pumpa blod genom dem. Detta gör att man känner sig trött, yr och andfådd.
Volibris vidgar lungartärerna och gör det lättare för hjärtat att pumpa blod genom dem. Detta sänker blodtrycket och lindrar symtomen.
Volibris kan även användas i kombination med andra läkemedel som används för att behandla PAH.
Vad du behöver veta innan produkten används
Ta inte Volibris
- om du är allergisk mot ambrisentan, soja eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar)
- om du är gravid, om du planerar att bli gravid eller om du kan bli gravid eftersom du inte använder ett tillförlitligt preventivmedel. Läs informationen under ”Graviditet”
- om du ammar. Läs informationen under ”Amning”
- om du har leversjukdom. Tala med din läkare som bestämmer om detta läkemedel är lämpligt för dig
- om du har ärrbildning på lungorna, av okänd orsak (idiopatisk lungfibros).
Varningar och försiktighet
Tala med läkare innan du tar detta läkemedel:
- om du har leverproblem
- om du har anemi (minskat antal röda blodkroppar)
- om du har svullna händer, anklar eller fötter orsakat av vätskeansamling (perifert ödem)
- om du har lungsjukdom som innebär att venerna i lungorna är blockerade (pulmonell veno-ocklusiv sjukdom).
→ Din läkare bestämmer om Volibris är lämpligt för dig.
Du behöver ta blodprov regelbundet Innan du börjar ta Volibris och regelbundet under tiden du tar det, kommer läkaren att ta blodprov för att kontrollera:
- om du har anemi
- om din lever fungerar som den ska.
→ Det är viktigt att du lämnar dessa regelbundna blodprover så länge du tar Volibris.
Tecken på att din lever kanske inte fungerar som den ska är till exempel:
- aptitförlust
- illamående
- kräkningar
- feber
- magont
- gulfärgning av huden eller ögonvitorna (gulsot)
- mörkfärgad urin
- klåda i huden.
Om du upptäcker något av dessa tecken:
→ Tala om det för din läkare omedelbart.
Barn
Ge inte detta läkemedel till barn under 8 års ålder eftersom säkerhet och effekt inte är känd för denna åldersgrupp.
Andra läkemedel och Volibris
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel.
Om du börjar ta ciklosporin A (ett läkemedel som används efter transplantation eller för att behandla psoriasis) kan din läkare behöva justera din dos Volibris.
Om du tar rifampicin (ett antibiotikum som används för att behandla allvarliga infektioner) kommer din läkare att kontrollera dig tätare när du börjar ta Volibris.
Om du tar andra läkemedel som används för att behandla PAH (t.ex. iloprost, epoprostenol, sildenafil) kan din läkare behöva kontrollera dig tätare.
→ Tala om för din läkare eller apotekspersonal om du tar något av dessa läkemedel.
Graviditet
Volibris kan skada det ofödda barnet om du blivit gravid före, under eller strax efter behandling.
→ Om det är möjligt att du kan bli gravid ska du använda ett tillförlitligt preventivmedel under tiden du tar Volibris. Diskutera det här med din läkare.
→ Ta inte Volibris om du är gravid eller planerar att bli gravid.
→ Om du blir gravid eller misstänker att du kan vara gravid under tiden du tar Volibris, kontakta omedelbart läkare.
Om du är kvinna och kan bli gravid kommer läkaren att be dig göra ett graviditetstest innan du börjar ta Volibris och regelbundet under tiden du tar detta läkemedel.
Amning
Det är inte känt om den aktiva substansen i Volibris kan gå över i bröstmjölk.
→ Amma inte under tiden du tar Volibris. Diskutera det här med din läkare.
Fertilitet
Om du är man och tar Volibris kan det finnas en risk att Volibris minskar antalet spermier. Tala med din läkare om du har några frågor gällande detta.
Körförmåga och användning av maskiner
Volibris kan ge biverkningar, som till exempel lågt blodtryck, yrsel, trötthet (se avsnitt Eventuella biverkningar) vilka kan påverka din förmåga att framföra fordon eller använda maskiner. Symtomen på din sjukdom kan också göra dig mindre lämpad att framföra fordon eller använda maskiner.
→ Kör inte något fordon och använd inte maskiner om du inte känner dig bra.
Volibris innehåller laktos
Volibris tabletter innehåller små mängder av en sockerart som kallas laktos. Om din läkare har sagt till dig att du inte tål vissa sockerarter:
→ Kontakta din läkare innan du tar detta läkemedel.
Volibris innehåller lecitin som kommer från soja
Om du är allergisk mot soja, ta inte detta läkemedel (se avsnitt Vad du behöver veta innan produkten används ”Ta inte Volibris”).
Volibris 5 mg och 10 mg tabletter innehåller ett färgämne som heter allurarött AC aluminiumlack (E129)
Detta kan ge allergiska reaktioner (se avsnitt Eventuella biverkningar).
Volibris innehåller natrium
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per tablett, dvs. är näst intill ”natriumfritt”.
Hur produkten används
Använd alltid detta läkemedel enligt läkarens eller apotekspersonalens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
Hur mycket Volibris du ska ta
Vuxna
Den vanliga dosen Volibris är en 5 mg tablett en gång om dagen. Läkaren kan bestämma att öka dosen till 10 mg en gång om dagen.
Om du tar ciklosporin A, ta inte mer än en 5 mg tablett Volibris en gång dagligen.
Ungdomar och barn i åldern 8 år till yngre än 18 år
| Vanlig startdos av Volibris | |
| Väger 35 kg eller mer |
En 5 mg tablet en gång dagligen |
| Väger minst 20 kg och mindre än 35 kg | En 2,5 mg tablett en gång dagligen |
Läkaren kan besluta att öka dosen. Det är viktigt att barn kommer till sina regelbundna läkarbesök eftersom dosen kan behöva justeras i takt med att de blir äldre eller ökar i vikt.
Vid samtidigt intag av ciklosporin A kommer dosen av Volibris för ungdomar och barn som väger mindre än 50 kg att begränsas till 2,5 mg en gång dagligen eller 5 mg en gång dagligen om de väger 50 kg eller mer.
Hur du tar Volibris Det är bäst att ta tabletten vid samma tidpunkt varje dag. Svälj tabletten hel med ett glas vatten. Tabletten ska inte delas, krossas eller tuggas. Du kan ta Volibris med eller utan mat.
Att ta ut en tablett från en blisterkarta (endast 5 mg och 10 mg tabletter)
Tabletterna tillhandahålls i speciella förpackningar för att förhindra att barn tar ut dem.
1. Ta loss en tablett: riv längs den perforerade linjen för att ta loss en blisterficka från kartan.
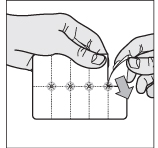
2. Dra av ytterhöljet: börja vid det färgade hörnet, lyft upp och dra längs blisterfickan.
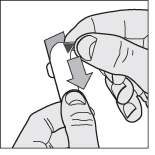
3. Tryck ut tabletten: tryck försiktigt ena änden av tabletten genom foliehöljet.
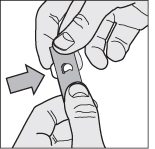
Volibris 2,5 mg är förpackade i en burk, inte blisterkartor.
Om du har tagit för stor mängd av Volibris
Om du tar för många tabletter är risken större att du får biverkningar såsom huvudvärk, blodvallningar, yrsel, illamående eller lågt blodtryck vilket kan orsaka yrsel.
→ Fråga läkare eller apotekspersonal om råd om du tar fler tabletter än ordinerat.
Om du har glömt att ta Volibris
Om du har glömt att ta en dos Volibris, ta den så snart som möjligt. Fortsätt sedan att ta medicinen enligt föreskrift.
→ Ta inte dubbel dos för att kompensera för den glömda dosen.
Om du slutar att använda Volibris
Volibris är en behandling som du måste fortsätta att ta för att kontrollera din PAH.
→Sluta inte ta Volibris utan att du har kommit överens om det med din läkare.
Om du har ytterligare frågor om detta läkemedel, kontakta läkare eller apotekspersonal.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem.
Allvarliga biverkningar
Tala om för din läkare om du får något av följande:
Allergiska reaktioner
Detta är en vanlig biverkan som kan förekomma hos upp till 1 av 10 användare. Du kan få utslag eller klåda och svullnad (vanligtvis i ansikte, läppar, tunga eller hals), vilket kan orsaka andnings- eller sväljsvårigheter.
Svullnad (ödem), speciellt av anklar och fötter
Detta är en mycket vanlig biverkan som kan förekomma hos fler än 1 av 10 användare.
Hjärtsvikt
Detta beror på att hjärtat inte pumpar ut tillräckligt med blod. Detta är en vanlig biverkning som kan förekomma hos upp till 1 av 10 användare. Symtomen inkluderar:
- andnöd
- extrem trötthet
- svullna anklar och ben.
Minskat antal röda blodkroppar (anemi)
Detta är en mycket vanlig biverkan som kan förekomma hos fler än 1 av 10 användare. Ibland kräver detta en blodtransfusion. Symtomen inkluderar:
- trötthet och svaghet
- andnöd
- allmän sjukdomskänsla.
Lågt blodtryck (hypotoni)
Det är en vanlig biverkan som kan förekomma hos upp till 1 av 10 användare. Symtomen inkluderar:
- yrsel.
→Tala omedelbart om för läkare om du (eller ditt barn) får dessa biverkningar eller om de inträffar plötsligt efter att du (eller ditt barn) har använt Volibris.
Det är viktigt att du tar regelbundna blodprover, för att kontrollera om du har anemi och att din lever fungerar som den ska. Se till att du också har läst informationen i avsnitt Vad du behöver veta innan produkten används under ”Du behöver ta blodprov regelbundet” och ”Tecken på att din lever kanske inte fungerar som den ska”.
Andra biverkningar
Mycket vanliga (kan förekomma hos fler än 1 av 10 användare)
- huvudvärk
- yrsel
- hjärtklappning (snabba eller oregelbundna hjärtslag)
- andnöd som förvärras strax efter att behandlingen med Volibris påbörjats
- rinnande eller täppt näsa, täppthet eller smärtor i bihålorna
- illamående
- diarré
- trötthet.
I kombination med tadalafil (ett annat läkemedel mot PAH)
Förutom de ovanstående:
- blodvallningar (hudrodnad)
- kräkningar
- smärtor/obehag i bröstet.
Vanliga (kan förekomma hos upp till 1 av 10 användare)
- dimsyn eller andra synförändringar
- svimning
- onormala resultat på blodprov för leverfunktion
- rinnande näsa
- förstoppning
- magont
- bröstsmärta eller obehag
- blodvallningar (hudrodnad)
- kräkningar
- svaghetskänsla
- näsblod
- hudutslag.
I kombination med tadalafil (ett annat läkemedel mot PAH)
Förutom de ovanstående, (undantaget onormala leverfunktionsvärden):
- tinnitus (öronsusningar).
Mindre vanliga (kan förekomma hos upp till 1 av 100 användare)
- leverskada
- inflammation i levern orsakad av kroppens eget immunförsvar (autoimmun hepatit).
I kombination med tadalafil
- plötslig hörselnedsättning.
Biverkningar hos barn och ungdomar
Dessa förväntas vara liknande som hos vuxna.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet. Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på förpackningen efter EXP.
Utgångsdatumet är den sista dagen i angiven månad.
Inga särskilda förvaringsanvisningar.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
Den aktiva substansen är ambrisentan
Varje filmdragerad tablett innehåller 2,5 mg, 5 mg eller 10 mg ambrisentan.
För 2,5 mg tabletter:
Övriga innehållsämnen är: laktosmonohydrat, mikrokristallin cellulosa, kroskarmellosnatrium, magnesiumstearat, polyvinylalkohol, talk, titandioxid (E171), makrogol och lecitin (soja) (E322).
För 5 mg och 10 mg tabletter:
Övriga innehållsämnen är: laktosmonohydrat, mikrokristallin cellulosa, kroskarmellosnatrium, magnesiumstearat, polyvinylalkohol, talk, titandioxid (E171), makrogol, lecitin (soja) (E322) och allurarött AC aluminiumlack (E129).
Läkemedlets utseende och förpackningsstorlekar
Volibris 2,5 mg filmdragerad tablett (tablett) är en vit, 7 mm rund, konvex tablett med ”GS” präglat på ena sidan och ”K11” på den andra sidan.
Volibris 5 mg filmdragerad tablett (tablett) är en 6,6 mm ljusrosa, fyrkantig, konvex tablett med ”GS” präglat på ena sidan och ”K2C” på den andra sidan.
Volibris 10 mg filmdragerad tablett (tablett) är en 9,8 mm x 4,9 mm mörkrosa, oval, konvex tablett med ”GS” präglat på ena sidan och ”KE3” på den andra sidan.
Volibris finns som 2,5 mg filmdragerade tabletter i burkar. Varje burk innehåller 30 tabletter.
Volibris finns som 5 mg och 10 mg filmdragerade tabletter i endosblisterförpackningar om 10x1 eller 30x1 tabletter.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning
GlaxoSmithKline Trading Services Limited
12 Riverwalk
Citywest Business Campus
Dublin 24
Irland
D24 YK11
Tillverkare
GlaxoSmithKline Trading Services Limited
12 Riverwalk
Citywest Business Campus
Dublin 24
Irland
För ytterligare upplysningar om detta läkemedel, kontakta ombudet för innehavaren av godkännandet för försäljning:
Suomi/Finland
GlaxoSmithKline Oy
Puh/Tel: + 358 (0)10 30 30 30
Denna bipacksedel ändrades senast 04/2026
Övriga informationskällor
Ytterligare information om detta läkemedel finns tillgänglig på Europeiska läkemedelsmyndighetens webbplats http://www.ema.europa.eu/. Där finns också länkar till andra hemsidor rörande sällsynta sjukdomar och behandlingar