INNOHEP injektionsvätska, lösning i endosspruta 8000 anti-Xa IU, 10000 anti-Xa IU, 12000 anti-Xa IU, 14000 anti-Xa IU, 16000 anti-Xa IU, 18000 anti-Xa IU
Tilläggsinformation
innohep 8 000 anti-Xa IU injektionsvätska, lösning, förfylld spruta
innohep 10000 anti-Xa IU injektionsvätska, lösning, förfylld spruta
innohep 12000 anti-Xa IU injektionsvätska, lösning, förfylld spruta
innohep 14000 anti-Xa IU injektionsvätska, lösning, förfylld spruta
innohep 16000 anti-Xa IU injektionsvätska, lösning, förfylld spruta
innohep 18000 anti-Xa IU injektionsvätska, lösning, förfylld spruta
tinzaparinnatrium
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad innohep är och vad det används för
2. Vad du behöver veta innan du använder innohep
3. Hur du använder innohep
4. Eventuella biverkningar
5. Hur innohep ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
innohep används för behandling av blodpropp i djupa venösa blodkärl och vid blodpropp i lunga hos vuxna.
innohep kan även användas för att behandla blodpropp och förebygga ny blodpropp vid cancer hos vuxna.
Om läkaren angivit annat användningsområde, är det läkarens anvisning som ska följas.
Vad du behöver veta innan produkten används
Använd inte innohep
- vid ökad blödningsrisk (generell eller lokal), infektion i hjärtat, hjärnblödning eller blödande magsår
- om du är allergisk mot tinzaparin eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
Vid ryggmärgsprov eller annan ryggbedövning ska innohep avbrytas minst 24 timmar före proceduren utförs. innohep får inte börja användas före minst 4-6 timmar efter proceduren avslutats.
Varningar och försiktighet
Tala med läkare eller apotekspersonal innan du använder innohep:
- vid kraftigt nedsatt njurfunktion
- om du har en förhöjd risk att drabbas av blödningar eller om du har brist på blodplättar (trombocytopeni)
- om du har diabetes
- om du har astma
- om du har förhöjda kaliumvärden i blodet
- vid ryggmärgsprov eller ryggbedövning
- om du har inopererad hjärtklaffsprotes
- om du är äldre med nedsatt njurfunktion.
innohep ska ej ges i muskel. På grund av risken för blödningar under huden ska även andra läkemedel som ges i en muskel inte ges samtidigt.
Patienter som behandlas med innohep och som får ryggbedövning ska kontrolleras noggrant för att upptäcka eventuell påverkan av ryggmärgen i form av muskelsvaghet eller nedsatt känsel.
Andra läkemedel och innohep
Tala om för läkare eller apotekspersonal om du använder, nyligen har använt eller kan tänkas använda andra läkemedel. En del läkemedel kan påverka effekten av innohep.
Vissa läkemedel påverkar blodet och dess förmåga att levra sig (koagulation). Eftersom innohep gör att du blöder lättare kan kombination med dessa läkemedel öka blödningsrisken. Tala med din läkare om du använder något av följande läkemedel:
- Läkemedel för behandling av inflammation eller smärta, speciellt icke-steroida antiinflammatoriska läkemedel (NSAID) som acetylsalicylsyra eller ibuprofen
- Läkemedel som används för att lösa blodproppar (blodförtunnande)
- Läkemedel som blockerar upptag av vitamin K (så kallade vitamin K-antagonister)
- Läkemedel som reglerar blodkoaguleringen med hjälp av aktiverat protein C
- Antikoagulerande läkemedel med direktverkande faktor Xa och IIa hämmare.
Graviditet, amning och fertilitet
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du använder detta läkemedel.
Behandling av blodpropp hos gravida kvinnor kräver involvering av specialistläkare.
innohep kan användas under hela graviditeten om läkare bedömer att det är medicinskt motiverat. Tinzaparin passerar inte över till moderkakan.
innohep ska inte användas av gravida kvinnor med hjärtklaffsprotes.
Det är okänt om innohep utsöndras i modersmjölk. Rådgör med din läkare före användning av innohep under amning.
Det finns inga studier gjorda beträffande innoheps påverkan på fertiliteten.
Körförmåga och användning av maskiner
innohep har ingen eller försumbar effekt på förmågan att framföra fordon och använda maskiner.
innohep innehåller natriummetabisulfit och natrium
De förfyllda sprutorna innehåller natriummetabisulfit och natriumhydroxid.
Natriummetabisulfit: Kan i sällsynta fall ge överkänslighetsreaktioner och kramp i luftrören. Ska användas med försiktighet om du har astma.
Natrium: Detta läkemedel innehåller 40 mg natrium (huvudingrediensen i koksalt/bordssalt) per ml. Detta motsvarar 2 % av högsta rekommenderat dagligt intag av natrium för vuxna.
Hur produkten används
Använd alltid detta läkemedel enligt läkarens anvisningar. Rådfråga läkare om du är osäker.
Din läkare kommer att förskriva den rätta dosen för dig. Behandlingen kommer att ges en gång dagligen under minst 6 dagar och kan fortsätta i upp till 6 månader. Behovet av fortsatt behandling efter 6 månader kommer att utvärderas av din läkare.
Din läkare kommer informera dig om hur länge du ska behandlas med innohep.
Användarinstruktion:
innohep ska sprutas in under huden (subkutant) enligt läkarens anvisning. Spruta aldrig in läkemedlet i muskler eller blodkärl. Injektionen bör ges vid samma tidpunkt varje dag.
Om du själv ska ge injektionen, ska praktisk anvisning först ges av läkare eller sjuksköterska.
Alla innohep engångssprutor innehåller en luftbubbla som inte behöver pressas ut före injektion.
- Tvätta händerna innan du ska ge injektionen. Tvätta injektionsstället, t.ex. på buken, med sprit och låt det torka. Undvik att gnida eller gnugga.
2. Öppna plasttuben genom att vika upp fliken på tubens färgade lock helt och tag sedan ut sprutan. Inspektera sprutans innehåll före användning. Om injektionsvätskan är grumlig eller innehåller någon utfällning, ska du inte använda den utan ta en annan spruta. Injektionsvätskan kan gulna vid förvaring men kan fortfarande användas om den är klar.
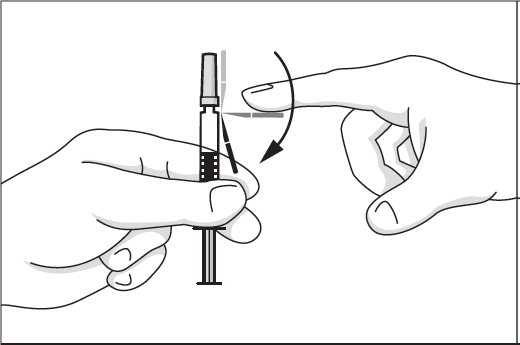
3. Böj ner säkerhetsanordningen bort från nålskyddet.
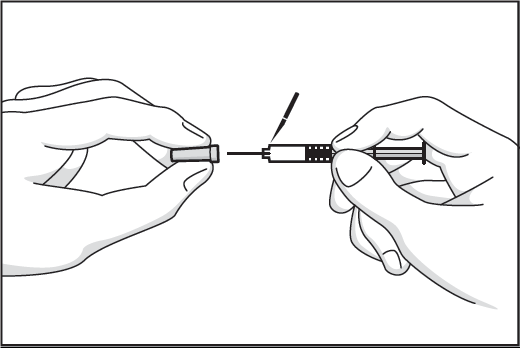
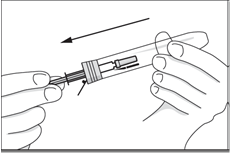
4. Avlägsna nålskyddet utan att böja nålen genom att fatta tag i dess upphöjda kant och vrida ett kvarts varv innan det försiktigt tas bort. Undvik att fatta tag på nålskyddets mjuka mittdel eller att dra av nålskyddet snabbt. Justera vid behov mängden i sprutan till den dos som din läkare har ordinerat. Överskjutande mängd avlägsnas genom att trycka sprutkolven i lodrät riktning. Dra inte tillbaka kolven och pressa inte ut luftbubblan. Om luftbubblan inte hamnar vid kolven, knacka lätt på sprutan tills luftbubblan hamnar på rätt plats.
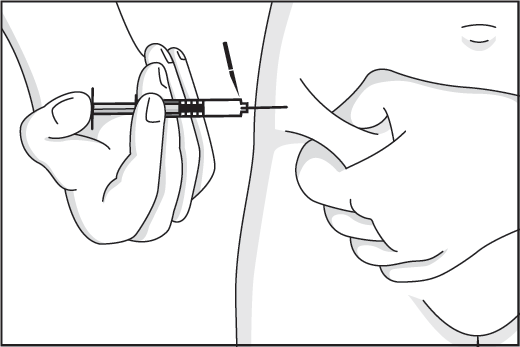
5. Lyft upp ett hudveck mellan tummen och pekfingret med ena handen och stick in nålen, vinkelrät mot huden, med den andra handen.
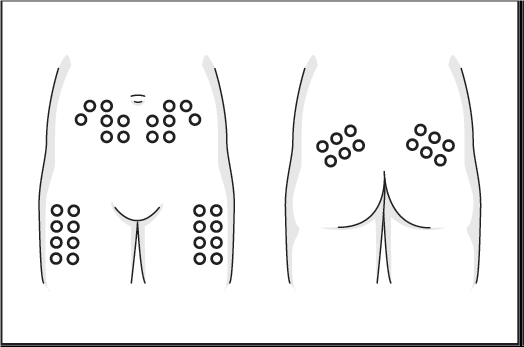
6. Spruta långsamt in ordinerad dos i underhudsfettet på buken. Drag ut nålen till hälften och räkna till 10. Drag sedan ut nålen helt.
Injicera inte närmare än 5 cm från naveln. Använd lårens utsidor, skinkorna eller överarmen om det inte går att injicera i buken.
7. Torka bort eventuellt blod med en kompress.
Välj ett annat injektionsställe nästa gång. Börja t.ex. på bukens högra sida och gå till vänster.
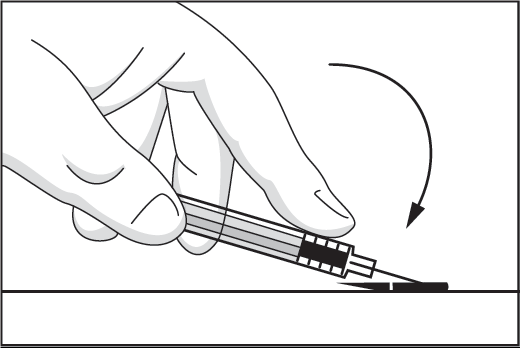
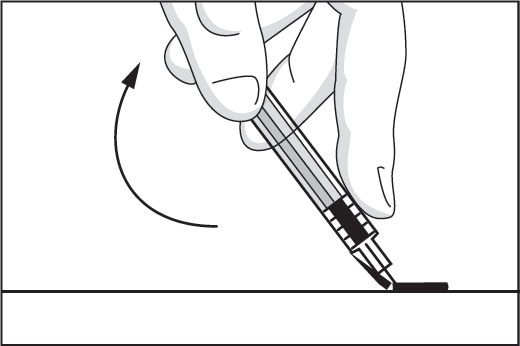
8. Böj tillbaka säkerhetsanordningen till den ursprungliga positionen så att den nu sitter under nålen. Lägg därefter säkerhetsanordningen platt mot ett hårt underlag och pressa tills nålen sitter fast i säkerhetsanordningen.
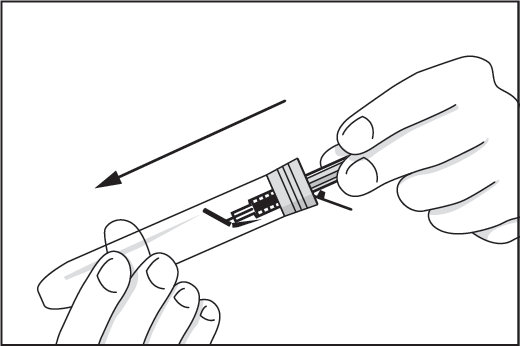
9. Du kan antingen lägga tillbaka den använda sprutan i plasttuben med nålspetsen nedåt eller i en behållare för använda kanyler.
Sprutan är nu säkert förvarad och plasttuben eller behållaren för använda kanyler kan lämnas till sjukhus eller apotek.
Om du har använt för stor mängd av innohep
Om du fått i dig för stor mängd läkemedel eller om t.ex. ett barn fått i sig läkemedlet av misstag kontakta läkare, sjukhus eller Giftinformationscentralen (tel. 112 i Sverige, 0800 147 111 i Finland) för bedömning av risken samt rådgivning.
Överdosering kan resultera i blödning.
Om du har glömt att använda innohep
Ta inte dubbel dos för att kompensera för glömd dos.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem.
Sluta att ta innohep och kontakta omedelbart läkare om du får någon av följande biverkningar:
- Angioödem (förekommer hos upp till 1 av 1000 användare). Symptom på angioödem är:
- svullnad av ansikte, tunga eller svalg
- svårighet att svälja
- nässelutslag och andningssvårigheter.
- En extremt kraftig allergisk reaktion med hudutslag vanligen i form av blåsor eller sår i munhåla och ögon samt andra slemhinnor exempelvis genitalier (förekommer hos upp till 1 av 1000 användare).
Andra biverkningar:
Vanliga (förekommer hos upp till 1 av 10 användare):
Reaktioner vid injektionsstället (smärta, klåda, svullnad, blåmärke). Blödning. Hudrodnad. Blodbrist.
Mindre vanliga (förekommer hos upp till 1 av 100 användare):
Ökat eller minskat antal blodplättar. Överkänslighet. Blåmärken. Rodnad. Övergående leverpåverkan. Utslag. Inflammation i huden. Klåda.
Sällsynta (förekommer hos upp till 1 av 1000 användare):
Allergiska reaktioner.
Nässelutslag, lokal vävnadsdöd. Benskörhet. Ökad kaliumhalt i blodet. Smärtsam kvarstående erektion.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Inga särskilda förvaringsanvisningar.
Används före utgångsdatum som anges på kartongen. Utgångsdatumet är den sista dagen i angiven månad.
Ska inte användas om injektionsvätskan är grumlig eller utfällning kan observeras. Injektionsvätskan kan färgas gul vid förvaring men är fortfarande användbar.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- Den aktiva substansen är tinzaparinnatrium. En ml innehåller 20000 anti-Xa IU/ml tinzaparinnatrium (motsvarande 240 mg tinzaparin). IU = IE (Internationella enheter).
- Övriga innehållsämnen är: Natriummetabisulfit (E 223), natriumhydroxid för pH-justering, vatten för injektionsvätskor.
Läkemedlets utseende och förpackningsstorlekar
innohep är en färglös/svagt gulaktig lösning.
Graderade förfyllda sprutor av glas med nålskyddsanordning av plast. Nålskydd av styrenbutadiengummi eller polyisoprene gummi:
8000 anti-Xa IU (0,4 ml): 6×1, 10×1, 30×1, 30 (3×10) st
10 000 anti-Xa IU (0,5 ml): 6×1, 10×1, 30×1, 30 (3×10) st
12 000 anti-Xa IU (0,6 ml): 6×1, 10×1, 30×1, 30 (3×10) st
14 000 anti-Xa IU (0,7 ml): 6×1, 10×1, 30×1, 30 (3×10) st
16 000 anti-Xa IU (0,8 ml): 6×1, 10×1, 30×1, 30 (3×10) st
18 000 anti-Xa IU (0,9 ml): 6×1, 10×1, 30×1, 30 (3×10) st
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning och tillverkare
Innehavare av godkännande för försäljning
LEO Pharma A/S Industriparken 55, DK-2750 Ballerup, Danmark.
Tillverkare
Laboratoires LEO, 39 Route de Chartres, 28500 Vernouillet, Frankrike
Finland: Ytterligare upplysningar om detta läkemedel kan erhållas hos ombudet för innehavaren av godkännandet för försäljning:
LEO Pharma Oy, Vanda, tel. 020 721 8440.
Denna bipacksedel ändrades senast
19.4.2022