OLIMEL N7E infuusioneste, emulsio
Olimel N7E infuusioneste, emulsio
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti, ennen kuin aloitat lääkkeen käyttämisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai sairaanhoitajan puoleen.
- Jos havaitset haittavaikutuksia, käänny lääkärin tai sairaanhoitajan puoleen. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
- Mitä Olimel N7E on ja mihin sitä käytetään
- Mitä sinun on tiedettävä, ennen kuin käytät Olimel N7E -valmistetta
- Miten Olimel N7E -valmistetta käytetään
- Mahdolliset haittavaikutukset
- Olimel N7E -valmisteen säilyttäminen
- Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Olimel N7E on infuusioneste, emulsio, joka on pakattu kolmiosastoiseen pussiin.
Kukin kammio sisältää kalsiumia sisältävää glukoosiliuosta, lipidiemulsiota ja muita elektrolyyttejä sisältävää aminohappoliuosta.
Olimel N7E infuusionestettä käytetään aikuisilla ja yli 2-vuotiailla lapsilla ravinnon antoon infuusioletkulla laskimoon, kun ravinnon anto suun kautta ei ole mahdollista.
Olimel N7E infuusionestettä on käytettävä lääkärin valvonnassa.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Olimel N7E -valmistetta ei saa käyttää:
- keskosille, vauvoille ja alle 2-vuotiaille lapsille.
- jos olet yliherkkä (allerginen) kananmunan, soijapavun, maapähkinän proteiinille tai maissille/maissituotteille (ks. myös kohta “Varoitukset ja varotoimet” alla) tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa).
- jos elimistösi aminohappoaineenvaihdunnassa on häiriöitä.
- jos veresi rasva-arvot ovat erityisen korkeat.
- jos sinulla on hyperglykemia (liian korkea verensokeri).
- jos sinulla on jonkin elektrolyytin (natrium, kalium, magnesium, kalsium ja/tai fosfori) epänormaalin korkea pitoisuus veressä.
Lääkäri tekee päätöksen siitä, voiko potilaalle antaa tätä lääkevalmistetta. Lääkärin päätös perustuu potilaan ikään, painoon ja terveydentilaan sekä mahdollisesti tehtyjen kokeiden tuloksiin.
Varoitukset ja varotoimet
Keskustele lääkärin tai sairaanhoitajan kanssa ennen kuin käytät Olimel N7E -valmistetta.
Täydellisen parenteraalisen ravitsemusliuoksen (TPN) liian nopea antaminen voi aiheuttaa vamman tai olla hengenvaarallista.
Infuusio on lopetettava välittömästi, jos potilaalla on allergisen reaktion löydöksiä tai oireita (kuten hikoilua, kuumetta, vilunväreitä, päänsärkyä, ihottumaa tai hengenahdistusta). Valmiste sisältää soijaöljyä ja kananmunan fosfolipidejä, jotka voivat aiheuttaa yliherkkyysreaktioita. Soijapapujen ja maapähkinöiden välillä on havaittu ristiallergiareaktioita.
Olimel N7E sisältää glukoosia, joka on peräisin maissista. Tämä voi aiheuttaa yliherkkyysreaktioita, jos olet allerginen maissille tai maissituotteille (ks. kohta “Olimel N7E -valmistetta ei saa käyttää” yllä).
Hengitysvaikeudet voivat myös olla merkki siitä, että on muodostunut pieniä hiukkasia, jotka tukkivat keuhkojen verisuonia (saostumia keuhkoverisuonissa). Jos sinulle ilmaantuu hengitysvaikeuksia, kerro tästä lääkärille tai sairaanhoitajalle. He päättävät mahdollisista hoitotoimenpiteistä.
Keftriaksoni-nimistä antibioottia ei saa sekoittaa tai antaa samanaikaisesti infuusiona laskimoon minkään kalsiumia sisältävän liuoksen, mukaan lukien Olimel N7E, kanssa. Näitä lääkkeitä ei pidä antaa sinulle yhdessä edes eri infuusioletkuja pitkin tai eri infuusiokohtiin.
Sinulle voidaan kuitenkin antaa Olimel N7E -valmistetta ja keftriaksonia peräkkäin, jos käytetään eri paikoissa olevia infuusioletkuja tai jos infuusioletkut vaihdetaan tai huuhdellaan huolellisesti fysiologisella suolaliuoksella infuusioiden välissä saostumien (keftriaksonin kalsiumsuolan partikkeleiden muodostuminen) välttämiseksi.
Tietyt lääkkeet ja sairaudet voivat suurentaa infektion tai verenmyrkytyksen riskiä. Erityinen infektio- tai verenmyrkytysvaara on olemassa, kun laskimoon asetetaan putki (laskimokatetri). Lääkäri tarkkailee sinua huolellisesti infektioon viittaavien oireiden varalta. Parenteraalisesti (suonensisäisesti) annettua ravitsemushoitoa tarvitsevilla potilailla on suurempi riski saada infektio johtuen heidän perustilastaan. Infektiotartunnan vaaraa voidaan vähentää käyttämällä ns. aseptista (mikrobitonta) tekniikkaa katetrin asettamisessa ja hoidossa sekä ravintovalmisteiden valmistelussa.
Jos sinulla on vakava aliravitsemus, niin että tarvitset laskimoon annettavaa ravintoliuosta, parenteraalisen ravinnon anto tulee aloittaa hitaasti. Lääkäri seuraa tarkasti potilaan tilaa estääkseen äkilliset neste-, vitamiini-, elektrolyytti- ja hivenainemäärien muutokset.
Ennen infuusion aloittamista hoidetaan elimistön neste- ja suolatasapaino- sekä aineenvaihduntahäiriöt. Lääkäri valvoo potilaan tilaa lääkevalmisteen antamisen aikana ja voi muuttaa annostusta tai antaa tarvittaessa ravintolisiä, kuten vitamiineja, elektrolyyttejä ja hivenaineita.
Maksan toimintahäiriöitä kuten sappihapon poistumisen vaikeuksia (kolestaasi), maksan rasvoittumista, maksafibroosia, jotka voivat aiheuttaa maksan vajaatoimintaa, sekä sappirakkotulehdusta ja sappikivitautia on raportoitu potilailla, jotka ovat saaneet laskimoon annettavaa ravintoliuosta. Näiden häiriöiden syy voi johtua monista tekijöistä ja ne voivat vaihdella potilaiden välillä. Ota yhteys lääkäriin, jos sinulla ilmenee pahoinvointia, oksentelua, vatsakipua ja ihon tai silmien keltaisuutta, jotta voidaan selvittää oireiden mahdolliset syyt ja niihin vaikuttavat seikat, ja mahdollinen hoito tai profylaksia voidaan aloittaa.
Lääkärille on kerrottava seuraavista tiloista:
- vaikea munuaisongelma; lääkärille on kerrottava myös dialyysihoidosta (keinomunuaishoito) tai muun tyyppisestä verenpuhdistushoidosta
- vaikea maksaongelma
- veren hyytymishäiriöitä
- lisämunuaisten vajaatoiminta (adrenaliininpuutos); lisämunuaiset ovat kolmionmuotoisia rauhasia munuaisten yläosassa
- sydämen vajaatoiminta
- keuhkosairaus
- nesteen kertyminen elimistöön (hyperhydraatio)
- elimistön nestehukka
- hoitamaton korkea verensokeri (diabetes mellitus)
- sydänkohtaus tai sokki äkillisen sydämen vajaatoiminnan takia
- vaikea metabolinen asidoosi (jossa veri on liian hapanta)
- yleinen infektio (verenmyrkytys)
- kooma.
Lääkevalmisteen tehon ja turvallisuuden tarkistamiseksi potilaalle tehdään kliinisiä kokeita ja laboratoriokokeita lääkevalmisteen antamisen aikana. Jos lääkevalmistetta käytetään useiden viikkojen ajan, säännölliset verikokeet ovat tarpeen.
Elimistön heikentynyt kyky poistaa tämän valmisteen sisältämiä rasvoja voi johtaa rasvakuormitukseksi kutsuttuun oireyhtymään (ks. kohta Mahdolliset haittavaikutukset – Mahdolliset haittavaikutukset).
Jos havaitset infuusion aikana kipua, polttelua tai turvotusta infuusiokohdassa tai infuusion vuotamista, kerro lääkärille tai sairaanhoitajalle. Lääkkeen anto lopetetaan välittömästi ja aloitetaan uudelleen toiseen laskimoon.
Jos verensokerisi nousee liikaa, lääkärisi muuttaa valmisteen antonopeutta tai antaa lääkettä verensokerin säätelyyn (insuliini).
Olimel N7E infuusionestettä voidaan annostella vain letkun (katetri) kautta rinnan suureen laskimoon (keskuslaskimo).
Lapset ja nuoret
Jos lapsi on alle 18-vuotias, oikea annostus valitaan erityisen huolellisesti. Erityistä huolellisuutta noudatetaan myös siksi, että lapsilla on suurempi infektiotartunnan vaara. Infuusioon on aina lisättävä vitamiineja ja hivenaineita sekä käytettävä lapsille tarkoitettuja koostumuksia.
Muut lääkevalmisteet ja Olimel N7E
Kerro lääkärille jos parhaillaan käytät tai olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä.
Yleensä muiden lääkkeiden samanaikainen otto ei aiheuta ongelmia. Kerro lääkärillesi, jos parhaillaan käytät tai olet äskettäin käyttänyt muita lääkkeitä, myös lääkkeitä, joita lääkäri ei ole määrännyt.
Kerro lääkärille jos parhaillaan käytät tai saat jotakin seuraavista lääkkeistä:
- Insuliini
- Hepariini.
Olimel N7E infuusionestettä ei saa annostella samanaikaisesti veren kanssa samalla välineistöllä.
Olimel N7E sisältää kalsiumia. Sitä ei saa antaa yhdessä tai samaa infuusioletkuja pitkin keftriaksoni-nimisen antibiootin kanssa, koska se voi aiheuttaa hiukkasten muodostumista. Jos sinulle annetaan näitä lääkkeitä samalla välineistöllä, pitää se huuhdella huolellisesti.
Valmisteessa oleva oliivi- ja soijaöljy sisältävät K-vitamiinia. Tämä ei normaalisti vaikuta verenohennuslääkkeisiin (hyytymisenestolääkkeisiin) kuten kumariiniin. Sinun pitää kuitenkin kertoa lääkärille, jos käytät hyytymisenestolääkitystä.
Saostumisriskin vuoksi Olimel N7E -valmistetta ei saa antaa saman infuusiolinjan kautta tai sekoittaa yhdessä ampisilliinin (antibiootti) tai fosfenytoiinin (epilepsialääke) kanssa.
Emulsion sisältämät lipidit voivat vääristää joitakin laboratoriokokeiden tuloksia, jos verinäyte on otettu ennen kuin rasvat ovat poistuneet verenkierrostasi (yleensä rasvat ovat poistuneet elimistöstä 5–6 tunnin kuluttua niiden annosta).
Olimel N7E sisältää kaliumia. Diureettilääkitystä, ACE:n estäjiä, angiotensiini II ‑reseptorin antagonisteja (verenpainelääkkeitä) tai immunosuppressiolääkitystä saaville potilaille valmistetta on annettava varoen. Tämän tyyppiset lääkkeet voivat suurentaa veren kaliumpitoisuutta.
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä neuvoa ennen kuin sinulle annettaan tätä lääkettä.
Ei ole olemassa riittäviä tietoja Olimel N7E -valmisteen käytöstä raskaana olevilla tai imettävillä naisilla. Olimel N7E -valmisteen käyttöä voidaan tarvittaessa harkita raskauden ja imetyksen aikana. Olimel N7E -valmistetta tulee käyttää raskauden aikana tai imettävillä naisilla vasta huolellisen harkinnan jälkeen.
Ajaminen ja koneiden käyttö
Ei merkityksellinen.
Miten valmistetta käytetään
Annostus
Olimel N7E -valmistetta saa antaa vain aikuisille ja yli 2-vuotiaille lapsille.
Valmiste on infuusioneste, emulsio, joka annetaan letkulla (katetri) rinnan laskimoon.
Olimel N7E -valmistetta tulee olla annettaessa huoneenlämpöistä.
Vain kerta-antoon.
Yhden pussin infuusio kestää tavallisesti 12–24 tuntia.
Aikuisten annostus
Lääkäri määrittää infuusionopeuden tarpeittesi ja vointisi mukaan.
Hoitoa voidaan jatkaa niin kauan kuin tarvitaan riippuen voinnistasi.
Yli 2-vuotiaiden lasten ja nuorten annostus
Lääkäri päättää lääkevalmisteen annoksen ja hoidon keston. Tämä riippuu iästä, painosta, pituudesta, potilaan voinnista sekä elimistön kyvystä hajottaa ja käyttää Olimel N7E -valmisteessa olevia ainesosia.
Jos saat enemmän Olimel N7E -valmistetta kuin sinun pitäisi
Jos annos tai infuusionopeus on liian suuri, valmisteen sisältämät aminohapot voivat happamoittaa verta liikaa ja hypervolemian (kiertävän verimäärän kasvu) oireita voi esiintyä. Glukoosi voi nostaa veren ja virtsan glukoosipitoisuutta, hyperosmolarisuutta (liian paksu veri) voi esiintyä ja lipidit voivat nostaa veren triglyseridipitoisuutta. Liian nopean infuusion tai liian suuren valmistemäärän saaminen voi aiheuttaa pahoinvointia, oksentelua, vilunväristyksiä, päänsärkyä, kuumia aaltoja, liiallista hikoilua (hyperhidroosi) ja elektrolyyttitasapainohäiriöitä. Tällöin infuusio on lopetettava välittömästi.
Joissakin vaikeissa tapauksissa lääkäri voi määrätä potilaan väliaikaiseen munuaisdialyysiin auttaakseen munuaisia poistamaan liian valmisteen.
Lääkäri valvoo tilaasi ja testaa veriarvot säännöllisesti, jotta nämä oireet vältettäisiin.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin puoleen.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Kerro heti lääkärille tai hoitajalle, jos vointisi muuttuu hoidon aikana tai sen jälkeen.
Lääkärin määräämät kokeet lääkevalmisteen käytön aikana pienentävät haittavaikutusten vaaraa.
Infuusio on lopetettava välittömästi, jos ilmenee poikkeavuuksia tai allergisen reaktion löydöksiä tai oireita kuten hikoilua, kuumetta, vilunväreitä, päänsärkyä, ihottumaa tai hengenahdistusta.
Seuraavia haittavaikutuksia on raportoitu valmisteen käytön yhteydessä:
Yleiset haittavaikutukset (voi vaikuttaa enintään 1 käyttäjään 10:stä)
- Nopea syke (takykardia)
- Vähentynyt ruokahalu
- Suurentunut rasvapitoisuus veressä (hypertriglyseridemia)
- Vatsakipu
- Ripuli
- Pahoinvointi
- Kohonnut verenpaine (hypertensio).
Esiintymistiheys tuntematon (saatavissa oleva tieto ei riitä arviointiin)
- Yliherkkyysreaktiot mukaan lukien hikoilu, kuume, vilunväristykset, päänsärky, ihottuma (punoittava, näppyläinen, märkärakkulainen, täplikäs, laajalle levittynyt ihottuma), kutina, kuumat aallot, hengitysvaikeudet
- Infuusion vuotaminen ympäröivään kudokseen (ekstravasaatio), joka voi aiheuttaa infuusiokohdan kipua, ärsytystä, turvotusta, punoitusta/lämmön tunnetta, kudossolujen kuolemaa (ihonekroosi) tai rakkuloita/vesikkelien muodostumista, tulehduksia, ihon kovettumista tai kireyttä
- Oksentelu.
Seuraavia haittavaikutuksia on raportoitu samanlaisten parenteraalisten ravintovalmisteiden käytön yhteydessä:
Hyvin harvinaiset haittavaikutukset (voi vaikuttaa enintään 1 käyttäjään 10 000:sta)
- Heikentynyt kyky poistaa rasvoja (rasvakuormitusoireyhtymä), johon liittyy äkillinen potilaan terveydentilan heikkeneminen. Seuraavat rasvakuormitusoireyhtymän oireet häviävät yleensä, kun lipidiemulsio lopetetaan:
Kuume
- Punasolujen määrän väheneminen (anemia), joka voi aiheuttaa kalpeutta ja heikkoutta tai hengitysvaikeuksia
- Valkosolujen määrän väheneminen (leukopenia), joka voi suurentaa infektio-riskiä
- Verihiutaleiden niukkuus (trombosytopenia), joka voi suurentaa mustelmien ja/tai verenvuodon riskiä
- Hyytymishäiriöt, jotka vaikuttavat veren hyytymiseen
- Veren korkeat rasva-arvot (hyperlipidemia)
- Rasvan kertyminen maksaan (hepatomegalia)
- Maksan toiminnan heikentyminen
- Keskushermosto-oireet (esim. kooma).
Esiintymistiheys tuntematon (saatavissa oleva tieto ei riitä arviointiin)
- Allergiset reaktiot
- Maksan toimintaverikokeen epänormaalit tulokset
- Sappihapon poistamisen vaikeudet (kolestaasi)
- Maksan koon suureneminen (hepatomegalia)
- Parenteraaliseen (suonensisäiseen) ravinnonantoon liittyvä maksasairaus (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä “Varoitukset ja varotoimet”)
- Keltatauti (ikterus)
- Verihiutaleiden määrän väheneminen (trombosytopenia)
- Lisääntynyt typen määrä veressä (atsotemia)
- Kohonneet maksaentsyymitasot
- Pienten keuhkoverisuonia tukkivien hiukkasten (keuhkoverenkierron saostumat) muodostuminen, mikä johtaa keuhkoverisuonen veritulppaan ja hengitysvaikeuksiin.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai sairaanhoitajalle. Tämä koskee myös kaikkia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä pakkauksessa ja ulkopakkauksessa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Ei saa jäätyä.
Säilytettävä päällyspussissa.
Lääkkeitä ei tule heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä Olimel N7E -valmiste sisältää
Sekoitetun emulsion kunkin pussin vaikuttavat aineet: L-aminohappoliuos 11,1 g/100 ml (alaniini, arginiini, glysiini, histidiini, isoleusiini, leusiini, lysiini (lysiiniasetaattina), metioniini, fenyylialaniini, proliini, seriini, treoniini, tryptofaani, tyrosiini, valiini, asparagiinihappo, glutamiinihappo) ja elektrolyytit (natrium, kalium, magnesium, fosfaatti, asetaatti, kloridi), lipidiemulsio 20 g/100 ml (puhdistettu oliiviöljy ja puhdistettu soijaöljy) ja glukoosiliuos 35 g/100 ml (glukoosimonohydraattina) ja kalsium.
Muut aineet:
| Lipidiemulsio-osasto | Aminohappoliuos-osasto | Glukoosiliuos-osasto |
Puhdistetut kananmunan fosfolipidit, glyseroli, natriumoleaatti, natriumhydroksidi (pH:n säätöön), injektionesteisiin käytettävä vesi | Väkevä etikkahappo (pH:n säätöön), injektionesteisiin käytettävä vesi | Kloorivetyhappo (pH:n säätöön), injektionesteisiin käytettävä vesi |
Valmisteen kuvaus ja pakkauskoot
Olimel N7E on kolmikammiopussiin pakattu infuusioneste, emulsio. Yksi osasto sisältää lipidiemulsion, toinen aminohappoliuoksen ja elektrolyytit ja kolmas glukoosiliuoksen ja kalsiumin. Osastot on erotettu toisistaan avautuvilla saumoilla. Osastojen sisältö sekoitetaan ennen annostelua rullaamalla pussia yläosasta alaspäin, kunnes saumat ovat avautuneet.
Ulkonäkö ennen sekoittamista:
- Aminohappo- ja glukoosiliuokset ovat kirkkaita, värittömiä tai kellertäviä.
- Lipidiemulsio on homogeeninen, maitomainen.
Ulkonäkö sekoittamisen jälkeen: homogeeninen, maitomainen emulsio.
Kolmiosastoinen pussi on monikerroksinen muovipussi. Pussin sisäkerroksen materiaali on yhteensopiva lääkevalmisteen aineiden ja hyväksyttyjen lisäyksien kanssa.
Jotta ilman happea ei pääse valmisteeseen, pussi on pakattu happitiiviiseen päällyspussiin, jossa on happea imevä tyyny.
Pakkauskoot
1000 ml:n pussi: 1 laatikko, jossa on 6 pussia
1500 ml:n pussi: 1 laatikko, jossa on 4 pussia, 1 laatikko, jossa on 5 pussia
2000 ml:n pussi: 1 laatikko, jossa on 4 pussia, 1 laatikko, jossa on 5 pussia
1 pussi, jossa 1000 ml, 1500 ml tai 2000 ml.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija
Baxter Oy
PL 35
01531 Vantaa
Valmistaja
Baxter S.A.
Boulevard René Branquart, 80
7860 Lessines
Belgia
Tämä pakkausseloste on tarkistettu viimeksi 01.10.2025
Ohjeet terveydenhuollon ammattilaiselle
1000 ml |
1500 ml |
2000 ml |
|
35 % glukoosiliuos (vastaten 35 g/100 ml) |
400 ml |
600 ml |
800 ml |
11,1 % aminohappoliuos (vastaten 11,1 g/100 ml) |
400 ml |
600 ml |
800 ml |
20 % lipidiemulsio (vastaten 20 g/100 ml) |
200 ml |
300 ml |
400 ml |
Kunkin pussikoon sekoitetun emulsion koostumus, kun kolmen osaston sisältö on sekoitettu:
Vaikuttavat aineet |
1000 ml |
1500 ml |
2000 ml |
Puhdistettu oliiviöljy + puhdistettu soijaöljya |
40,00 g |
60,00 g |
80,00 g |
Alaniini |
6,41 g |
9,61 g |
12,82 g |
Arginiini |
4,34 g |
6,51 g |
8,68 g |
Asparagiinihappo |
1,28 g |
1,92 g |
2,56 g |
Glutamiinihappo |
2,21 g |
3,32 g |
4,42 g |
Glysiini |
3,07 g |
4,60 g |
6,14 g |
Histidiini |
2,64 g |
3,97 g |
5,29 g |
Isoleusiini |
2,21 g |
3,32 g |
4,42 g |
Leusiini |
3,07 g |
4,60 g |
6,14 g |
Lysiini (lysiininasetaattina) |
3,48 g (4,88 g) |
5,23 g (7,31 g) |
6,97 g (9,75 g) |
Metioniini |
2,21 g |
3,32 g |
4,42 g |
Fenyylialaniini |
3,07 g |
4,60 g |
6,14 g |
Proliini |
2,64 g |
3,97 g |
5,29 g |
Seriini |
1,75 g |
2,62 g |
3,50 g |
Treoniini |
2,21 g |
3,32 g |
4,42 g |
Tryptofaani |
0,74 g |
1,10 g |
1,47 g |
Tyrosiini |
0,11 g |
0,17 g |
0,22 g |
Valiini |
2,83 g |
4,25 g |
5,66 g |
Natriumasetaattitrihydraatti |
1,50 g |
2,24 g |
2,99 g |
Natriumglyserofosfaatti, hydratoitu |
3,67 g |
5,51 g |
7,34 g |
Kaliumkloridi |
2,24 g |
3,35 g |
4,47 g |
Magnesiumkloridiheksahydraatti |
0,81 g |
1,22 g |
1,62 g |
Kalsiumklorididihydraatti |
0,52 g |
0,77 g |
1,03 g |
Glukoosi (glukoosimonohydraattina) |
140,00 g (154,00 g) |
210,00 g (231,00 g) |
280,00 g (308,00 g) |
a Puhdistetun oliiviöljyn (noin 80 %) ja puhdistetun soijaöljyn (noin 20 %) sekoitus, jolloin välttämättömien rasvahappojen osuus kaikista rasvahapoista on 20 %.
Apuaineet ovat:Lipidiemulsio-osasto |
Aminohappoliuososasto sisältäen elektrolyyttejä |
Glukoosiliuos sisältäen kalsiumia |
Puhdistetut kananmunan fosfolipidit, glyseroli, natriumoleaatti, natriumhydroksidi (pH:n säätöön), injektionesteisiin käytettävä vesi |
Väkevä etikkahappo (pH:n säätöön), injektionesteisiin käytettävä vesi |
Kloorivetyhappo (pH:n säätöön), injektionesteisiin käytettävä vesi |
Sekoitetun emulsion ravintosisältö kussakin pussikoossa:
1000 ml |
1500 ml |
2000 ml |
|
Lipidit |
40 g |
60 g |
80 g |
Aminohapot |
44,3 g |
66,4 g |
88,6 g |
Typpi |
7,0 g |
10,5 g |
14,0 g |
Glukoosi |
140,0 g |
210,0 g |
280,0 g |
Energia: |
|||
Kokonaiskalorit noin |
1140 kcal |
1710 kcal |
2270 kcal |
Proteiinittomat kalorit |
960 kcal |
1440 kcal |
1920 kcal |
Glukoosikalorit |
560 kcal |
840 kcal |
1120 kcal |
Lipidikalorita |
400 kcal |
600 kcal |
800 kcal |
Proteiinittomien kalorien kalori-typpisuhde |
137 kcal/g |
137 kcal/g |
137 kcal/g |
Glukoosi-/lipidikalorien suhde |
58/42 |
58/42 |
58/42 |
Lipidikaloreiden osuus kokonaiskaloreista |
35 % |
35 % |
35 % |
Elektrolyytit: |
|||
Natrium |
35,0 mmol |
52,5 mmol |
70,0 mmol |
Kalium |
30,0 mmol |
45,0 mmol |
60,0 mmol |
Magnesium |
4,0 mmol |
6,0 mmol |
8,0 mmol |
Kalsium |
3,5 mmol |
5,3 mmol |
7,0 mmol |
Fosfaattib |
15,0 mmol |
22,5 mmol |
30,0 mmol |
Asetaatti |
45 mmol |
67 mmol |
89 mmol |
Kloridi |
45 mmol |
68 mmol |
90 mmol |
pH |
6,4 |
6,4 |
6,4 |
Osmolaarisuus |
1360 mOsm/l |
1360 mOsm/l |
1360 mOsm/l |
a Sisältää puhdistetun kananmunan fosfolipidien kalorit.
b Sisältää lipidiemulsion fosfaatin.
B. ANNOSTUS JA ANTOTAPA AnnostusOlimel N7E -valmisteen käyttöä alle 2-vuotiaille lapsille ei suositella sopimattoman koostumuksen ja pussien tilavuuden vuoksi (ks. valmisteyhteenvedon kohdat 4.4, 5.1 ja 5.2).
Alla mainittua suurinta vuorokausiannosta ei saa ylittää. Moniosastoisen pussin valmiin koostumuksen takia ei ole mahdollista tyydyttää samanaikaisesti kaikkia potilaan ravintoainetarpeita. Joissakin kliinisissä tilanteissa potilas voi tarvita muita kuin valmiin pussin sisältämiä ravintoainemääriä. Tällöin tilavuuden (annoksen) muuttamisessa on otettava huomioon tästä aiheutuvat vaikutukset kaikkiin muihin Olimel N7E -valmisteen ravintoainekomponenttien annoksiin.
Aikuiset
Annos valitaan potilaan energiankulutuksen, sairaudentilan ja painon mukaan. Lisäksi otetaan huomioon potilaan kyky metaboloida Olimel N7E -valmisteen aineosia sekä oraalisesti tai enteraalisesti annettua lisäenergiaa tai -proteiinia. Siksi pussin koko on valittava tarpeen mukaisesti.
Keskimääräinen ravinnontarve vuorokaudessa:
- 0,16–0,35 g typpeä/kg (1–2 g aminohappoja/kg) potilaan ravitsemustilan ja katabolian mukaan
- 20–40 kcal/kg
- 20–40 ml nestettä/kg tai 1–1,5 ml kulutettua kilokaloria (kcal) kohden.
Olimel N7E -valmisteen suurin vuorokausiannos perustuu kalorimäärään 40 kcal tilavuudessa 35 ml/kg, joka vastaa 1,5 g aminohappoja, 4,9 g glukoosia, 1,4 g lipidejä, 1,2 mmol natriumia ja 1,1 mmol kaliumia painokiloa kohden. 70 kg painavalla potilaalla tämä vastaa 2450 millilitraa Olimel N7E -valmistetta vuorokaudessa, jolloin saanti on 108 g aminohappoja, 343 g glukoosia ja 98 g lipidejä (eli noin 2352 kcal proteiinittomia kaloreita ja 2793 kcal kokonaiskaloreita).
Tavallisesti infuusionopeutta nostetaan vähitellen ensimmäisen tunnin aikana, minkä jälkeen antonopeus määrätään annoksen suuruuden, vuorokautisen nestemäärän ja infuusion keston mukaan.
Olimel N7E -valmisteen suurin infuusionopeus on 1,7 ml/kg tunnissa eli 0,08 g aminohappoja, 0,24 g glukoosia ja 0,07 g lipidejä kiloa kohden tunnissa.
Yli 2-vuotiaat lapset ja nuoret
Valmistetta ei ole tutkittu lapsilla.
Annos valitaan potilaan energiankulutuksen ja sairaudentilan mukaan. Lisäksi otetaan huomioon potilaan kyky metaboloida Olimel N7E -valmisteen aineosia sekä oraalisesti tai enteraalisesti annettua lisäenergiaa tai -proteiinia. Siksi pussin koko on valittava tarpeen mukaisesti.
Lisäksi päivittäinen neste- typpi- ja energiantarve pienenevät iän mukaan. tarkastelussa on otettu huomioon kaksi ryhmää, 2–11-vuotiaat ja 12–18-vuotiaat.
Olimel N7E -valmisteen antoa molemmissa ikäryhmissä rajoittaa vuorokausiannoksessa magnesiumpitoisuus ja infuusionopeudessa glukoosipitoisuus tunnissa. Kun rajoitukset otetaan huomioon, saadaan seuraavat annokset:
Aineosa |
2–11-vuotiaat |
12–18-vuotiaat |
||
Suositusa |
Enimmäisannos Olimel N7E -valmistetta |
Suositusa |
Enimmäisannos Olimel N7E -valmistetta |
|
Enimmäisvuorokausiannos (vrk) |
||||
Nestemäärä (ml/kg/vrk) |
60 – 120 |
25 |
50 – 80 |
25 |
Aminohapot (g/kg/vrk) |
1 – 2 (-2,5) |
1,1 |
1 – 2 |
1,1 |
Glukoosi (g/kg/vrk) |
1,4 – 8,6 |
3,5 |
0,7 – 5,8 |
3,5 |
Lipidit (g/kg/vrk) |
0,5 – 3 |
1,0 |
0,5 – 2 (-3) |
1,0 |
Kokonaisenergia (kcal/kg/vrk) |
30 – 75 |
28,5 |
20 – 55 |
28,5 |
Suurin infuusionopeus tunnissa (h) |
||||
Olimel N7E (ml/kg/h) |
2,6 |
1,7 |
||
Aminohapot (g/kg/h) |
0,20 |
0,11 |
0,12 |
0,08 |
Glukoosi (g/kg/h) |
0,36 |
0,36 |
0,24 |
0,24 |
Lipidit (g/kg/h) |
0,13 |
0,10 |
0,13 |
0,07 |
a Suositusarvot 2018 ESPGHAN/ESPEN/ESPR suosituksista
Tavallisesti infuusionopeutta suurennetaan vähitellen ensimmäisen tunnin aikana, minkä jälkeen se säädetään sopivaksi ottaen huomioon annoksen suuruus, vuorokautinen nestemäärä ja infuusion kesto.
Tavallisesti pienten lasten infuusio aloitetaan pienellä päivittäisellä annoksella, minkä jälkeen annosta suurennetaan vähitellen enimmäisannokseen (annettu yllä).
Antotapa ja hoidon kesto
Vain kerta-antoon.
Pussin avaamisen jälkeen on suositeltavaa, että sisältö käytetään heti ja liuosta ei saa säilyttää myöhempää käyttöä varten.
Yhdistämisen jälkeen seos on homogeeninen ja maitomainen.
Infuusionesteen, emulsion sekoitus- ja käyttöohjeet, ks. valmisteyhteenvedon kohta 6.6.
Korkean osmolaarisuuden vuoksi Olimel N7E -valmistetta voidaan antaa vain keskuslaskimoon.
Parenteraalisen ravintoliuosinfuusion suositeltu kesto on 12–24 tuntia.
Parenteraalisen ravinnon antoa voidaan jatkaa niin kauan kuin potilaan sairaudentila sitä edellyttää.
C. YHTEENSOPIMATTOMUUDETMuita lääkkeitä tai muita aineita ei saa lisätä mihinkään pussin kolmesta osastosta eikä sekoitettuun emulsioon, ennen kuin on varmistettu niiden yhteensopivuus ja sekoitetun valmisteen (erityisesti lipidiemulsion) stabiilius.
Yhteensopimattomuutta voi aiheuttaa esimerkiksi liiallinen happamuus (alhainen pH) tai kaksiarvoisten kationien (Ca2+ ja Mg2+) sopimaton pitoisuus, joka saattaa häiritä lipidiemulsion tasapainoa. Kuten kaikkien parenteraalisten ravintosekoituksien kohdalla, kalsium- ja fosfaattisuhde täytyy huomioida. Liiallinen kalsiumin ja fosfaatin lisääminen erityisesti mineraalisuolojen muodossa voi johtaa kalsiumfosfaattisaostumien muodostumiseen.
Olimel N7E sisältää kalsiumioneja, jotka lisäävät hyytymisriskiä, jos veren/verikomponenttien antikoagulaatiossa/säilytyksessä on käytetty sitraattia.
Keftriaksonia ei saa sekoittaa tai antaa samanaikaisesti laskimonsisäisten kalsiumia sisältävien liuosten kanssa, kuten Olimel N7E -valmisteen kanssa, samalla infuusioletkulla (esim. Y-liittimen kautta), koska siihen liittyy keftriaksonin kalsiumsuolan saostumisen vaara (ks. valmisteyhteenvedon kohdat 4.4 ja 4.5). Keftriaksonia ja kalsiumia sisältäviä liuoksia voidaan antaa peräkkäin tai eri infuusiokohtiin tai jos infuusioletkut vaihdetaan tai huuhdotaan huolellisesti fysiologisella suolaliuoksella infuusioiden välissä saostumien välttämiseksi.
Saostumisriskin vuoksi Olimel N7E -valmistetta ei saa antaa saman infuusiolinjan kautta tai sekoittaa yhdessä ampisilliinin tai fosfenytoiinin kanssa.
Tarkista samanaikaisesti saman katetrin tai kanyylin kautta annettavien liuosten yhteensopivuus.
Valmistetta ei saa antaa veren kanssa samanaikaisesti tai ennen veren antoa tai sen jälkeen samoilla välineillä kuin verta, koska silloin on olemassa pseudoagglutinaation vaara.
D. ERITYISET VAROTOIMET HÄVITTÄMISELLE JA MUUT KÄSITTELYOHJEETOhjeet Olimel N7E -valmisteen valmisteluvaiheista löytyy kuvasta 1.
Avaaminen
Poista päällyspussi.
Hävitä happea imevä tyyny.
Varmista, että pussi ja avautuvat saumat ovat ehjät. Käytä valmistetta vain, jos pussi ja osastojen väliset avautuvat saumat ovat vahingoittumattomia (kolmen osaston sisältö ei ole sekoittunut), aminohappo- ja glukoosiliuokset ovat kirkkaita, värittömiä tai hieman kellertäviä eikä niissä ole näkyviä hiukkasia ja lipidiemulsio on homogeeninen ja maitomainen.
Liuosten ja emulsion sekoittaminen
Varmista, että valmiste on huoneenlämpöinen, ennen kuin avaat osastojen väliset saumat.
Rullaa pussia käsin yläreunasta (ripustuspäästä) lähtien. Saumat avautuvat porttien puolelta. Jatka pussin rullaamista, kunnes saumat ovat auenneet puoliväliin.
Sekoita liuokset ja emulsio kääntämällä pussi ylösalaisin vähintään kolme kertaa.
Valmiste on sekoituksen jälkeen homogeeninen maitomainen emulsio.
Lisäykset
Pussiin voidaan lisätä esim. vitamiineja, elektrolyyttejä ja hivenaineita.
Aineet (myös vitamiinit) voidaan lisätä käyttövalmiiksi sekoitettuun valmisteeseen (kun osastojen väliset saumat on avattu ja kolmen osaston sisältö on sekoitettu).
Vitamiineja voidaan lisätä glukoosiliuososastoon myös ennen osastojen välisten saumojen avaamista ja liuosten ja emulsion sekoittamista. Tehtäessä lisäyksiä elektrolyyttejä sisältäviin koostumuksiin, valmisteessa oleva elektrolyyttimäärä tulee ottaa huomioon.
Aineet saa lisätä vain hoitohenkilökunta aseptisissa olosuhteissa.
Olimel N7E -valmisteeseen voidaan lisätä elektrolyyttejä seuraavan taulukon mukaisesti:
Per 1000 ml |
|||
Valmisteen pitoisuus |
Lisäys enintään |
Kokonaispitoisuus enintään |
|
Natrium |
35 mmol |
115 mmol |
150 mmol |
Kalium |
30 mmol |
120 mmol |
150 mmol |
Magnesium |
4,0 mmol |
1,6 mmol |
5,6 mmol |
Kalsium |
3,5 mmol |
1,5 (0,0a) mmol |
5,0 (3,5a) mmol |
Epäorgaaninen fosfaatti |
0 mmol |
3,0 mmol |
3,0 mmol |
Orgaaninen fosfaatti |
15 mmolb |
10 mmol |
25 mmolb |
a Arvo epäorgaanista fosfaattia lisättäessä.
b Sisältää lipidiemulsion fosfaatin.
Hivenaineet ja vitamiinit:
Valmisteen on osoitettu säilyvän stabiilina, jos siihen lisätään yleisiä vitamiini- ja hivenainevalmisteita (joissa on enintään 1 mg rautaa).
Tietoja muiden lisäysten yhteensopivuudesta on saatavissa pyydettäessä.
Lisää aineet seuraavasti:
- Huolehdi aseptisista olosuhteista.
- Valmistele pussin injektioportti.
- Lävistä injektioportti ja lisää lisättävät aineet injektioneulalla tai lääkkeenlisäysvälikappaleella.
- Sekoita pussin sisältö ja lisäykset.
Infuusion valmisteleminen
Huolehdi aseptisista olosuhteista.
Ripusta pussi.
Irrota annosteluportin muovisuojus.
Työnnä infuusioletkuston piikkiliitin tiiviisti annosteluporttiin.
Kuva 1: Valmisteluvaiheet Olimel N7E-valmisteen antamista varten
1. |
|
2. |
|
3. |
|
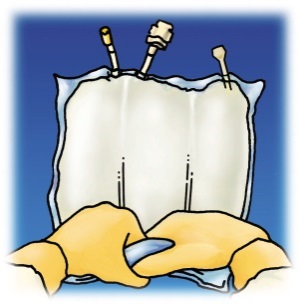
Avaa päällyspussi repäisemällä se auki yläosasta. |
Irrota päällyspussin etuosa ja ota Olimel N7E -pussi esiin. Hävitä päällyspussi ja happea imevä tyyny. |
Aseta pussi vaakasuoralle ja puhtaalle alustalle niin, että kahva on sinuun päin. |
|||
4. |
|
5. |
|
6. |
|
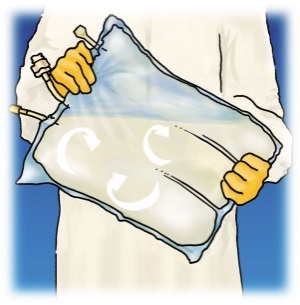
Nosta ripustuskohtaa, jotta liuos poistuu pussin yläosasta. Rullaa pussin yläosaa tiiviisti ylhäältä aloittaen, kunnes saumat ovat auenneet (noin puoliväliin). |
Sekoita sisältö kääntämällä pussi ylösalaisin vähintään kolme kertaa. |
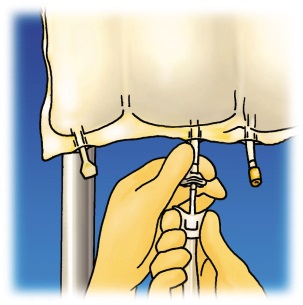
Ripusta pussi. Irrota annosteluportin muovisuojus. Kytke piikkiliitin tiiviisti. |
|||
Annostelu
Kerta-antoon.
Aloita valmisteen antaminen potilaalle vasta, kun kaikki avautuvat saumat osastojen välillä on avattu ja kolmen osaston sisältö on sekoittunut.
Varmista, että käyttövalmiissa infuusioemulsiossa ei näy faasien erottumista.
Pussin avaamisen jälkeen sen sisältö on käytettävä heti, eikä avattua pussia saa säilyttää myöhempää käyttöä varten. Osittain käytettyä pussia ei saa käyttää uudelleen.
Pusseja ei saa kytkeä sarjaan, koska ensimmäiseen pussiin mahdollisesti jäänyt kaasu voi aiheuttaa ilmaemboliavaaran.
Käyttämätön valmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Ekstravasaatio
Katetrin paikkaa tulee tarkkailla säännöllisesti ekstravasaation merkkien tunnistamiseksi. Jos ekstravasaatiota esiintyy, lääkkeen anto täytyy lopettaa välittömästi ja asetettu katetri tai kanyyli on pidettävä paikallaan potilaan välitöntä hoitoa varten. Mikäli mahdollista, aspirointi tulisi tehdä asetetun katetrin/kanyylin läpi ennen katetrin/kanyylin poistamista, jotta kudoksissa oleva neste vähenee.
Riippuen siitä mitä valmistetta ekstravasaatio on (mukaan lukien valmiste(et) joita on sekoitettu Olimel N7E -valmisteeseen) on ryhdyttävä asianmukaisiin toimenpiteisiin vaurion laajuuden mukaisesti. Hoitovaihtoehdot voivat olla ei farmakologisia, farmakologisia ja/tai kirurgisia. Mikäli kyseessä on laaja ekstravasaatio, plastiikkakirurgia tulisi konsultoida 72 tunnin sisällä.
Ekstravasaatiokohtaa tulisi tarkkailla vähintään neljän tunnin välein ensimmäisen 24 tunnin aikana ja sen jälkeen kerran päivässä.
Infuusiota ei saa aloittaa uudelleen samaan keskuslaskimoon.