PLENVU pulver till oral lösning
Tilläggsinformation
Makrogol 3350, natriumaskorbat, vattenfritt natriumsulfat, askorbinsyra, natriumklorid och kaliumklorid
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för dig.
Ta alltid detta läkemedel exakt enligt beskrivning i denna bipacksedel eller enligt anvisningar från din läkare eller apotekspersonal.
- Spara denna information, du kan behöva läsa den igen.
- Vänd dig till apotekspersonalen om du behøver mer information eller råd.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
- Du måste tala med läkare om du inte mår bättre eller om du mår sämre.
I denna bipacksedel finns information om följande
- Vad Plenvu är och vad det används för
- Vad du behöver veta innan du tar Plenvu
- Hur du tar Plenvu
- Eventuella biverkningar
- Hur Plenvu ska förvaras
- Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Plenvu innehåller en kombination av aktiva substanserna makrogol 3350, natriumaskorbat, vattenfritt natriumsulfat, askorbinsyra, natriumklorid och kaliumklorid.
Plenvu är ett laxermedel.
Plenvu är avsedd för 18 åriga och äldre vuxna inför en klinisk undersökning som kräver en ren tarm.
Plenvu renar din tarm genom att orsaka diarré åt dig.
Vad du behöver veta innan produkten används
Ta inte Plenvu:
- om du är allergisk mot aktiva substanser eller något annat innehållsämne i Plenvu (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
- om du har en blockering i din tarm (tarmobstruktion)
- om du har hål i din magsäcks- eller tarmvägg (tarmperforation)
- om du har tarmparalys (ileus)
- om du upplever problem med att tömma innehållet av mat och vätska från din mage (t.ex. gastropares, gastrisk retention)
- om du lider av fenylketonuri. Detta är en ärftlig oförmåga av kroppen att använda en specifik aminosyra. Plenvu innehåller en fenylalaninkälla
- om din kropp inte kan producera tillräckligt med glukos-6-fosfatdehydrogenas
- om du har en mycket utvidgad tarm (toxisk megakolon)
Varningar och försiktighet
Tala med läkare, apotekspersonal eller sjuksköterska innan du tar Plenvu om någon av nedanstående gäller dig. Om du:
- har hjärtproblem och/eller hjärtrytmstörningar
- har njurproblem och/eller dehydrering
- har hjärtsvikt, allvarliga njurproblem eller tar blodtrycksmedicin
- har mag- eller tarmproblem, inkluderat tarminflammation
- har problem med att svälja (se också Plenvu med mat och dryck)
- har hög eller låg salthalt i blodet ( t.ex. natrium, kalium)
- har andra medicinska tillstånd (t.ex. anfall)
- har epilepsi eller har haft krampanfall
Plenvu ska inte ges ges till patienter med sänkt medvetandegrad utan medicinsk övervakning.
Om du har ett dåligt hälsotillstånd eller allvarligt medicinskt tillstånd ska du vara speciellt medveten om eventuella biverkningar som anges i avsnitt Eventuella biverkningar. Tala med läkare, apotekspersonal eller sjuksköterska ifall du är orolig.
Om du upplever plötslig buksmärta eller ändtarmsblödning medan du tar Plenvu för tarmrengöring ska du omedelbart kontakta läkare eller uppsöka sjukvård.
Om du får (blod)kräkningar åtföljt av plötslig bröst-, nack- eller buksmärta, svårigheter att svälja eller andningssvårigheter när du tar Plenvu ska du sluta ta läkemedlet och omedelbart kontakta din läkare.
Barn och ungdomar
Plenvu rekommenderas inte för barn under 18 års ålder.
Andra läkemedel och Plenvu
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel (inkluderat orala preventivmedel).
Läkemedel som tas via munnen kan passera genom magtarmkanalen utan att eventuellt absorberas ordentligt då de tas 1 timme före, under eller 1 timme efter intag av Plenvu.
Ifall orala preventivmedel används kan du dessutom behöva annan form av preventivmedel (t.ex kondom) för att förhindra graviditet.
Plenvu med mat och dryck
Dagen före det kliniska ingreppet kan du äta en lätt frukost med därpå följande lätt lunch.
För Två dagars delade ELLER Dagen före doseringsschemat ska du avsluta ätande av lunch minst 3 timmar före du börjar ta Plenvu, efter detta får du bara konsumera klara vätskor.
För Endast morgon doseringensschemat kan du ta klar soppa och/eller enkel yoghurt till middag (som borde vara avklarad ungefär 20.00). Du får bara konsumera klara vätskor efter middag på kvällen före det kliniska ingreppet.
Märk: För information om doseringsscheman hänvisas till avsnitt Hur produkten används.
Ingen frukost är tillåten på morgonen före det kliniska ingreppet.
Fortsätt att dricka klara vätskor före, under och efter att du tagit Plenvu för att hjälpa förhindra vätskeförlust (dehydrering). Det är viktigt för dig att dricka i tillägg den mängden av klara vätskor som ordinerats.
Exempel på klara vätskor är vatten, klara soppor, örtte, svart te eller kaffe (utan mjölk), läskedrycker/utspädda saftkoncentrat och fruktjuicer (utan fruktkött).
Viktigt:
- Drick inte alkohol, mjölk, någonting färgat rött eller purpur (t.ex svartvinbärssaft) eller någon annan dryck som innehåller fruktkött.
- Ät inte när du tar Plenvu utan först efter ditt kliniska ingrepp.
Konsumeringen av all vätska ska avslutas senast:
- två timmar före det kliniska ingreppet när det görs i allmän anestesi, eller
- en timme före det kliniska ingreppet utan allmän anestesi
Om du behöver förtjocka vätskor för att kunna svälja dem säkert, kan Plenvu motverka effekten av förtjockningsmedlet.
Graviditet, amning och fertilitet
Det finns inga data från användning av Plenvu under graviditet eller amning, och är därmed inte rekommenderad. Det bör endast användas om läkaren bedömer att detta är nödvändigt. Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du använder detta läkemedel.
Körförmåga och användning av maskiner
Plenvu påverkar inte förmågan att köra bil eller hantera maskiner.
Plenvu innehåller natrium, kalium och en fenylalaninkälla
Detta läkemedel innehåller 458,5 mmol (10,5 g) natrium per behandling. Detta bör beaktas av patienter som står på en kost med kontrollerat natriumintag.
Detta läkemedel innehåller 29,4 mmol (1,1 g) kalium per behandling. Detta bör beaktas av patienter med nedsatt njurfunktion eller patienter som står på en kost med kontrollerat kaliumintag.
Plenvu innehåller en fenylalaninkälla som kan vara skadligt för personer med fenylketonuri. Plenvu innehåller också askorbat som kan vara skadligt för personer med glukos-6-fosfatdehydrogenas brist.
Hur produkten används
Ta alltid detta läkemedel enligt läkarens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
Läs vänligen noggrant igenom följande instruktioner före du tar Plenvu. Du bör veta:
- När Plenvu ska tas
- Hur Plenvu ska förberedas
- Hur Plenvu ska drickas
- Vad du ska förvänta dig att händer
När Plenvu ska tas
Din behandling med Plenvu ska vara slutförd före ditt kliniska ingrepp.
Denna behandlingen kan tas i delade doser såsom beskrivet nedan:
Två dagars delade doseringsschema
Dos 1 tas på kvällen före kliniska ingreppet och Dos 2 tas på morgonen dagen av det kliniska ingreppet, ungefär 12 timmar efter start av den första dosen, eller
Endast morgon doseringsschema
Dos 1 och Dos 2 tas på morgonen dagen av det kliniska ingreppet; den andra dosen ska tas minst 2 timmar efter start av den första dosen, eller
Dagen före doseringsschema
Dos 1 och Dos 2 tas på kvällen dagen före det kliniska ingreppet; den andra dosen ska tas minst 2 timmar efter start av den första dosen.
Din läkare informerar dig vilket doseringsschema som ska följas. Tillägg INTE någon annan substans till doserna.
Ät inte då du tar Plenvu utan först efter ditt kliniska ingrepp.
För information om tidsinställning av måltiderna före Plenvu tas hänvisas till avsnitt Vad du behöver veta innan produkten används.
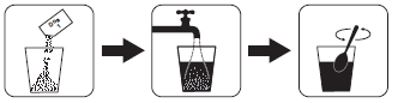
Hur Plenvu Dos 1 ska förberedas
- Öppna kartongen och avlägsna Dos 1 dospåsen.
- Häll innehållet av Dos 1 i ett måttkärl som rymmer 500 ml vätska
- Tillägg vatten så att mängden blir 500 ml och rör om tills pulvret har upplösts. Detta kan ta upp till ungefär 8 minuter.
Hur Plenvu Dos 1 ska drickas
Drick 500 ml lösning som innehåller Dos 1 samt ytterligare 500 ml klar vätska under 60 minuters tid. Du kan växla mellan den beredda lösningen och den klara vätskan. Försök att dricka ett glas varje 10 till 15 minuter.
Klar vätska kan vara vatten, klar soppa, utspädd saftkoncentrat/ klara fruktjuicer (utan fruktkött), te eller kaffe utan mjölk.
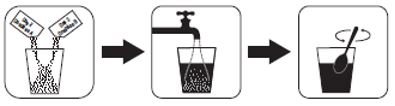
Hur Plenvu Dos 2 ska förberedas
- När du är färdig att ta Dos 2 häll innehållet av Dos 2 Dospåsen A och Dos 2 Dospåsen B i ett måttkärl som rymmer 500 ml vätska.
- Tillägg vatten så att mängden blir 500 ml och rör om tills pulvret har upplösts. Detta kan ta upp till ungefär 8 minuter.
Hur Plenvu Dos 2 ska drickas
När du är instruerad enligt rekommenderade doseringsschemat, gör i ordning och drick 500 ml lösning som innehåller Dos 2 samt ytterligare 500 ml klar vätska under 60 minuter. Du kan växla mellan den beredda lösningen och den klara vätskan.
Ytterligare klar vätska kan drickas under processen för rengöring av tarm, dvs. före, under, och efter att du tagit Plenvu, men du måste sluta dricka 1-2 timmar före ditt kliniska ingrepp. Att dricka klar vätska hjälper att förhindra vätskeförlust (dehydrering).
Vad du ska förvänta dig att händer
När du börjar dricka Plenvu lösningen är det viktigt att du stannar nära en toalett. I något skede kommer du att börja uppleva vattenfyllda tarmtömningar. Detta är fullkomligt normalt och är ett tecken på att Plenvu lösningen verkar. Du kan ha uppsvullnad i området kring magen före du har din första tarmtömning.
Om du följer dessa instruktioner kommer din tarm att vara ren och det kommer att hjälpa dig att få en lyckad undersökning. Du ska reservera tillräckligt med tid efter att dina tarmtömningar har lugnat sig för att resa till kliniken/sjukhuset.
Om du tar mera laxermedel än du borde
Om du tar Plenvu före eller efter att du tagit andra laxativa produkter kan du utveckla våldsam diarré, som kan leda till dehydrering. Ta riklig mängd klar vätska. Om du är orolig kontakta din läkare eller gå omedelbart till närmaste sjukhus akutmottagning.
Om du fått i dig för stor mängd läkemedel eller om t.ex. ett barn fått i sig läkemedlet av misstag kontakta läkare, sjukhus eller Giftinformationscentralen (tel.112) för bedömning av risken samt rådgivning.
Om du har glömt att ta Plenvu
- Om du glömmer att ta Plenvu enligt instruktionerna, ta den så snart du inser att du inte tagit den och kontakta din läkare, apotekspersonal eller sjuksköterska för råd före ditt kliniska ingrepp.
- Det är viktigt att du har reserverat tillräckligt med tid att slutföra din behandling med Plenvu för att försäkra att din tarm är helt rengjord åtmistone 2 timmar före ditt kliniska ingrepp.
Om du har ytterligare frågor om detta läkemedel, kontakta läkare, apotekspersonal eller sjuksköterska.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Det är normalt att få diarré när du tar Plenvu.
Om du inte har en tarmtömning inom 6 timmar från att du tagit Plenvu sluta med användningen och kontakta din läkare omedelbart.
Om du har någon av följande biverkningar sluta ta Plenvu och berätta åt din läkare omedelbart, eftersom dessa symtom kan vara tecken på en allvarlig allergisk reaktion:
- Extrem trötthet
- Hjärtklappning
- Utslag eller klåda
- Andfåddhet
- Svullnad i ditt ansikte, anklar eller annan kroppsdel
Sluta ta Plenvu och kontakta omedelbart läkare om du märker något av följande biverkningar:
- Krampanfall
Berätta åt din läkare omedelbart om du har någon av dessa symtom medan du tar Plenvu eftersom dessa symtom kan tyda på en förlust av för stor mängd kroppsvätska (dehydrering):
- Yrsel
- Huvudvärk
- Urinering mera sällan än normalt
- Kräkning
Berätta även genast åt din läkare om du har hård smärta i magområdet (buken).
Allvarliga hjärtrytmproblem kan förekomma sällan (dvs. det kan kännas som om hjärtat dunkar, fladdrar eller slår oregelbundet, oftast under några sekunder eller eventuellt några minuter) under användning av laxativer vid förberedelse av tarmen, speciellt hos patienter med underliggande hjärtsjukdom eller saltrubbning. Tala med din läkare om symtomerna fortsätter.
Vanliga biverkningar (kan påverka upp till 1 av 10 personer):
- Dehydrering
- Illamående (känna sig illamående)
- Kräkning
Mindre vanliga biverkningar (kan påverka upp till 1 av 100 personer):
- Buksvullnad och smärta
- Värkar och smärtor
- Allergisk reaktion
- Frossa
- Trötthet
- Huvudvärk eller migrän
- Värmevallningar
- Förhöjd blodsockernivå hos patienter med diabetes
- Förhöjd hjärtfrekvens
- Hjärtklappning
- Ömhet kring ändtarmsöppningen
- Sömnighet
- Tillfällig förhöjning av blodtrycket
- Tillfällig förhöjning av leverenzymerna
- Törstighet
- Olika salt (elektrolyt) störningar
Svaghet
Ingen känd frekevens (kan inte beräknas från tillgängliga data)
- Bristning i matstrupen på grund av kräkning
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan) Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
Webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Bivirkningsregistret
PB 55
00034 Fimea
Hur produkten ska förvaras
Förvaras utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på dospåsen och kartongen efter ”EXP”. Utgångsdatumet är den sista dagen i angiven månad.
Lägg märke till att utgångsdatumen kan variera för varje dospåse och kartong.
Före öppnande förvaras under 25 °C.
Förvara den förberedda lösningen under 25 °C och drick den inom 24 timmar. Lösningarna kan bevaras i ett kylskåp. Lösingarna måste täckas.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
Dos 1 dospåsen
- De aktiva substanserna är:
| Makrogol 3350 | 100 g |
| Vattenfritt natriumsulfat | 9 g |
| Natriumklorid | 2 g |
| Kaliumklorid | 1 g |
Koncentrationen av elektrolytjonerna när första dosen är kompletterad till 500 ml lösning är följande:
| Natrium | 160,9 mmol/500 ml |
| Sulfat | 63,4 mmol/500 ml |
| Klorid | 47,6 mmol/500 ml |
| Kalium | 13,3 mmol/500 ml |
Dos 1 innehåller också 0,79 g av sukralos (E955).
Dos 2 ( Dospåsarna A och B)
- De aktiva substanserna är:
Dospåse A:
| Makrogol 3350 | 40 g |
| Natriumklorid | 3,2 g |
| Kaliumklorid | 1,2 g |
Dospåse B:
| Natriumaskorbat | 48,11 g |
| Askorbinsyra | 7,54 g |
Koncentrationen av elektrolytjonerna när andra dosen (Dospåsarna A och B) är kompletterad till 500 ml lösning är följande:
| Natrium | 297,6 mmol/500 ml |
| Askorbat | 285,7 mmol/500 ml |
| Klorid | 70,9 mmol/500 ml |
| Kalium | 16,1 mmol/500 ml |
Hjälpämnen med känd effekt
Dos 2 (Dospåse A) innehåller också 0,88 g av aspartam (E951).
-Övriga innehållsämnen är:
mangoarom innehållande glycerol (E422), aromämnen, akaciagummi (E414), maltodextrin (E1400) och naturliga aromämnen; och fruktjuicearom innehållande aromämnen, akaciagummi (E414), maltodextrin (E1400) och aromämnen. För ytterligare information hänvisas till avsnitt Vad du behöver veta innan produkten används.
Läkemedlets utseende och förpackningsstorlekar
Denna förpackning innehåller tre dospåsar: Dos 1, Dos 2 Dospåse A, och Dos 2 Dospåse B. Plenvu pulver för oral lösning finns tillgänglig i förpackningar som innehåller 1 behandling och i förpackningar som innehåller 40, 80, 160 och 320 behandlingar. Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning och tillverkare
Innehavare av godkännande för försäljning
Norgine B.V.
Antonio Vivaldistraat 150
1083 HP Amsterdam
Nederländerna
Tillverkare:
Norgine B.V.
Antonio Vivaldistraat 150
1083 HP Amsterdam
Nederländerna
eller
Norgine Pharma
29 rue Ethe Virton
Dreux 28100
Frankrike
Detta läkemedel är godkänt inom Europeiska ekonomiska samarbetsområdet och i Förenade kungariket (Nordirland) under namnen:
Belgien, Bulgarien, Tjeckien, Kroatien, Danmark, Finland, Frankrike, Tyskland, Ungern, Island, Irland, Italien, Luxemburg, Norge, Polen, Portugal, Rumänien, Slovakien, Slovenien, Sverige, Storbritannien (Nordirland): : PLENVU
Österrike, Nederländerna, Spanien: PLEINVUE
Denna bipacksedel ändrades senast 23.07.2025