ENANTON DEPOT DUAL injektiokuiva-aine ja liuotin suspensiota varten, esitäytetty ruisku 30 mg
Enanton Depot Dual 30 mg injektiokuiva-aine ja liuotin suspensiota varten, esitäytetty ruisku
leuproreliiniasetaatti
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin aloitat tämän lääkkeen käyttämisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
- Tämä lääke on määrätty vain sinulle eikä sitä pidä antaa muiden käyttöön. Se voi aiheuttaa haittaa muille, vaikka heillä olisikin samanlaiset oireet kuin sinulla.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
- Mitä Enanton Depot Dual 30 mg on ja mihin sitä käytetään
- Mitä sinun on tiedettävä, ennen kuin käytät Enanton Depot Dual 30 mg ‑valmistetta
- Miten Enanton Depot Dual 30 mg ‑valmistetta käytetään
- Mahdolliset haittavaikutukset
- Enanton Depot Dual 30 mg ‑valmisteen säilyttäminen
- Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Enanton Depot Dual 30 mg on ihon alle ruiskutettava lääkevalmiste, joka sisältää leuproreliiniasetaattia. Lääkeaine on synteettinen hormoni, joka vähentää elimistön testosteroni- ja estrogeenipitoisuuksia. Lääkettä käytetään pitkälle edenneen eturauhassyövän hoitoon.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä käytä Enanton Depot Dual 30 mg ‑valmistetta, jos:
- olet allerginen leuproreliiniasetaatille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa) tai muille leuproreliinin kaltaisille aineille (synteettiselle GnRH:lle tai GnRH-johdannaisille).
Varoitukset ja varotoimet
Keskustele lääkärin kanssa ennen kuin käytät Enanton Depot Dual ‑valmistetta, jos sinulla on:
- virtsatietukos
- selkäydinvaurio
- diabetes
- suurentunut riski saada aineenvaihdunta-, sydän- tai verisuonisairauksia
- jokin sydän- tai verisuonisairaus, kuten sydämen rytmihäiriö (arytmia), tai sinua hoidetaan lääkkeillä sen takia. Sydämen rytmihäiriön riski voi kasvaa kun käytetään Enanton Depot Dual ‑valmistetta.
- suurentunut riski saada osteoporoosi ja luunmurtumia
- epilepsia tai sinulla on ollut epileptisiä kohtauksia
- rasvamaksa
- jos sinulle ilmaantuu kovaa tai toistuvaa päänsärkyä, näköhäiriöitä ja korvien soimista tai surinaa, ota välittömästi yhteys lääkäriin.
Potilailla, jotka käyttävät Enanton Depot Dual ‑valmistetta on raportoitu masennusta, joka saattaa olla vakavaa. Kerro lääkärille, jos Enanton Depot Dual ‑valmisteen käytön yhteydessä sinulle ilmaantuu masentuneisuutta.
Leuproreliinin yhteydessä on raportoitu vaikeita ihottumia, mukaan lukien Stevens–Johnsonin oireyhtymä ja toksinen epidermaalinen nekrolyysi (SJS/TEN). Lopeta leuproreliinin käyttö ja hakeudu välittömästi lääkärin hoitoon, jos havaitset jotakin näihin vakaviin ihoreaktioihin liittyvistä oireista, jotka on kuvattu kohdassa Mahdolliset haittavaikutukset.
Muut lääkevalmisteet ja Enanton Depot Dual 30 mg
Enanton Depot Dual ‑valmisteella voi olla yhteisvaikutuksia joidenkin sydämen rytmihäiriön hoitoon käytettyjen lääkkeiden kanssa (esim. kinidiini, prokaiiniamidi, amiodaroni ja sotaloli) tai lisätä riskiä sydämen rytmihäiriöön kun sitä käytetään joidenkin muiden lääkkeiden kanssa (esim. metadoni (käytetään kivun lievitykseen ja huumeriippuvuuden katkaisuhoitoon), moksifloksasiini (antibiootti), psyykkisten sairauksien hoitoon käytettävät psykoosilääkkeet).
Kerro lääkärille, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä. Tämä koskee sekä reseptilääkkeitä että ilman reseptiä saatavia lääkkeitä, rohdosvalmisteita ja luontaistuotteita. Kerro lääkärille myös, jos sinulla on muita sairauksia tai allergioita.
Muista mainita tämän valmisteen käytöstä seuraavien lääkärissä käyntien yhteydessä.
Raskaus ja imetys
Valmiste on tarkoitettu vain miehille eturauhassyövän hoitoon.
Ajaminen ja koneiden käyttö
Valmiste voi vaikuttaa ajokykyyn ja koneiden käyttökykyyn, koska leuproreliiniasetaatin on raportoitu aiheuttaneen uupumusta, väsymystä, näköhäiriöitä ja huimausta.
Lääkkeet voivat heikentää kykyä kuljettaa moottoriajoneuvoa tai suorittaa erityistä tarkkaavaisuutta vaativia tehtäviä. On omalla vastuullasi arvioida, pystytkö näihin tehtäviin lääkehoidon aikana. Lääkkeen vaikutuksia ja haittavaikutuksia on kuvattu muissa kappaleissa. Lue koko pakkausseloste opastukseksesi. Keskustele lääkärin tai apteekkihenkilökunnan kanssa, jos olet epävarma.
Enanton Depot Dual sisältää polysorbaattia
Tämä lääke sisältää polysorbaattia 1,0 mg/injektioruisku. Polysorbaatit saattavat aiheuttaa allergisia reaktioita. Jos sinulla on allergioita, kerro asiasta lääkärille.
Muut apuaineet
Tämä lääke sisältää alle 1 mmol (23 mg) natriumia per annos eli sen voidaan sanoa olevan ”natriumiton”.
Miten valmistetta käytetään
Lääkäri on määrännyt sinulle ja sairauteesi sopivan annostuksen sekä hoidon keston. Käytä tätä lääkettä juuri siten kuin lääkäri on määrännyt. Jos valmisteen vaikutus on mielestäsi liian voimakas tai liian heikko, ota yhteys lääkäriin tai apteekkihenkilökuntaan.
Enanton Depot Dual -valmisteen saa antaa vain lääkäri tai hoitohenkilökunta. He myös huolehtivat valmisteen käyttövalmiiksi saattamisesta.
Annostus ja hoitoaika
- Eturauhassyövän lääkehoito on yleensä pitkäkestoista.
- 30 mg lääkeainetta annetaan kerta-annoksena ihon alle noin kuuden kuukauden välein (168–180 päivää).
- Oikea annosväli (6 kk) on tärkeä, jotta eturauhassyövän oireet eivät pahene.
- Lääke ruiskutetaan ihon alle. Laskimoon tai valtimoon annettu ruiske saattaa aiheuttaa verisuonitukoksen.
Lääkäri tai sairaanhoitaja antaa sinulle injektion. Katso kohta ”Injektion valmistaminen ja antotapa” pakkausselosteen lopusta.
Jos otat enemmän Enanton Depot Dual 30 mg ‑valmistetta kuin sinun pitäisi
Jos olet ottanut liian suuren lääkeannoksen tai vaikkapa lapsi on ottanut lääkettä vahingossa, ota aina yhteyttä lääkäriin, sairaalaan tai Myrkytystietokeskukseen (puh. 0800 147 111) riskien arvioimiseksi ja lisäohjeiden saamiseksi.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa. Lääkkeen haittavaikutukset johtuvat pääosin hormonitoiminnan muutoksista.
Hoidon alussa eturauhassyövän oireet voivat ohimenevästi paheta, mistä voi seurata luukipua, virtsatiehyiden oireita, alaraajojen heikkoutta ja harhatuntemuksia. Lisäksi Enanton Depot Dual 30 mg ‑valmisteen käytön yhteydessä voi ilmetä muutoksia aineenvaihdunnassa (esim. glukoosi-intoleranssia tai diabeteksen pahentumista) tai sydän‑ ja verisuonitapahtumien riskin suurenemista.
Aivolisäkeperäinen halvaus (pituitaarinen apopleksia) on kuvattu erittäin harvinaisena haittavaikutuksena, kun tämän tyyppistä lääkettä on annettu ensimmäistä kertaa potilaille, joilla on aivolisäkkeen kasvain. Apopleksian oireita ovat äkillinen päänsärky, oksentelu, näköhäiriöt ja silmälihashalvaus.
Esiintymistiheys tuntematon (koska saatavissa oleva tieto ei riitä arviointiin):
Hakeudu kiireellisesti hoitoon, jos saat seuraavia oireita:
- punoittavia läiskiä keholla (maalitaulun näköisiä tai rengasmaisia läiskiä, jotka eivät ole koholla ja joiden keskellä saattaa olla rakkuloita), ihon kesimistä, haavaumia suussa, nielussa, nenässä, sukupuolielimissä ja silmissä. Näitä vakavia ihottumia voivat edeltää kuume ja flunssankaltaiset oireet. (Stevens–Johnsonin oireyhtymä/toksinen epidermaalinen nekrolyysi/eksfoliatiivinen dermatiitti).
- ihon punoitus ja kutiseva ihottuma (toksinen ihottuma)
- rakkulaihottuma
- ihoreaktio, joka aiheuttaa iholle punaisia täpliä tai läiskiä, joiden muoto saattaa muistuttaa maalitaulua (tummanpunainen keskiosa, jota ympäröivät vaaleammat punertavat renkaat) (erythema multiforme)
- nopeasti ilmaantuvat punaiset ihoalueet, jotka ovat täynnä pieniä märkärakkuloita (pieniä rakkuloita, joissa on valkoista tai keltaista nestettä; reaktiota kutsutaan akuutiksi yleistyneeksi eksantematoottiseksi pustuloosiksi [AGEP]).
Yleiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 10:stä):
Mielialan vaihtelu, masennus, unettomuus, kuumat aallot, laktaattidehydrogenaasi-entsyymin pitoisuuden nousu veressä, maksan toiminnan häiriö (keltaisuus), hikoilu, lihasheikkous, vähentynyt seksuaalinen halu ja kyky, kivesten pieneneminen, pistoskohdan reaktiot, kuumotus.
Melko harvinaiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 100:sta):
Anemia, verihiutaleiden väheneminen, painon muutos, ruokahaluttomuus, triglyseridi‑, kolesteroli‑, sokeri‑, kalium‑ tai virtsahappopitoisuuden nousu veressä, päänsärky, huimaus, tuntoharhat, kuurous, korvien soiminen, epänormaalit EKG-löydökset, sydämen suureneminen, kasvojen kuumotus, pahoinvointi, oksentelu, bilirubiinipitoisuuden ja maksa-arvojen nousu veressä, ihotulehdus, lisääntynyt hiustenkasvu, ihottuma, kutina, nivel‑, luu-, hartia‑, alaselkä‑ tai raajakipu, tihentynyt virtsaamistarve, verivirtsaisuus, veren ureapitoisuuden nousu, rintojen kasvu, epämiellyttävä tunne lantionpohjan alueella, kävelemisvaikeudet, turvotus, paineen tunne rinnassa, jäykkyys, huonovointisuus, väsymys, kuume, oireet injektioalueella (kipu, kovettumat, punoitus).
Harvinaiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 1 000:sta):
Yliherkkyys, ihottuma, kutina, nokkosihottuma, hengityksen vinkuminen, kuume, vilunväristykset, anafylaktinen reaktio, veritulppa, keuhkoveritulppa, ripuli, lihaskipu, injektioalueen märkäpesäkkeet.
Hyvin harvinaiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 10 000:sta):
Aivolisäkeperäinen halvaus.
Esiintymistiheys tuntematon (koska saatavissa oleva tieto ei riitä arviointiin):
Metabolinen oireyhtymä kuten kohonnut verenpaine, dyslipidemia (aineenvaihduntahäiriöstä johtuva haitallinen tila, jossa veren lipidien suhteelliset osuudet tai pitoisuudet poikkeavat tavoitearvoista), insuliiniresistenssi (ominaisuus jonka takia insuliini pienentää veren glukoosipitoisuutta odotettua vähemmän) tai heikentynyt insuliinitoleranssi, epileptinen kohtaus, rasvamaksa, näköhäiriöt, sydämentykytys, muutokset EKG:ssä (QT‑ajan pidentyminen), keuhkotulehdus, keuhkosairaus, luukato (sis. selkärangan murtuma), luun mineraalipitoisuuden lasku, idiopaattinen kallonsisäisen paineen (aivopaineen) kohoaminen (jonka oireita ovat päänsärky, kaksoiskuvat ja muut näköhäiriöt sekä korvan tai korvien soiminen tai surina).
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Valmisteen säilyttäminen
Älä säilytä kylmässä. Ei saa jäätyä.
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pakkauksessa mainitun viimeisen käyttöpäivämäärän jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää. Käyttövalmis suspensio on käytettävä välittömästi.
Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä Enanton Depot Dual 30 mg sisältää
Injektiokuiva-aine sisältää 30 mg leuproreliiniasetaattia, joka vastaa 28,58 mg leuproreliiniemästä. Injektiokuiva-aineen apuaineet ovat poly(maitohappo) ja mannitoli.
Esitäytetty ruisku sisältää 1 ml liuotinta, joka sisältää mannitolia, karmelloosinatriumia, polysorbaatti 80:a, väkevää etikkahappoa (pH:n säätöön) ja injektionesteisiin käytettävää vettä.
Lääkevalmisteen kuvaus ja pakkauskoko
Esitäytetty ruisku on kaksikammioruisku turvasuojuksellisella neulalla, ja se sisältää valkoista jauhetta ja kirkasta, väritöntä liuosta.
1 esitäytetty kaksikammioruisku, jonka toisessa kammiossa on injektiokuiva-ainetta ja toisessa kammiossa 1 ml liuotinta (lasi Ph. Eur. tyyppi I, kumitulpat silikonoitua klorobutyylikumia), ja 1 turvasuojuksellinen neula (23 G).
Myyntiluvan haltija
Orion Corporation
Orionintie 1
02200 Espoo
Valmistaja
Orion Corporation Orion Pharma
Orionintie 1
02200 Espoo
Orion Corporation Orion Pharma
Joensuunkatu 7
24100 Salo
Tämä pakkausseloste on tarkistettu viimeksi 28.10.2024
Ohjeet terveydenhuollon ammattilaiselle
Injektion valmistaminen ja antotapa
Injektiokuiva-aine ja liuotin sekoitetaan ennen käyttöä. HUOM.! Älä vedä mäntää taaksepäin missään vaiheessa, koska tämän seurauksena tulpat erkaantuvat toisistaan, mikä voi johtaa vuotamiseen tulppien väleistä tai ruiskun mäntäpuolelta.
Yleisiä ohjeita
- Varmista, että suspensio on tasa-aineinen ennen annostelua.
- Käytä valmis suspensio välittömästi.
- Lääkettä ei saa pistää samaan paikkaan kahta kertaa peräkkäin, vaan pistoskohtaa tulee vaihdella.
- Käyttövalmista suspensiota ei saa säilyttää, koska valmiste ei sisällä säilöntäainetta.
- Pistoskohtaa ei saa hieroa.
- Peitä injektiokohta tarvittaessa laastarilla.
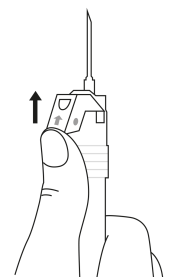
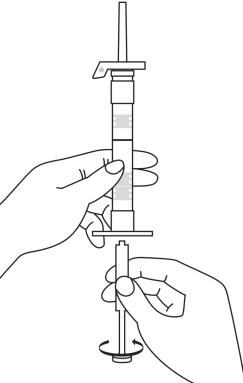 | 1. Pidä ruisku pystyasennossa (neula ylöspäin). Männän varsi kierretään kiinni ruiskun päähän kunnes taaempi kumitulppa alkaa liikkua. | 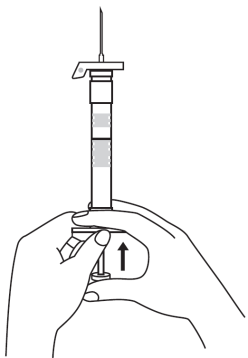 | 5. Pidä ruiskua siten, että neula osoittaa ylöspäin, jotta näet, onko ruiskun sisällä ilmakuplia. Jos ilmakuplia näkyy, paina mäntää varovasti, kunnes kaikki ilma (mutta ei yhtään nestettä) poistuu ruiskusta. |
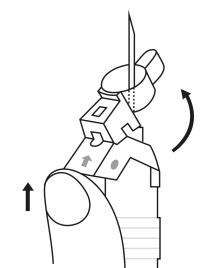
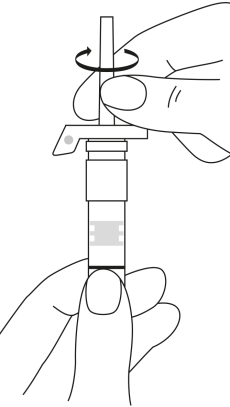 | 2. Pidä ruisku pystyasennossa (neula ylöspäin). Tarkista, että neula on kunnolla kiinnitetty ruiskuun kiertämällä neulansuojuksesta myötäpäivään. Varo kiertämästä liian tiukkaan. Naputa ruiskua varovasti sormella, jotta jauhe irtoaa kammion seinästä. |
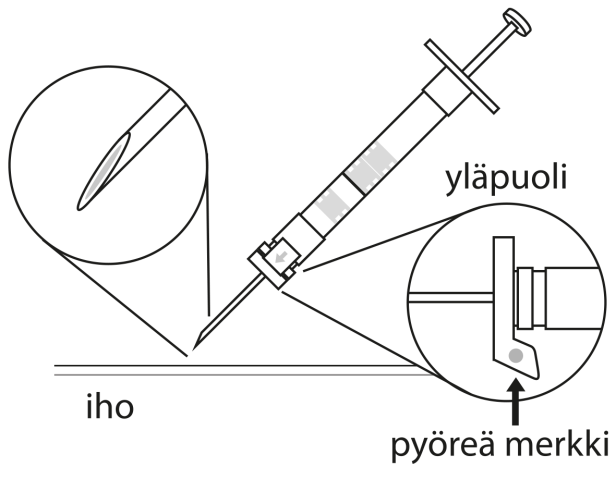
6. Puhdista ihoalue ennen pistosta antiseptisella aineella. Injektiota annettaessa turvasuojuksen pyöreän merkin tulee osoittaa ylöspäin. Varmista, että neula ei lävistä verisuonta ja injisoi ruiskun koko sisältö kerralla ihonalaisesti, kuten normaalia injektiota annettaessa. | |
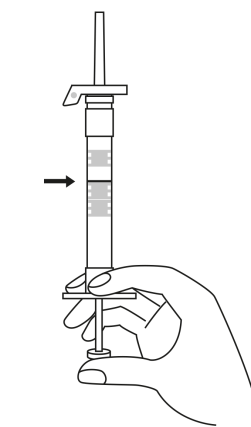 | 3. Pidä ruisku pystyasennossa (neula ylöspäin). Työnnä mäntää hitaasti (6‑8 sekuntia) kunnes keskimmäisen kumitulpan yläosa on sinisen viivan kohdalla. | ||
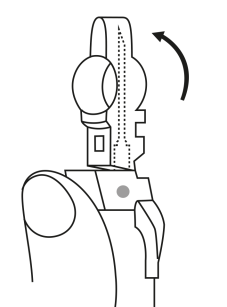
INJEKTION JÄLKEEN 7. Turvasuojuksen vipuun on painettuna nuoli. Heti injektion jälkeen työnnä sormella turvalaitteen vipua nuolen osoittamaan suuntaan. Tällöin suojus liukuu kohti neulan kärkeä ja lukittuu sen suojaksi. Varmista lukitus kuuntelemalla tai tunnustelemalla (lukituksesta kuuluu ”klik” tai tuntuu napsahdus). | |||
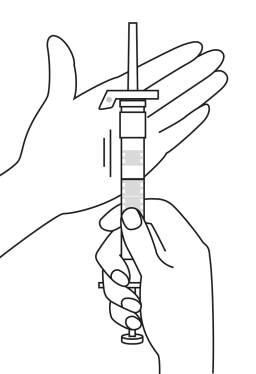 | 4. Pidä ruisku pystyasennossa (neula ylöspäin). Ravistele varovasti ruiskua, kunnes suspensio on tasa-aineinen. Valmis injektio on valkoinen maitomainen suspensio. Vedä varovasti neulan suojus irti. | ||