VIGAMOX ögondroppar, lösning 5 mg/ml
Tilläggsinformation
Vigamox 5 mg/ml ögondroppar, lösning
moxifloxacin
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
- Vad Vigamox är och vad det används för
- Vad du behöver veta innan du använder Vigamox
- Hur du använder Vigamox
- Eventuella biverkningar
- Hur Vigamox ska förvaras
- Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Vigamox innehåller den aktiva substansen moxifloxacin. Moxifloxacin tillhör en klass av antibiotika som kallas fluorokinoloner som används för att behandla bakteriella infektioner i ögonen.
Vigamox ögondroppar används för att behandla infektioner i ögat (konjunktivit) som orsakats av bakterier.
Moxifloxacin som finns i Vigamox kan också vara godkänd för att behandla andra sjukdomar som inte nämns i denna bipacksedel. Fråga läkare, apotekspersonal eller annan hälso- och sjukvårdspersonal om du har ytterligare frågor och följ alltid deras instruktion.
Vad du behöver veta innan produkten används
Använd inte Vigamox
- Om du är allergisk mot moxifloxacin, mot andra kinoloner eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
Varningar och försiktighet
Tala med läkare eller apotekspersonal innan du använder Vigamox.
- Om du får en allergisk reaktion mot Vigamox. Allergiska reaktioner uppkommer i mindre vanliga fall och allvarliga reaktioner är sällsynta. Om du får en allergisk (överkänslighets-) reaktion eller en biverkan, se avsnitt Eventuella biverkningar.
- Om du använder kontaktlinser – sluta att använda linserna om du har tecken eller symtom på en ögoninfektion. Använd dina glasögon istället. Börja inte använda linserna igen förrän tecknen och symtomen på infektion har gått över och du har slutat använda läkemedlet.
- Det har hänt att personer som tagit flurokinoloner via munnen eller intravenöst har drabbats av svullna senor och bristningar, särskilt hos äldre patienter och hos dem som samtidigt behandlas med kortikosteroider. Sluta ta Vigamox om du får ont i en sena eller om den börjar svullna.
I likhet med alla antibiotika kan långtidsanvändning av Vigamox leda till andra infektioner.
Andra läkemedel och Vigamox
Tala om för läkare eller apotekspersonal om du använder, nyligen har använt eller kan tänkas använda andra läkemedel.
Graviditet, amning och fertilitet
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare eller apotekspersonal innan du använder detta läkemedel.
Körförmåga och användning av maskiner
Du kanske märker att du ser suddigt under en kort tid precis efter det att du använt Vigamox. Kör inte bil och använt inte maskiner förrän synen är normal igen.
Du är själv ansvarig för att bedöma om du är i kondition att framföra motorfordon eller utföra arbete som kräver skärpt vaksamhet. En av faktorerna som kan påverka din förmåga i dessa avseenden är användning av läkemedel på grund av deras effekter och/eller biverkningar. Beskrivning av dessa effekter och biverkningar finns i andra avsnitt. Läs därför all information i denna bipacksedel för vägledning. Diskutera med läkare eller apotekspersonal om du är osäker.
Hur produkten används
Använd alltid detta läkemedel enligt läkarens eller apotekspersonalens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
Rekommenderad dos:
Vuxna, inklusive äldre, och barn: 1 droppe i det/de angripna ögat/ögonen, 3 gånger per dag (på morgonen, på eftermiddagen och på kvällen).
Vigamox kan användas till barn, till patienter över 65 år och till patienter med njur- eller leverproblem. Det finns bara mycket begränsad information om användning av detta läkemedel till nyfödda, och därför rekommenderas inte användning till nyfödda.
Använd detta läkemedel i båda ögonen endast om läkaren har sagt åt dig att göra det. Vigamox ska endast användas för ögonbruk.
Infektionen brukar förbättras inom 5 dagar. Du bör fortsätta att använda dropparna i ytterligare 2–3 dagar eller enligt läkarens anvisningar. Om du inte märker någon förbättring efter 5 dagar, kontakta läkaren.
- Ta fram flaskan med Vigamox och stå framför en spegel
- Tvätta händerna
- Vrid av locket
- Om den säkerhetsförseglade lockkragen är lös efter att locket tagits av ska även den tas av innan produkten används.
- Håll flaskan upp och ned mellan tummen och fingrarna
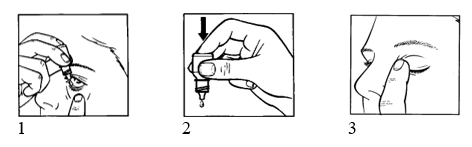
- Luta huvudet bakåt. Dra ner det undre ögonlocket med ett rent finger tills det bildas en ”ficka” mellan ögonlocket och ögat. Där ska droppen placeras (bild 1)
- Håll flaskans droppspets nära ögat. Använd spegeln som hjälp.
- Undvik att vidröra ögat eller ögonlocket, omgivande områden eller andra ytor med droppspetsen. Då kan dropparna infekteras.
- Tryck lätt i flaskans botten för att pressa ut en droppe av läkemedlet i taget (bild 2)
- När du använt Vigamox, tryck med ett finger i ögonvrån vid näsan i 2–3 minuter (bild 3). Detta hindrar läkemedlet från att komma ut i resten av kroppen, vilket är särskilt viktigt för små barn.
- Om du använder dropparna i båda ögonen, tvätta händerna innan du upprepar samma steg för det andra ögat. Det hjälper till att förhindra att infektionen sprids från det ena ögat till det andra.
- Stäng flasklocket omedelbart efter användning.
Om en droppe missar ögat, försök igen.
Om du har använt för stor mängd av Vigamox skölj ut allt med ljummet vatten. Droppa inte i fler droppar förrän det är dags för din nästa vanliga dos.
Om du fått i dig för stor mängd läkemedel eller om t.ex. ett barn fått i sig läkemedlet av misstag kontakta läkare, sjukhus eller Giftinformationscentralen (tel. 0800 147 111) för bedömning av risken samt rådgivning.
Om du av misstag råkar svälja Vigamox ska du rådfråga läkare eller apotekspersonal.
Om du har glömt att använda Vigamox, fortsätt med nästa dos som planerat. Ta inte dubbel dos för att kompensera för glömd dos.
Om du använder andra ögonpreparat, vänta minst 5 minuter mellan användningen av Vigamox och de andra ögonpreparaten.
Om du har ytterligare frågor om detta läkemedel kontakta läkare eller apotekspersonal.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Du kan vanligtvis fortsätta att ta dropparna om inte biverkningarna är allvarliga eller du får en svår allergisk reaktion.
Om du får en svår allergisk reaktion och något av följande händer, sluta ta Vigamox omedelbart och kontakta omedelbart din läkare: Svullnad i händer, fötter, fotleder, ansikte, läppar, mun eller svalg, som kan göra det svårt att svälja eller andas, utslag eller nässelfeber, stora vätskefyllda blåsor, ömma ställen och sår.
Vanliga biverkningar (kan förekomma hos upp till 1 av 10 användare)
Biverkningar i ögat: Ögonsmärta, ögonirritation
Mindre vanliga biverkningar (kan förekomma hos upp till 1 av 100 användare)
Biverkningar i ögat: Torra ögon, kliande ögon, ögonrodnad, inflammation eller ärrbildning på ögats yta, brustna blodkärl i ögat, onormal känsla i ögat, ögonlocksproblem, klåda, rodnad eller svullnad
Allmänna biverkningar: Huvudvärk, dålig smak i munnen
Sällsynta biverkningar (kan förekomma hos upp till 1 av 1000 användare)
Biverkningar i ögat: Hornhinnestörning, dimsyn eller nedsatt synförmåga, inflammation eller infektion i bindhinnan, ögontrötthet, ögonsvullnad
Allmänna biverkningar: Kräkning, obehag i näsan, känsla av att ha en klump i halsen, minskad järnhalt i blodet, onormala resultat av leverprover, onormal känsla i huden, smärta, halsirritation
Har rapporterats (förekommer hos ett okänt antal användare)
Biverkningar i ögat: Infektion i ögat, grumling av ögats yta, svullnad i hornhinnan, utfällningar på ögats yta, ökat tryck i ögat, rispor på ögats yta, ögonallergi, sekretion från ögat, ökad tårproduktion, ljuskänslighet.
Allmänna biverkningar: Andfåddhet, oregelbunden hjärtrytm, yrsel, förvärrade allergiska symtom, klåda, utslag, hudrodnad, illamående och nässelutslag.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
I Finland:
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
FI-00034 Fimea
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på flaskan och kartongen efter ”EXP”. Utgångsdatumet är den sista dagen i angiven månad.
Inga särskilda förvaringsanvisningar.
Kasseras 4 veckor efter öppnandet. Detta görs för att förhindra infektioner.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
Den aktiva substansen är moxifloxacin.
En ml av ögondropparna innehåller 5,45 mg moxifloxacinhydroklorid motsvarande 5 mg moxifloxacin. En ögondroppe innehåller 190 mikrogram moxifloxacin.
Övriga innehållsämnen är: Natriumklorid, borsyra, renat vatten.
Mycket små mängder natriumhydroxid och saltsyra kan tillsättas för att justera surhetsnivåerna (pH-nivåer).
Läkemedlets utseende och förpackningsstorlekar
Detta läkemedel är en vätska (en klar, grön-gul lösning) som levereras i en förpackning innehållande en 5 ml plastflaska med skruvlock.
Innehavare av godkännande för försäljning
Novartis Finland Oy
Norrskensgränden 1
02100 Esbo
Tillverkare
Novartis Farmacéutica, S.A.
Gran Via de les Corts Catalanes, 764
08013 Barcelona
Spanien
Novartis Manufacturing NV
Rijksweg 14
2870 Puurs-Sint-Amands
Belgien
Detta läkemedel är godkänt inom Europeiska ekonomiska samarbetsområdet och i Storbritannien (Nordirland) under följande namn:
MOXIFLOXACIN ALCON: Tyskland
KANAVIG: Belgien, Luxemburg
VIGAMOX: Bulgarien, Cypern, Danmark, Estland, Finland, Grekland, Island, Italien, Lettland, Litauen, Malta, Nederländerna, Polen, Portugal, Rumänien, Slovakien, Slovenien, Spanien, Sverige, Tjeckiska Republiken, Ungern
MOXIVIG: Storbritannien (Nordirland)
Denna bipacksedel ändrades senast:
I Finland 18.12.2025