AREXVY injektiokuiva-aine ja suspensio, suspensiota varten
Arexvy injektiokuiva‑aine ja suspensio suspensiota varten
RSV‑rokote (rekombinantti, adjuvanttia sisältävä)
Respiratory Syncytial Virus (RSV) vaccine (recombinant, adjuvanted)
Lisäseuranta
▼Tähän lääkevalmisteeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti turvallisuutta koskevaa uutta tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista. Ks. kohdan Mahdolliset haittavaikutukset lopusta, miten haittavaikutuksista ilmoitetaan.
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin saat tätä rokotetta, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
- Tämä lääke on määrätty vain sinulle eikä sitä pidä antaa muiden käyttöön.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
1. Mitä Arexvy on ja mihin sitä käytetään
2. Mitä sinun on tiedettävä, ennen kuin saat Arexvya
3. Miten Arexvy annetaan
4. Mahdolliset haittavaikutukset
5. Arexvyn säilyttäminen
6. Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Arexvy on rokote, joka suojaa vähintään 18‑vuotiaita aikuisia RS‑virukselta (RSV eli respiratory syncytial virus).
RSV on hyvin helposti leviävä hengitysteiden virus.
- RSV voi aiheuttaa alahengitystiesairauden eli infektion keuhkoissa ja muissa hengityselimissä.
RSV‑infektio aiheuttaa terveille aikuisille yleensä lieviä, flunssankaltaisia oireita. RSV voi kuitenkin myös:
- aiheuttaa vakavamman hengitystiesairauden ja komplikaatioita, kuten keuhkotulehduksen (keuhkokuumeen), iäkkäämmille aikuisille ja aikuisille, joilla on jokin perussairaus
- pahentaa tiettyjä sairauksia, kuten kroonista hengitystie‑ tai sydänsairautta.
Miten Arexvy vaikuttaa
Arexvy auttaa elimistön luontaista puolustusjärjestelmää muodostamaan vasta‑aineita ja tietyntyyppisiä valkosoluja, jotka suojaavat RS‑virukselta.
Arexvy ei sisällä itse virusta, eli se ei voi aiheuttaa infektiota.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä käytä Arexvya
- jos olet allerginen vaikuttaville aineille tai tämän rokotteen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa).
Älä käytä Arexvya, jos jokin edellä mainituista koskee sinua. Keskustele lääkärin tai apteekkihenkilökunnan kanssa, jos olet epävarma.
Varoitukset ja varotoimet
Keskustele lääkärin, apteekkihenkilökunnan tai sairaanhoitajan kanssa ennen kuin sinulle annetaan Arexvya
- jos olet joskus saanut vakavan allergisen reaktion minkä tahansa muun rokotteen pistämisen yhteydessä.
- jos sinulla on vaikea infektio, johon liittyy kuumetta. Tällaisessa tilanteessa rokotusta voidaan siirtää, kunnes voit paremmin. Vähäinen infektio kuten nuhakuume ei luultavasti ole ongelma, mutta keskustele asiasta ensin lääkärin kanssa.
- jos sinulla on verenvuotohäiriö tai saat herkästi mustelmia.
- jos olet joskus pyörtynyt rokotustilanteessa – pyörtyminen voi tapahtua ennen neulanpistoa tai neulanpiston jälkeen
sinulla on heikentynyt immuunijärjestelmä, mikä saattaa estää sinua saamasta Arexvysta täyttä hyötyä.
Jos jokin edellä mainituista koskee sinua (tai olet epävarma asiasta), ota yhteys lääkäriin tai apteekkihenkilökuntaan ennen kuin sinulle annetaan Arexvya.
Kuten muutkaan rokotteet, Arexvy ei välttämättä tuota kaikille rokotetuille täydellistä suojaa.
Muut lääkevalmisteet/rokotteet ja Arexvy
Kerro lääkärille tai apteekkihenkilökunnalle:
- jos parhaillaan otat, olet äskettäin ottanut tai saatat ottaa muita lääkkeitä. Tämä koskee myös ilman reseptiä saatavia lääkkeitä.
- jos olet äskettäin saanut jotain muuta rokotetta.
Arexvy voidaan antaa samaan aikaan influenssarokotteen, pneumokokkikonjugaattirokotteen, vyöruusurokotteen (herpes zoster) tai COVID-19 mRNA-rokotteen kanssa.
Jos Arexvy annetaan samaan aikaan toisen pistosmuotoisen rokotteen kanssa, rokotteet pistetään eri kohtaan eli eri käsivarsiin.
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä tai apteekista neuvoa ennen kuin saat tätä rokotetta.
Arexvyn käyttö raskauden tai imetyksen aikana ei ole suositeltavaa.
Ajaminen ja koneiden käyttö
Joillakin jäljempänä kohdassa Mahdolliset haittavaikutukset ”Mahdolliset haittavaikutukset” mainituilla haittavaikutuksilla (esim. väsymyksellä) voi olla ohimenevä vaikutus ajokykyyn tai koneidenkäyttökykyyn. Älä aja äläkä käytä koneita tai työkaluja, jos vointisi on huono.
Arexvy sisältää natriumia ja kaliumia
Tämä lääkevalmiste sisältää alle 1 mmol natriumia (23 mg) per annos eli sen voidaan sanoa olevan ”natriumiton”.
Tämä lääkevalmiste sisältää kaliumia alle 1 mmol (39 mg) per annos eli sen voidaan sanoa olevan ”kaliumiton”.
Miten valmistetta käytetään
Arexvy pistetään 0,5 ml:n kerta‑annoksena lihakseen, yleensä olkavarteen.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Vakavat haittavaikutukset
Hyvin harvinaiset (voi esiintyä enintään 1 rokoteannoksen yhteydessä 10000:sta):
- hermoston häiriö, joka alkaa yleensä pistelystä ja raajojen heikkoudesta ja voi edetä osan tai koko kehon halvaantumiseen (Guillain-Barrén oireyhtymä).
Kerro lääkärille välittömästi, jos huomaat merkkejä tästä vakavasta haittavaikutuksesta.
Arexvyn annon jälkeen voi esiintyä seuraavia haittavaikutuksia:
Hyvin yleiset (voi esiintyä yli 1 rokoteannoksen yhteydessä 10:stä)
- pistoskohdan kipu
- väsymys
- päänsärky
- lihaskipu
nivelkipu
Yleiset (voi esiintyä enintään 1 rokoteannoksen yhteydessä 10:stä)
- pistoskohdan turvotus
- pistoskohdan punoitus
- kuume
- vilunväristykset.
Melko harvinaiset (voi esiintyä enintään 1 rokoteannoksen yhteydessä 100:sta)
- pistoskohdan kutina
- kipu
- yleinen huonovointisuus
- kaulan, kainaloiden tai nivusten imusolmukkeiden suureneminen (turvotus)
- allergiset reaktiot, kuten ihottuma
- pahoinvointi
- oksentelu
- vatsakipu.
Tuntematon (koska saatavissa oleva tieto ei riitä esiintyvyyden arviointiin):
ihokudoksen kuolio pistoskohdassa (pistoskohdan nekroosi)
Kerro lääkärille tai apteekkihenkilökunnalle, jos sinulle ilmaantuu jokin edellä mainituista haittavaikutuksista. Useimmiten nämä haittavaikutukset ovat lieviä tai keskivaikeita eivätkä kestä pitkään.
Jos havaitset sellaisia haittavaikutuksia, joita ei ole mainittu tässä selosteessa, tai jos kokemasi haittavaikutus on vakava, kerro niistä lääkärille tai apteekkihenkilökunnalle.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Valmisteen säilyttäminen
- Ei lasten ulottuville eikä näkyville.
- Älä käytä tätä lääkettä etiketissä ja kotelossa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
- Säilytä jääkaapissa (2 °C – 8 °C).
- Ei saa jäätyä.
- Säilytä alkuperäispakkauksessa. Herkkä valolle.
- Lääkkeitä ei pidä heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.
Pakkauksen sisältö ja muuta tietoa
Mitä Arexvy sisältää
- Vaikuttavat aineet ovat:
Käyttökuntoon saattamisen jälkeen yksi annos (0,5 ml) sisältää:
RSVPreF31‑antigeeni2,3 120 mikrogrammaa
1 RSVPreF3 = RS-viruksen rekombinantti glykoproteiini F, joka on stabiloitu fuusioitumista edeltävään konformaatioon.
2 RSVPreF3 on valmistettu kiinanhamsterin munasarjasoluissa yhdistelmä‑DNA‑tekniikalla.
3 Adjuvantti AS01E sisältää seuraavia aineita:
Quillaja saponaria Molina ‑kasviuute, fraktio 21 (QS‑21) 25 mikrogrammaa
3‑O‑desasyyli‑4’‑monofosforyylilipidi A (MPL) Salmonella minnesota ‑mikrobista 25 mikrogrammaa
RSVPreF3 on RS‑viruksessa esiintyvä proteiini. Tämä proteiini ei ole tartuttava.
Adjuvantilla tehostetaan elimistön reagointia rokotteeseen.
- Muut aineet ovat:
- Kuiva‑aine (RSVPreF3‑antigeeni): trehaloosidihydraatti, polysorbaatti 80 (E 433), kaliumdivetyfosfaatti (E340), dikaliumfosfaatti (E340).
- Suspensio: dioleoyylifosfatidyylikoliini (E322), kolesteroli, natriumkloridi, vedetön dinatriumfosfaatti (E339), kaliumdivetyfosfaatti (E340) ja injektionesteisiin käytettävä vesi.
Ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä, ”Arexvy sisältää natriumia ja kaliumia”.
Lääkevalmisteen kuvaus ja pakkauskoko (‑koot)
- Injektiokuiva‑aine ja suspensio suspensiota varten.
- Kuiva‑aine on valkoista.
- Suspensio on opalisoivaa, väritöntä tai vaalean rusehtavaa nestettä.
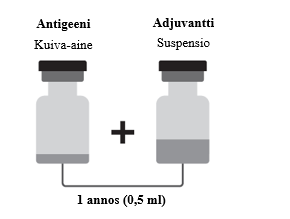
Yhdessä Arexvy‑pakkauksessa on:
- Kuiva‑aine (antigeeni) yhtä annosta varten injektiopullossa
- Suspensio (adjuvantti) yhtä annosta varten injektiopullossa
Arexvy on saatavilla pakkauksessa, jossa on 1 injektiopullo kuiva‑ainetta ja 1 injektiopullo suspensiota, sekä pakkauksessa, jossa on 10 injektiopulloa kuiva‑ainetta ja 10 injektiopulloa suspensiota.
Kaikkia pakkauskokoja ei välttämättä ole myynnissä.
Myyntiluvan haltija ja valmistaja
GlaxoSmithKline Biologicals SA
Rue de l’Institut 89
1330 Rixensart
Belgia
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
Suomi/Finland
GlaxoSmithKline Oy
Puh/Tel: + 358 10 30 30 30
Tämä pakkausseloste on tarkistettu viimeksi 02/2026
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla https://www.ema.europa.eu .
Ohjeet terveydenhuollon ammattilaiselle
Seuraavat tiedot on tarkoitettu vain terveydenhuollon ammattilaisille:
Arexvy‑pakkauksessa on kuiva‑ainetta (antigeenia) sisältävä injektiopullo, jossa on kellertävänvihreä irti napsautettava korkki, ja suspensiota (adjuvanttia) sisältävä injektiopullo, jossa on ruskea irti napsautettava korkki.
Kuiva‑aine ja suspensio on saatettava käyttökuntoon ennen antoa.
Kuiva‑aine ja suspensio on tarkastettava silmämääräisesti vieraiden hiukkasten ja/tai ulkonäkömuutosten varalta. Jos jompaakumpaa näistä todetaan, rokotetta ei saa saattaa käyttökuntoon.
Arexvyn valmistelu
Arexvy on saatettava käyttökuntoon ennen antoa.
- Vedä suspensiota sisältävän injektiopullon koko sisältö ruiskuun.
- Lisää ruiskun koko sisältö injektiopulloon, jossa kuiva‑aine on.
- Pyöritä injektiopulloa varovasti, kunnes kuiva‑aine on liuennut kokonaan.
Käyttökuntoon saatettu rokote on opalisoivaa, väritöntä tai vaaleanrusehtavaa nestettä.
Käyttökuntoon saatettu rokote on tarkastettava silmämääräisesti vieraiden hiukkasten ja/tai ulkonäkömuutosten varalta. Jos jompaakumpaa näistä todetaan, rokotetta ei saa antaa.
Valmisteen on osoitettu säilyvän käytön aikana kemiallisesti ja fysikaalisesti stabiilina 4 tuntia 2–8 °C:n lämpötilassa tai huoneenlämmössä (enintään 25 °C).
Mikrobiologiselta kannalta valmiste on käytettävä välittömästi. Jos valmistetta ei käytetä välittömästi, käytönaikaiset säilytysajat ja käyttöä edeltävät säilytysolosuhteet ovat käyttäjän vastuulla. Säilytysaika saa olla enintään 4 tuntia.
Ennen antoa
- Vedä 0,5 ml käyttökuntoon saatettua rokotetta ruiskuun.
- Vaihda neula – rokotteen antoon on käytettävä uutta neulaa.
Anna rokote lihakseen.
Käyttämätön lääkevalmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.