Pakkausseloste
AMGEVITA injektionsvätska, lösning i förfylld injektionspenna 40 mg
Tilläggsinformation
AMGEVITA 40 mg injektionsvätska, lösning i förfylld injektionspenna
adalimumab
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Din läkare kommer även ge dig ett Patientkort, som innehåller viktig säkerhetsinformation som du måste vara medveten om innan AMGEVITA ges till dig och under behandling med AMGEVITA. Behåll detta Patientkort.
- Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information (se avsnitt Eventuella biverkningar).
I denna bipacksedel finns information om följande
- Vad AMGEVITA är och vad det används för
- Vad du behöver veta innan du använder AMGEVITA
- Hur du använder AMGEVITA
- Eventuella biverkningar
- Hur AMGEVITA ska förvaras
- Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
AMGEVITA innehåller den aktiva substansen adalimumab, ett läkemedel som påverkar immunsystemet (immunförsvaret).
AMGEVITA är avsett för behandling av de inflammatoriska sjukdomarna som beskrivs nedan:
- Reumatoid artrit (ledgångsreumatism)
- Polyartikulär juvenil idiopatisk artrit (barnreumatisk ledsjukdom)
- Entesitrelaterad artrit (muskel-, senfästes- och ledinflammation)
- Ankyloserande spondylit (reumatisk sjukdom med inflammation i ryggradens leder)
- Axial spondylartrit utan radiografiska tecken på ankyloserande spondylit (reumatisk sjukdom med inflammation i axeln)
- Psoriasisartrit
- Plackpsoriasis
- Hidradenitis suppurativa (inflammation i huden)
- Crohns sjukdom (inflammation i tarmen)
- Ulcerös kolit (inflammation i tjocktarmen)
- Icke-infektiös uveit (uveit utan infektion, inflammation i ögat)
Den aktiva substansen i AMGEVITA, adalimumab, är en monoklonal antikropp från människa. Monoklonala antikroppar är proteiner som fäster vid ett specifikt mål.
Målet för adalimumab är ett protein som kallas tumörnekrosfaktor (TNFα), som är involverat i immunförsvaret och finns i förhöjda nivåer vid de inflammatoriska sjukdomar som anges ovan. Genom att binda till TNFα, kan AMGEVITA minska den inflammatoriska processen vid dessa sjukdomar.
Reumatoid artrit
Reumatoid artrit är en inflammatorisk sjukdom i lederna.
AMGEVITA används för att behandla reumatoid artrit hos vuxna. Om du har måttlig till svår aktiv reumatoid artrit, kommer du i regel först att få andra sjukdomsmodifierande läkemedel, såsom metotrexat. Om du inte svarar tillräckligt väl på dessa läkemedel, kan läkaren sätta in AMGEVITA för att behandla din reumatoid artrit.
AMGEVITA kan också användas för att behandla svår, aktiv och progressiv (fortskridande) reumatoid artrit som inte tidigare behandlats med metotrexat.
AMGEVITA bromsar förstörelsen av brosk och skelett i lederna som sjukdomen orsakar och kan därför öka din förmåga att utföra dagliga aktiviteter.
AMGEVITA används vanligen tillsammans med metotrexat. Om din läkare beslutar att metotrexat är olämpligt, kan AMGEVITA ges ensamt.
Polyartikulär juvenil idiopatisk artrit och entesitrelaterad artrit
Polyartikulär juvenil idiopatisk artrit och entesitrelaterad artrit är inflammatoriska sjukdomar i lederna som vanligen uppträder första gången i barndomen.
AMGEVITA används för att behandla polyartikulär juvenil idiopatisk artrit hos patienter 2 år och äldre samt entesitrelaterad artrit hos patienter 6 år och äldre. Du kanske först får andra sjukdomsmodifierande läkemedel, såsom metotrexat. Om dessa läkemedel inte hjälper tillräckligt så kommer du att få AMGEVITA för att behandla din polyartikulära juvenila idiopatiska artrit eller entesitrelaterade artrit.
Ankyloserande spondylit och axial spondylartrit utan radiografiska tecken på ankyloserande spondylit.
Ankyloserande spondylit och axial spondylartrit utan radiografiska tecken på ankyloserande spondylit är inflammatoriska sjukdomar i ryggraden.
AMGEVITA används för att behandla ankyloserande spondylit och axial spondylartrit utan radiografiska förändringar av ankyloserande spondylit hos vuxna. Om du har ankyloserande spondylit eller axial spondylartrit utan radiografiska tecken på ankyloserande spondylit så kommer du först att få andra läkemedel. Om dessa läkemedel inte hjälper tillräckligt så kommer du att få AMGEVITA för att minska tecken och symtom på din sjukdom.
Psoriasisartrit
Psoriasisartrit är en inflammation i lederna som beror på sjukdomen psoriasis.
AMGEVITA används för att behandla psoriasisartrit hos vuxna. AMGEVITA bromsar skadan på brosk och ben i leden orsakad av sjukdomen, och att förbättra den fysiska funktionen.
Plackpsoriasis hos vuxna och barn
Plackpsoriasis är en sjukdom som orsakar röda, flagiga och torra plack på huden som täcks av silvriga fjäll. Plackpsoriasis kan också involvera naglarna, som då kan smula sönder, bli tjockare och lyfta från nagelbädden, vilket kan vara smärtsamt. Psoriasis tros orsakas av en störning i kroppens immunsystem som leder till en ökad produktion av hudceller.
AMGEVITA används för att behandla måttlig till svår plackpsoriasis hos vuxna. AMGEVITA används även för att behandla svår plackpsoriasis hos barn och ungdomar 4–17 år för vilka lokal behandling och ljusbehandling inte har fungerat eller inte är lämpligt.
Hidradenitis suppurativa hos vuxna och ungdomar
Hidradenitis suppurativa (ibland kallat acne inversa) är en kronisk och ofta smärtsam inflammatorisk hudsjukdom. Symtomen kan vara ömma noduli (knölar) och abscesser (bölder) som kan läcka var. Sjukdomen påverkar vanligen specifika områden av huden, t.ex. under brösten, armhålorna, innerlåren, ljumsken och rumpan. Ärrbildning kan också uppstå i de påverkade områdena.
AMGEVITA används för att behandla hidradenitis suppurativa hos vuxna och ungdomar från 12 års ålder. AMGEVITA kan minska antalet knölar och bölder du har samt smärtan som ofta är kopplad till sjukdomen. Du kanske först får andra läkemedel. Om du inte svarar tillräckligt på dessa läkemedel kommer du att få AMGEVITA.
Crohns sjukdom hos vuxna och barn
Crohns sjukdom är en inflammatorisk sjukdom i matsmältningssystemet.
AMGEVITA används för att behandla Crohns sjukdom hos vuxna och barn 6-17 år. Om du har Crohns sjukdom kommer du först att få andra läkemedel. Om dessa läkemedel inte hjälper tillräckligt kommer du att få AMGEVITA för att minska tecken och symtom på din Crohns sjukdom.
Ulcerös kolit hos vuxna och barn
Ulcerös kolit är en inflammatorisk sjukdom i tjocktarmen.
AMGEVITA används för att behandla måttlig till svår ulcerös kolit hos vuxna och barn 6−17 år. Om du har ulcerös kolit kan du först få andra läkemedel. Om dessa läkemedel inte hjälper tillräckligt så kommer du att få AMGEVITA för att minska tecken och symtom från din sjukdom.
Uveit utan infektion hos vuxna och barn
Uveit utan infektion är en inflammatorisk sjukdom som påverkar vissa delar av ögat.
AMGEVITA används för att behandla
- Vuxna med uveit utan infektion där inflammation påverkar bakre delen av ögat.
- Barn från 2 års ålder med kronisk uveit utan infektion där inflammationen påverkar främre delen av ögat.
Inflammationen kan leda till försämrad syn och/eller förekomst av floaters i ögat (svarta prickar eller stripiga linjer som rör sig över synfältet). AMGEVITA fungerar genom att minska denna inflammation.
Vad du behöver veta innan produkten används
Använd inte AMGEVITA
- Om du är allergisk mot adalimumab eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
- Om du har en allvarlig infektion, inklusive tuberkulos, sepsis (infektion i blodet) eller andra opportunistiska infektioner (ovanliga infektioner förknippade med ett försvagat immunsystem) (se ”Varningar och försiktighet”). Det är viktigt att du talar om för din läkare om du har symtom på infektioner, t.ex. feber, sår, trötthetskänsla, tandproblem.
- Om du har måttlig eller svår hjärtsvikt. Det är viktigt att berätta för din läkare om du har eller har haft en allvarlig hjärtåkomma (se ”Varningar och försiktighet”).
Varningar och försiktighet
Tala med läkare eller apotekspersonal innan du använder AMGEVITA:
Allergisk reaktion
- Om du får allergiska reaktioner med symtom såsom trånghetskänsla i bröstet, väsande andning, yrsel, svullnad eller utslag, ska du sluta injicera AMGEVITA och kontakta din läkare omgående, eftersom dessa reaktioner i sällsynta fall kan vara livshotande.
Infektioner
- Om du har någon infektion, inklusive kroniska infektioner eller lokala infektioner (t.ex. bensår) måste du rådgöra med din läkare innan du börjar med AMGEVITA. Om du är osäker, kontakta din läkare.
- Du kanske lättare får infektioner medan du får behandling med AMGEVITA. Denna risk kan öka ifall du har försämrad lungfunktion. Dessa infektioner kan vara allvarliga och inkludera tuberkulos, infektioner orsakade av virus, svamp, parasiter eller bakterier, eller andra opportunistiska infektioner och sepsis som i sällsynta fall kan bli livshotande. Det är viktigt att berätta för din läkare om du får symtom såsom feber, sår, trötthetskänsla eller tandbesvär. Din läkare kan råda dig att tillfälligt sluta använda AMGEVITA.
Tuberkulos
- Eftersom fall av tuberkulos har rapporterats hos patienter som behandlats med adalimumab, kommer läkaren att undersöka dig för tecken och symtom på tuberkulos innan behandling med AMGEVITA påbörjas. Denna inkluderar en omfattande sjukdomshistoria och lämpliga screeningundersökningar (t.ex. lungröntgen och en tuberkulintest). Utförandet och resultaten av dessa tester ska anges på ditt patientkort. Det är mycket viktigt att du berättar för din läkare om du någonsin har haft tuberkulos, eller om du har varit in nära kontakt med någon som har haft tuberkulos.
- Tuberkulos kan utvecklas under behandling även om du har fått förebyggande behandling mot tuberkulos.
- Om symtom på tuberkulos (ihållande hosta, viktminskning, apati, lätt feber), eller om någon annan infektion uppkommer under eller efter behandlingen, måste du genast berätta detta för din läkare.
Resor / återkommande infektion
- Tala om för din läkare ifall du bor eller reser i regioner där svampinfektioner såsom histoplasmos, koccidioidomykos eller blastomykos är ständigt närvarande (endemiska).
- Upplys din läkare om du tidigare har haft problem med återkommande infektioner eller andra åkommor som ökar risken för infektioner.
Hepatit B-virus
- Tala om för din läkare ifall du är bärare av hepatit B virus (HBV), ifall du har en aktiv HBV- infektion eller om du tror att du löper risk att få HBV. Din läkare bör testa dig för Hepatit B. AMGEVITA kan orsaka reaktivering av HBV hos personer som bär på detta virus. I vissa sällsynta fall, speciellt ifall du tar andra läkemedel som hämmar immunsystemet, kan reaktivering av HBV vara livshotande.
Personer över 65 år
- Om du är över 65 år kan du vara mer känslig för infektioner då du använder AMGEVITA. Du och din läkare ska vara särskilt uppmärksamma på tecken på infektion då du behandlas med AMGEVITA. Det är viktigt att tala om för din läkare om du får symtom på infektion, såsom feber, sår, trötthetskänsla eller tandbesvär.
Operation eller tandingrepp
- Om du snart ska genomgå en operation eller ett tandingrepp, informera din läkare om att du tar AMGEVITA. Din läkare kan råda dig att tillfälligt sluta använda AMGEVITA.
Demyelinerande sjukdom
- Om du har eller utvecklar en demyelinerande sjukdom såsom multipel skleros (MS), kommer din läkare att göra en bedömning om du kan få eller ska fortsätta behandlas med AMGEVITA. Berätta omedelbart för din läkare om du får symtom såsom synförändringar , svaghet i armar eller ben, eller domningar eller stickningar någonstans på kroppen.
Vaccinationer
- Vissa vacciner innehåller levande men försvagade former av sjukdomsalstrande bakterier eller virus som kan orsaka infektioner och ska inte ges under behandlingen med AMGEVITA. Kontrollera med din läkare innan du vaccineras. Det rekommenderas att barn, om möjligt, vaccineras enligt gällande riktlinjer för allmän vaccination före behandling med AMGEVITA påbörjas.
- Om du har fått AMGEVITA under din graviditet, så kan ditt nyfödda barn ha en ökad risk för att få en sådan infektion i upp till fem månader efter den sista dosen du fick under graviditeten. Det är viktigt att du berättar för barnläkaren och annan sjukvårdspersonal om att du använde AMGEVITA under din graviditet så att de kan bestämma när ditt nyfödda barn ska vaccineras.
Hjärtsvikt
- Om du har mild hjärtsvikt och behandlas med AMGEVITA, måste dina hjärtproblem övervakas noggrant av din läkare. Det är viktigt att tala om för din läkare om du har eller har haft en allvarlig hjärtåkomma. Om du utvecklar nya symtom eller om dina symtom på hjärtsvikt förvärras (t.ex. andfåddhet eller svullna fötter), måste du kontakta din läkare omedelbart. Din läkare kommer att avgöra om du bör få AMGEVITA.
Feber, blåmärken, blödning eller blekhet
- Hos vissa patienter klarar inte kroppen att tillverka tillräckligt antal blodceller som hjälper din kropp att bekämpa infektioner eller stoppa blödningar. Om du får feber som inte går ner, får blåmärken eller blöder lätt eller ser mycket blek ut bör du omedelbart ringa din läkare. Din läkare kan då besluta att behandlingen ska avbrytas.
Cancer
- Mycket sällsynta fall av vissa cancertyper har förekommit hos barn och vuxna som behandlas med adalimumab eller andra TNF-blockerare. Patienter med svårare reumatoid artrit som har haft sjukdomen under längre tid kan ha en förhöjd risk att utveckla lymfom (cancer som påverkar lymfsystemet) och leukemi (cancer som påverkar blod och benmärg).
- Om du behandlas med AMGEVITA så kanske risken ökar för att utveckla lymfom, leukemi eller annan cancertyp. Vid sällsynta tillfällen har en specifik och allvarlig typ av lymfom observerats hos patienter som använder adalimumab. Vissa av dessa patienter behandlades också med azatioprin eller 6-merkaptopurin. Berätta för din läkare om du tar azatioprin eller 6-merkaptopurin tillsammans med AMGEVITA.
- Även fall av icke-melanom hudcancer har förekommit hos patienter som behandlas med adalimumab. Om nya hudsår uppstår under eller efter behandling eller ifall existerande hudsår ändrar utseende, berätta detta för din läkare.
- Det har förekommit andra cancerformer än lymfom, hos de patienter med en särskild lungsjukdom kallad kronisk obstruktiv lungsjukdom (KOL) och som behandlas med andra TNF-blockerare. Om du har KOL, eller är storrökare, ska du diskutera med din läkare huruvida det är lämpligt att behandla dig med TNF-blockerare.
Autoimmun sjukdom
- I sällsynta fall kan behandling med AMGEVITA ge ett lupusliknande syndrom. Kontakta din läkare om symtom som ihållande, oförklarliga utslag, feber, ledsmärta eller trötthet uppstår.
För att lättare kunna spåra detta läkemedel bör din läkare eller apotekspersonal i din patientjournal notera namnet och lot-numret på det läkemedel som du har fått. Du kan också vilja notera dessa uppgifter för att ha till hands om du någon gång blir tillfrågad om denna information.
Barn och ungdomar
- Vaccinationer: om möjligt så ska ditt barn ha fått alla vaccinationer innan AMGEVITA börjar användas.
- Ge inte AMGEVITA till barn under 2 år med polyartikulär juvenil idiopatisk artrit.
- Ge inte AMGEVITA till barn under 4 år med plackpsoriasis.
- Ge inte AMGEVITA till barn under 6 år med Crohns sjukdom eller ulcerös kolit.
Andra läkemedel och AMGEVITA
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel.
AMGEVITA kan tas tillsammans med metotrexat eller vissa sjukdomsmodifierande anti-reumatiska medel (sulfasalazin, hydroxiklorokin, leflunomid och guldberedningar för injektion), steroider eller smärtstillande läkemedel, inklusive icke-steroida anti-inflammatoriska läkemedel (NSAID).
Du ska inte använda AMGEVITA tillsammans med läkemedel som innehåller de aktiva substanserna, anakinra eller abatacept på grund av den ökade risken för allvarliga infektioner. Om du har frågor, vänligen kontakta din läkare.
Graviditet och amning
- Du bör överväga att använda adekvat preventivmetod för att förhindra graviditet när du använder AMGEVITA och fortsätta använda det i minst 5 månader efter den sista behandlingen med AMGEVITA.
- Om du är gravid, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare innan du använder detta läkemedel.
- AMGEVITA ska endast användas under graviditet om det behövs.
- Enligt en graviditetsstudie fanns ingen ökad risk för fosterskador när mamman hade fått AMGEVITA under graviditeten jämfört med mammor med samma sjukdom som inte använt AMGEVITA.
- AMGEVITA kan användas under amning.
- Om du får AMGEVITA under din graviditet, så kan ditt nyfödda barn ha en ökad risk för att få en infektion.
- Det är viktigt att du berättar för barnläkaren och annan sjukvårdspersonal om att du använde AMGEVITA under din graviditet innan ditt nyfödda barn ska vaccineras. För mer information om vacciner se avsnittet ”Varningar och försiktighet”.
Körförmåga och användning av maskiner
AMGEVITA kan ha en liten påverkan på din förmåga att köra bil, cykla eller använda maskiner. En känsla av att rummet snurrar (yrsel) samt synstörningar kan inträffa när AMGEVITA används.
AMGEVITA innehåller natrium
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per 0,8 ml dos, d.v.s. är näst intill ”natriumfritt”.
Hur produkten används
Använd alltid detta läkemedel enligt läkarens eller apotekspersonalens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
Vuxna med reumatoid artrit, psoriasisartrit, ankyloserande spondylit eller axial spondylartrit utan radiografiska bevis på ankyloserande spondylit
AMGEVITA injiceras under huden (subkutan användning). Den vanliga doseringen för vuxna med reumatoid artrit, ankyloserande spondylit, axial spondylartrit utan radiografiska tecken på ankyloserande spondylit och för patienter med psoriasisartrit är 40 mg givet varannan vecka som en enkel dos.
Vid reumatoid artrit används metotrexat tillsammans med AMGEVITA. Om din läkare beslutar att metotrexat inte är lämpligt kan AMGEVITA användas ensamt.
Om du har reumatoid artrit och du inte får metotrexat tillsammans med AMGEVITA så kan din läkare besluta att ge dig 40 mg varje vecka eller 80 mg varannan vecka.
Barn, ungdomar och vuxna med polyartikulär juvenil idiopatisk artrit
Barn, ungdomar och vuxna från 2 års ålder som väger 30 kg eller mer
Den rekommenderade doseringen av AMGEVITA är 40 mg varannan vecka.
Barn, ungdomar och vuxna med entesitrelaterad artrit
Barn, ungdomar och vuxna från 6 års ålder som väger 30 kg eller mer
Den rekommenderade doseringen av AMGEVITA är 40 mg varannan vecka.
Vuxna med plackpsoriasis
Den vanliga dosen för vuxna med plackpsoriasis är en startdos på 80 mg (som två 40 mg injektioner på en dag), som följs av 40 mg som ges varannan vecka och som börjar en vecka efter startdosen. Du ska fortsätta injicera AMGEVITA så länge som din läkare ordinerar detta. Beroende på hur du svarar på behandlingen kan din läkare öka dosen till 40 mg varje vecka eller 80 mg varannan vecka.
Barn och ungdomar med plackpsoriasis
Barn och ungdomar 4–17 år som väger 30 kg eller mer
Den rekommenderade doseringen av AMGEVITA är en startdos på 40 mg följt, av 40 mg en vecka senare. Därefter är den vanliga dosen 40 mg varannan vecka.
Vuxna med hidradenitis suppurativa
Den vanliga dosen för hidradenitis suppurativa är en startdos på 160 mg (som fyra 40 mg injektioner på en dag eller två 40 mg injektioner per dag två dagar i följd), följt av 80 mg (som två 40 mg injektioner på en dag) två veckor senare. Efter ytterligare två veckor fortsätter behandlingen med en dos på 40 mg varje vecka eller 80 mg varannan vecka, enligt din läkares ordination. Det rekommenderas att du använder en bakteriedödande lösning dagligen på de områden som är påverkade.
Ungdomar med hidradenitis suppurativa 12–17 år som väger 30 kg eller mer
Den rekommenderade doseringen av AMGEVITA är en startdos på 80 mg (som två 40 mg injektioner på samma dag) följt av 40 mg varannan vecka med start en vecka senare. Om du inte svarar tillräckligt på AMGEVITA 40 mg varannan vecka kan din läkare öka dosen till 40 mg varje vecka eller 80 mg varannan vecka.
Det rekommenderas att du dagligen använder en bakteriedödande lösning på de påverkade områdena.
Vuxna med Crohns sjukdom
Den vanliga doseringen för Crohns sjukdom är 80 mg (som två 40 mg injektioner på en dag) initialt följt av 40 mg varannan vecka två veckor senare. Ifall en snabbare förbättring är nödvändig, kan din läkare ge dig en startdos på 160 mg vecka 0 (som fyra 40 mg injektioner på en dag eller två 40 mg injektioner per dag två dagar i följd), följt av 80 mg (som två 40 mg injektioner på en dag) två veckor senare och därefter 40 mg varannan vecka. Beroende på hur du svarar, kanske din läkare ökar dosen till 40 mg varje vecka eller 80 mg varannan vecka.
Barn och ungdomar med Crohns sjukdom
Barn och ungdomar 6–17 år som väger mindre än 40 kg
Den vanliga doseringen är 40 mg initialt följt av 20 mg två veckor senare. Om ett snabbare svar krävs så kan ditt barns läkare förskriva en startdos av 80 mg (som två 40 mg injektioner på en dag) följt av 40 mg två veckor senare.
Därefter är den vanliga dosen 20 mg varannan vecka. Beroende på hur ditt barn reagerar så kan ditt barns läkare öka doseringen till 20 mg varje vecka.
Den förfyllda injektionspennan med 40 mg kan inte användas för att ge dosen 20 mg. En 20 mg förfylld AMGEVITA-spruta finns dock för att ge dosen 20 mg.
Barn och ungdomar 6–17 år som väger 40 kg eller mer
Den vanliga doseringen är 80 mg (som två 40 mg injektioner på en dag) initialt följt av 40 mg två veckor senare. Om ett snabbare svar krävs så kan ditt barns läkare förskriva en startdos av 160 mg (som fyra 40 mg injektioner på en dag eller som två 40 mg injektioner per dag under två efterföljande dagar) följt av 80 mg (som två 40 mg injektioner på en dag) två veckor senare.
Därefter är den vanliga dosen 40 mg varannan vecka. Beroende på hur ditt barn reagerar så kan ditt barns läkare öka dosen till 40 mg varje vecka eller 80 mg varannan vecka.
Vuxna med ulcerös kolit
Den vanliga doseringen med AMGEVITA för vuxna med ulcerös kolit är initialt 160 mg (som fyra 40 mg injektioner under en dag eller som två 40 mg injektioner per dag under två på varandra följande dagar) följt av 80 mg (som två 40 mg injektioner på en dag) två veckor senare och därefter 40 mg varannan vecka. Beroende på hur du svarar kan läkaren öka dosen till 40 mg varje vecka eller 80 mg varannan vecka.
Barn och ungdomar med ulcerös kolit
Barn och ungdomar från 6 års ålder som väger mindre än 40 kg
Den vanliga doseringen av AMGEVITA är 80 mg (som två 40 mg injektioner samma dag) initialt, följt av 40 mg (som en 40 mg injektion) två veckor senare. Därefter är den vanliga dosen 40 mg varannan vecka.
Patienter som fyller 18 år medan de står på 40 mg varannan vecka ska fortsätta med sin ordinerade dos.
Barn och ungdomar från 6 års ålder som väger 40 kg eller mer
Den vanliga doseringen av AMGEVITA är 160 mg (som fyra 40 mg injektioner samma dag eller två 40 mg injektioner per dag under två dagar i följd) initialt, följt av 80 mg (som två 40 mg injektioner samma dag) två veckor senare. Därefter är den vanliga dosen 80 mg varannan vecka.
Patienter som fyller 18 år medan de står på 80 mg varannan vecka ska fortsätta med sin ordinerade dos.
Vuxna med uveit utan infektion
Den vanliga doseringen för vuxna med uveit utan infektion är en startdos på 80 mg (som två 40 mg injektioner på samma dag), följt av 40 mg varannan vecka med början en vecka efter startdosen. Du ska fortsätta injicera AMGEVITA så länge som din läkare ordinerar detta.
Vid uveit utan infektion kan kortikosteroider, eller andra läkemedel som påverkar immunsystemet, fortsätta att tas under behandling med AMGEVITA. AMGEVITA kan även ges ensamt.
Barn och ungdomar från 2 års ålder med kronisk uveit utan infektion
Barn och ungdomar från 2 års ålder som väger mindre än 30 kg
Den vanliga doseringen av AMGEVITA är 20 mg varannan vecka tillsammans med metotrexat.
Läkare kan också ordinera en startdos på 40 mg som ges en vecka före start av den vanliga dosen.
Den förfyllda injektionspennan med 40 mg kan inte användas för att ge dosen 20 mg. En 20 mg förfylld AMGEVITA-spruta finns dock för att ge dosen 20 mg.
Barn och ungdomar från 2 års ålder som väger 30 kg eller mer
Den vanliga doseringen av AMGEVITA är 40 mg varannan vecka tillsammans med metotrexat.
Läkare kan också ordinera en startdos på 80 mg som ges en vecka före start av den vanliga dosen.
Administreringssätt och administreringsväg
AMGEVITA ges via en injektion under huden (subkutan injektion).
Utförliga anvisningar om hur AMGEVITA injiceras finns i avsnittet ”Bruksanvisning”.
Om du använt mer AMGEVITA än du borde
Om du råkar injicera AMGEVITA oftare än din läkare eller apotekspersonal har ordinerat, kontakta din läkare eller apotekspersonal och berätta att du har tagit för mycket. Ta alltid med dig detta läkemedels yttre kartong, även om den är tom.
Om du har glömt att använda AMGEVITA
Om du glömmer bort att ge dig själv en injektion, ska du ta en dos av AMGEVITA så snart du kommer ihåg detta. Ta sedan din nästa dos på den bestämda dagen som du skulle ha gjort, om du inte hade glömt bort en dos.
Om du slutar att använda AMGEVITA
Beslutet att sluta använda AMGEVITA ska diskuteras med din läkare. Dina symtom kan återkomma då behandlingen avslutas.
Om du har ytterligare frågor om detta läkemedel, kontakta läkare eller apotek.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar men alla användare behöver inte få dem. De flesta biverkningar är milda till måttliga. Vissa kan emellertid vara allvarliga och kräva behandling. Biverkningar kan uppträda upp till 4 månader efter den sista AMGEVITA-injektionen.
Tala omedelbart om för din läkare om du märker något av följande tecken på allergisk reaktion eller hjärtsvikt:
- allvarlig klåda, nässelutslag eller andra tecken på allergisk reaktion;
- svullet ansikte, svullna händer, fötter;
- ansträngd andning, svårt att svälja;
- andnöd vid ansträngning eller då man ligger ner eller om fötterna svullnar.
Berätta för din läkare så fort som möjligt om du märker något av det följande:
- tecken på infektion såsom feber, illamående, sår, tandproblem, brännande känsla då man kissar;
- svaghets- eller trötthetskänsla;
- hosta;
- stickningar;
- känselbortfall;
- dubbelseende;
- arm eller bensvaghet;
- tecken på hudcancer såsom en bula eller ett öppet sår som inte läker;
- tecken och symtom på blodsjukdomar såsom långvarig feber, blåmärken, blödning, blekhet.
Symtomen som beskrivs ovan kan vara tecken på biverkningar som beskrivs nedan och som har observerats vid användning av adalimumab.
Mycket vanliga (kan förekomma hos fler än 1 av 10 användare)
- reaktioner på injektionsstället (inklusive smärta, svullnad, rodnad eller klåda);
- luftvägsinfektioner (inklusive förkylning, rinnande näsa, bihåleinflammation, lunginflammation);
- huvudvärk;
- buksmärta;
- illamående och kräkning;
- hudutslag;
- muskel- och skelettsmärta.
Vanliga (kan förekomma hos upp till 1 av 10 användare)
- allvarliga infektioner (inklusive blodförgiftning och influensa);
- infektioner i tarmarna (inklusive gastroenterit);
- hudinfektioner (inklusive celluliter och bältros);
- öroninfektioner;
- muninfektioner (inklusive tandinfektioner och herpes på läpparna);
- infektioner i könsorganen;
- urinvägsinfektioner;
- svampinfektioner;
- ledinfektioner;
- godartade tumörer;
- hudcancer;
- allergiska reaktioner (inklusive säsongsallergi);
- uttorkning;
- humörsvängningar (inklusive depression);
- oro;
- problem att sova;
- känselstörningar såsom stickningar, myrkrypningar eller domning;
- migrän;
- nervrotskompression (inklusive smärta i korsryggen och bensmärta);
- synstörningar;
- ögoninflammation;
- inflammation i ögonlocket och ögonsvullnad;
- yrsel (känsla av obalans eller att rummet snurrar);
- känsla av att hjärtat slår snabbt;
- högt blodtryck;
- rodnad;
- blödning (blodansamling utanför blodkärlen);
- hosta;
- astma;
- andfåddhet;
- blödning i magtarmkanalen;
- dyspepsi (matsmältningsbesvär, uppblåshet, halsbränna);
- magsyre-reflux (sura uppstötningar);
- torra ögon och torr mun;
- klåda;
- kliande utslag;
- blåmärken;
- hudinflammation (såsom eksem);
- sköra finger- och tånaglar;
- ökad svettning;
- håravfall;
- nytt utbrott av eller förvärrande av psoriasis;
- muskelspasmer;
- blod i urinen;
- njurproblem;
- bröstsmärta;
- ödem (vätskeansamling);
- feber;
- sänkt antal blodplättar (trombocyter) vilket ökar risken för blödning eller blåmärken;
- försämrad läkning.
Mindre vanliga (kan förekomma hos upp till 1 av 100 användare)
- opportunistiska infektioner (vilket inkluderar tuberkulos och andra infektioner som kan uppstå då motståndet mot sjukdomarna är sänkt);
- neurologiska infektioner (inklusive hjärnhinneinflammation orsakad av virus);
- ögoninfektioner;
- bakterieinfektioner;
- divertikulit (inflammation och infektion av tjocktarmen);
- cancer, inklusive cancer som påverkar lymfsystemet (lymfom) och melanom (hudcancer);
- immunrubbningar som kan påverka lungor, hud och lymfkörtlar (oftast som sarkoidos);
- vaskulit (inflammation i blodkärlen);
- skakningar;
- neuropati (nervsjukdom);
- stroke (slaganfall);
- hörselbortfall, ringande öron;
- känsla av att hjärtat slår oregelbundet såsom ett missat hjärtslag;
- hjärtproblem som kan orsaka andfåddhet eller svullna fötter;
- hjärtinfarkt;
- ett bråck i den stora artärväggen, inflammation och koagel i en ven, blockering av ett blodkärl;
- lungsjukdom som ger andfåddhet (inklusive lunginflammation);
- lungemboli (blockering i en lungartär);
- pleural effusion (onormal vätskeansamling mellan lungor och bröstkorg);
- inflammation i bukspottkörteln som orsakar svår smärta i buken och ryggen;
- svårighet att svälja;
- ansiktsödem (vätskeansamling i ansiktet);
- gallblåseinflammation, gallstenar;
- fettlever;
- nattliga svettningar;
- ärr;
- onormalt muskelsönderfall;
- systemisk lupus erythomatosus (inklusive inflammation av huden, hjärtat, lungor, leder och andra organsystem);
- sömnavbrott;
- impotens;
- inflammationer.
Sällsynta (kan förekomma hos upp till 1 av 1 000 användare)
- leukemi (cancer som påverkar blod och benmärg);
- allvarlig allergisk reaktion med chock;
- multipel skleros;
- nervrubbning (såsom ögonnervs-inflammation och Guillain-Barré syndrom som kan orsaka muskelsvaghet, känselrubbningar, stickningar i armar och överkropp);
- hjärtat slutar pumpa;
- lungfibros (ärrbildning i lungan);
- hål på tarmen (hål i tarmväggen);
- hepatit (leverinflammation);
- reaktivering av hepatit B;
- autoimmun hepatit (leverinflammation orsakad av kroppens eget immunsystem);
- kutan vaskulit (inflammation av blodkärlen i huden);
- Stevens-Johnson syndrom (livshotande reaktion med influensaliknande symtom och hudutslag med blåsor);
- ansiktsödem associerad med allergiska reaktioner;
- erytema multiforme (inflammatoriska hudutslag);
- lupus-liknande syndrom (ihållande, oförklarliga utslag, feber, ledsmärta eller trötthet);
- angioödem (lokal svullnad av huden);
- lichenoida hudreaktioner (kliande röd-lila hudutslag).
Ingen känd frekvens (kan inte beräknas från tillgängliga data)
- hepatosplenisk T-cellslymfom (en sällsynt blodcancer som ofta är dödlig);
- Merkel-cellcarcinom (en sorts hudcancer);
- Kaposis sarkom, en sällsynt cancer förknippad med infektion med humant herpesvirus 8. Kaposis sarkom uppträder oftast som purpurfärgade fläckar på huden;
- leversvikt;
- förvärrande av ett tillstånd som kallas dermatomyosit (ser ut som hudutslag och åtföljs av muskelsvaghet);
- viktökning (för de flesta patienter var viktökningen liten).
Vissa biverkningar som observerats med adalimumab kanske inte uppvisar symtom och kan endast påvisas genom blodprover. Dessa inkluderar:
Mycket vanliga (kan förekomma hos fler än 1 av 10 användare)
- låga blodvärden för vita blodceller;
- låga blodvärden för röda blodceller;
- förhöjda lipider i blodet;
- förhöjda leverenzymer.
Vanliga (kan förekomma hos upp till 1 av 10 användare)
- höga blodvärden för vita blodceller;
- låga blodvärden för blodplättar;
- förhöjd urinsyra i blodet;
- avvikande blodvärden för natrium;
- låga blodvärden för kalcium;
- låga blodvärden för fosfat;
- högt blodsocker;
- höga blodvärden för laktatdehydrogenas;
- autoantikroppar närvarande i blodet;
- låga blodvärden för kalium.
Mindre vanliga (kan förekomma hos upp till 1 av 100 användare)
- förhöjda värden av bilirubin (blodprov av levern).
Sällsynta (kan förekomma hos upp till 1 av 1 000 användare)
- låga blodvärden för vita blodceller, röda blodceller och blodplättar.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
Finland
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Sverige
Läkemedelsverket
Box 26
751 03 Uppsala
Webbplats: www.lakemedelsverket.se
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på etiketten och kartongen efter EXP. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras i kylskåp (2°C – 8°C). Får inte frysas.
Förvaras i originalförpackningen. Ljuskänsligt.
En AMGEVITA förfylld injektionspenna kan förvaras vid temperaturer upp till högst 25 °C under högst 14 dagar. Den förfyllda injektionspennan måste då skyddas från ljus och kasseras om den inte används inom 14 dagar.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- Den aktiva substansen är adalimumab. En förfylld injektionspenna innehåller 40 mg adalimumab i 0,8 ml lösning.
- De andra innehållsämnena är isättika, sackaros, polysorbat 80, natriumhydroxid och vatten för injektionsvätskor.
Läkemedlets utseende och förpackningsstorlekar
AMGEVITA är en klar och färglös till något gulaktig lösning.
En förpackning innehåller en, två, fyra eller sex förfyllda injektionspennor för engångsbruk (SureClick).
Innehavare av godkännande för försäljning och tillverkare
Amgen Europe B.V. Minervum 7061 4817 ZK Breda Nederländerna
Innehavare av godkännande för försäljning
Amgen Europe B.V. Minervum 7061 4817 ZK Breda Nederländerna
Tillverkare
Amgen Technology Ireland UC
Pottery Road
Dun Laoghaire
Co Dublin
Irland
Tillverkare
Amgen NV
Telecomlaan 5-7
1831 Diegem
Belgien
Kontakta ombudet för innehavaren av godkännandet för försäljning om du vill veta mer om detta läkemedel:
Finland
Orion Pharma
Tel: +358 10 4261
Sverige
Amgen AB
Tel: +46 (0)8 6951100
Denna bipacksedel ändrades senast maj 2024.
Övriga informationskällor
Ytterligare information om detta läkemedel finns på Europeiska läkemedelsmyndighetens webbplats http://www.ema.europa.eu.
Direktiv för användaren
Bruksanvisning: AMGEVITA SureClick förfylld injektionspenna för engångsbruk För subkutan användning | |
| Illustration av de olika delarna | |
| Före användning | Efter användning |
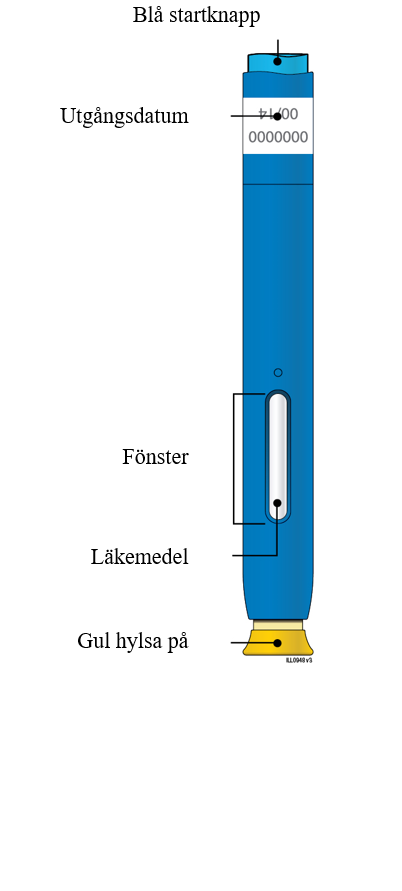 | 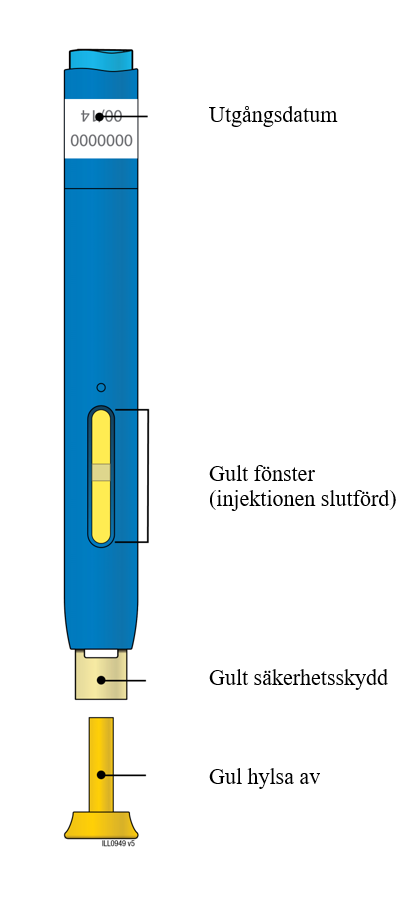 |
| Viktigt! Nålen är inuti | |
| Viktigt | |
| Läs följande viktiga information innan du använder en AMGEVITA förfylld injektionspenna: | |
| Användning av AMGEVITA förfyllda injektionspennor | |
| ● | Det är viktigt att du inte försöker ge dig själv en injektion såvida inte du eller din vårdare inte har fått anvisningar. |
| ● | Använd inte AMGEVITA förfylld injektionspenna om den har tappats på en hård yta. Injektionspennan kan ha skadats även om du inte kan se några sprickor. Använd en ny AMGEVITA förfylld injektionspenna. |
| Steg 1: Förbered |
| A. | Ta fram en AMGEVITA förfylld injektionspenna från förpackningen. |
Lyft försiktigt upp den förfyllda injektionspennan rakt upp från lådan. Ställ tillbaka originalförpackningen med oanvända injektionspennor i kylen. Låt den förfyllda injektionspennan ligga i rumstemperatur i 15 till 30 minuter innan du injicerar för att injektionen ska bli behagligare. | |
| ● | Lägg inte tillbaka den förfyllda injektionspennan i kylskåpet när den har antagit rumstemperatur. |
| ● | Försök inte värma den förfyllda injektionspennan med hjälp av någon värmekälla som varmt vatten eller mikrovågsugn. |
| ● | Skaka inte den förfyllda injektionspennan. |
| ● | Ta inte av den gula hylsan från den förfyllda injektionspennan ännu. |
| B. | Kontrollera AMGEVITA förfylld injektionspenna. |
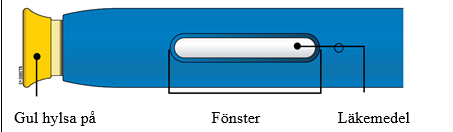 | |
| Kontrollera att läkemedlet i fönstret är klart och färglöst till något gulaktigt. | |
| ● | Använd inte den förfyllda injektionspennan om: |
| |
| I samtliga fall ska en ny injektionspenna användas. | |
| C. | Samla ihop allt material du behöver för injektionen. |
Tvätta händerna noga med tvål och vatten. Lägg en ny, förfylld injektionspenna på en ren och väl belyst arbetsyta. Du behöver även följande föremål, vilka inte ingår i förpackningen: | |
| ● | Alkoholservetter |
| ● | Bomullstuss eller kompress |
| ● | Plåster |
| ● | Avfallsbehållare för vassa föremål |
 | |
| D. | Välj och tvätta injektionsstället. |
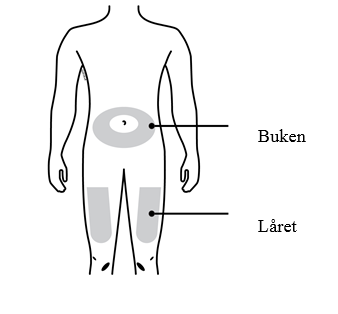 | |
| Du kan använda: | |
| ● | Låret |
| ● | Buken, förutom i en cirkel om 5 centimeter närmast naveln |
| Torka av injektionsstället med en alkoholservett. Låt huden torka. | |
| ● | Vidrör inte detta område igen innan du injicerar. |
| ● | Om du vill använda samma injektionsställe ska du se till att det inte är exakt samma ställe som vid den förra injektionen. |
| |
| ● | Om du har psoriasis ska du undvika att injicera direkt i svullna, tjocka, röda eller fjällande hudområden eller -skador. |
| Steg 2: Gör dig klar |
| E. | Dra den gula hylsan rakt av när du är klar att injicera. |
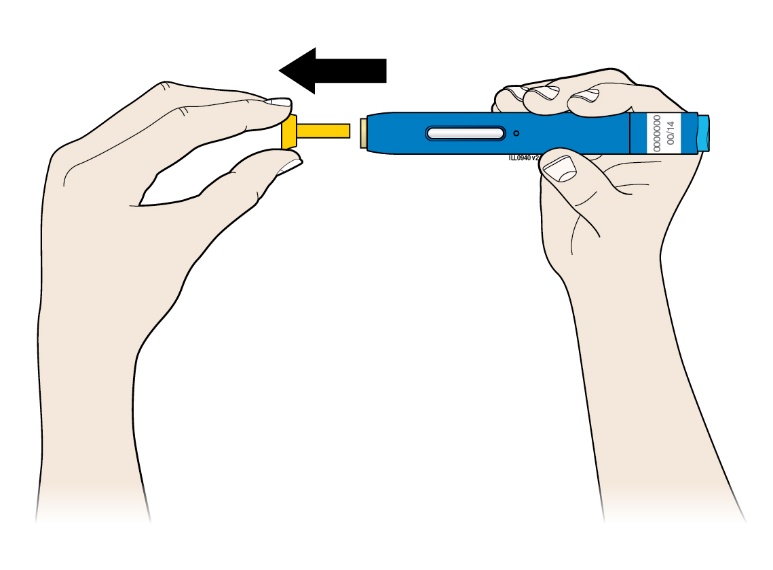 | |
| Det är normalt att se en droppe läkemedel på nålspetsen eller det gula säkerhetsskyddet. | |
| ● | Vrid eller böj inte den gula hylsan. |
| ● | Sätt inte tillbaka den gula hylsan på den förfyllda injektionspennan. |
| ● | Ta inte av den gula hylsan från den förfyllda injektionspennan förrän du är klar att injicera. |
| F. | Sträck ut eller nyp ihop området för injektionsstället för att få en spänd yta. |
| Sträckmetoden | |
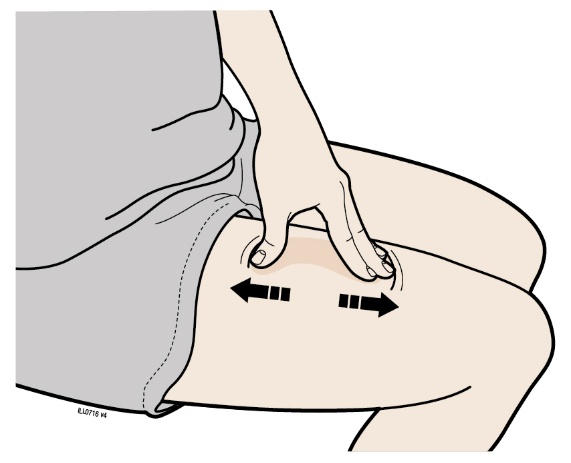 | |
| Sträck bestämt ut huden genom att föra tummen och fingrarna åt motsatt håll för att skapa ett spänt område på ungefär 5 cm. | |
| ELLER | |
| Nypmetoden | |
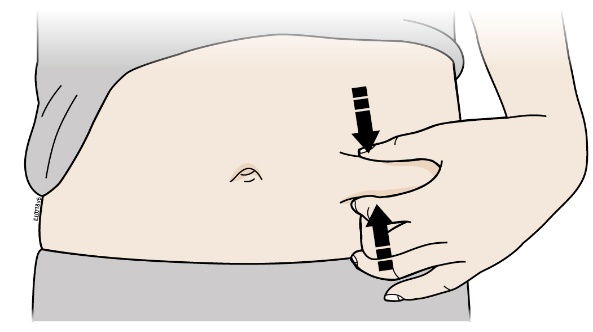 | |
| Nyp med ett fast grepp mellan tummen och fingrarna ihop huden så att ett område på ungefär 5 cm bildas. | |
| Viktigt! Håll huden utsträckt eller ihopnypt tills injektionen är klar. | |
| Steg 3: Injicera |
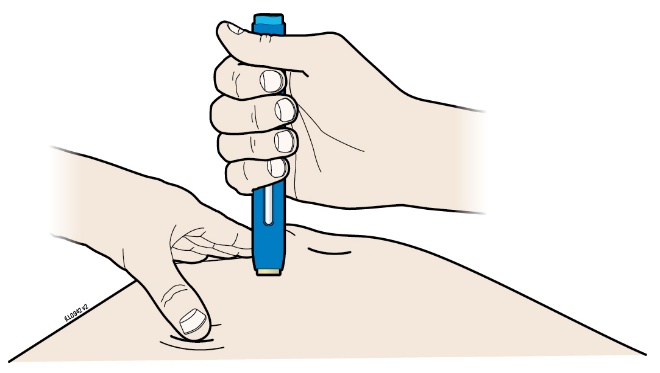
| G. | Fortsatt att hålla huden sträckt eller ihopnypt. Sätt den förfyllda injektionspennan mot huden med 90 graders vinkel. Den gula hylsan ska vara avtagen. |
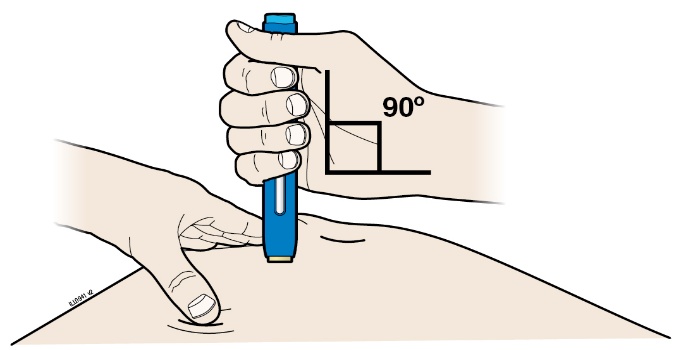 | |
| Viktigt! Rör inte den blå startknappen ännu. | |
| H. | Tryck bestämt ned den förfyllda injektionspennan mot huden tills det tar stopp. |
| |
| Viktigt! Du ska trycka hela vägen ned, men rör inte den blå startknappen förrän du är klar att injicera. | |
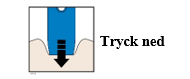
| I. | Tryck på den blå startknappen när du är klar att injicera. Du kommer att höra ett klick. |
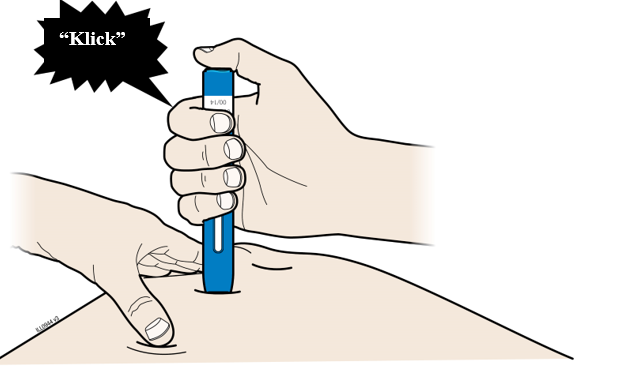 | |
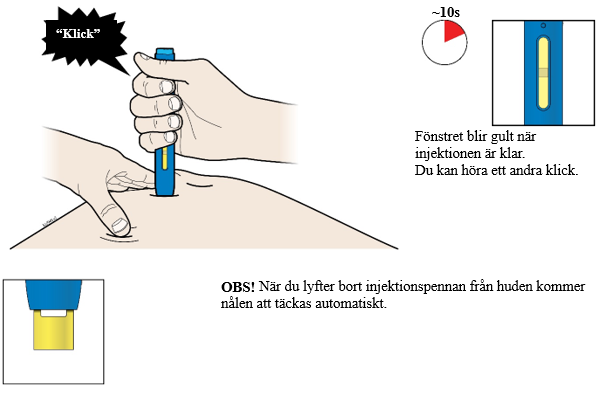
| J. | Fortsätt att trycka ned mot huden. Injektionen kan ta omkring 10 sekunder. |
Viktigt! Om fönstret inte är gult när du lyfter bort injektionspennan eller om det ser ut som om läkemedlet fortfarande injiceras betyder det att du inte har fått en fullständig dos. Kontakta i så fall läkare omedelbart. | |
| Steg 4: Slutför |
| K. | Kasta den använda injektionspennan och gula hylsan. | |
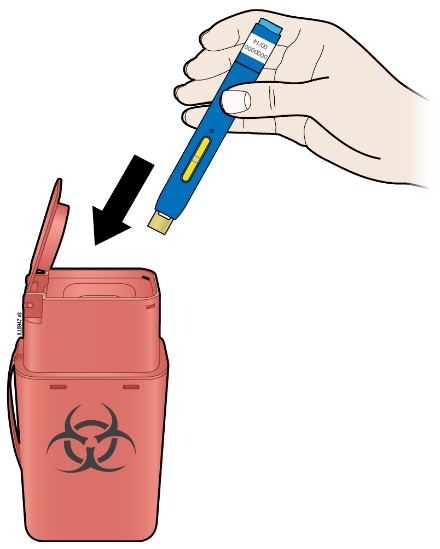 | ||
| ● | Placera omedelbart den använda injektionspennan och nålhylsan i en avfallsbehållare för vassa föremål när du är klar. Släng inte injektionspennan bland hushållsavfallet. | |
| ● | Tala med läkare eller apotekspersonal om hur avfallet ska tas om hand. Det kan finnas lokala riktlinjer för detta. | |
| ● | Återanvänd inte den förfyllda injektionspennan. | |
| ● | Återvinn inte injektionspennan eller avfallsbehållaren och kasta dem inte i hushållsavfallet. | |
| Viktigt: Förvara alltid avfallsbehållaren för vassa föremål utom syn- och räckhåll för barn. | ||
| L. | Undersök injektionsstället. |
| Om det blöder kan du trycka en bomullstuss eller kompress mot injektionsstället. Gnugga inte mot injektionsstället. Sätt på ett plåster om det behövs. | |