LEQVIO injektionsvätska, lösning i förfylld spruta 284 mg
Tilläggsinformation
Leqvio 284 mg injektionsvätska, lösning i förfylld spruta
Förfylld spruta med automatiskt nålskydd
inklisiran
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du får detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare, apotekspersonal eller sjuksköterska.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad Leqvio är och vad det används för
2. Vad du behöver veta innan du får Leqvio
3. Hur du får Leqvio
4. Eventuella biverkningar
5. Hur Leqvio ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Vad Leqvio är och hur det fungerar
Leqvio innehåller den aktiva substansen inklisiran, som sänker nivåerna av LDL-kolesterol (”dåligt” kolesterol). Förhöjda nivåer av LDL-kolesterol kan orsaka problem med hjärtat och blodcirkulationen.
Inklisiran verkar genom att påverka RNA (ett genetiskt material i kroppens celler), så att produktionen av ett protein som kallas PCSK9 begränsas. Detta protein kan öka nivåerna av LDL-kolesterol. När produktionen av proteinet förhindras, hjälper det till att sänka dina LDL-kolesterolnivåer.
Vad Leqvio används för
Leqvio används som tillägg till kolesterolsänkande kost hos vuxna med höga kolesterolvärden i blodet (primär hyperkolesterolemi, inklusive heterozygot familjär och icke-familjär, eller blandad dyslipidemi).
Leqvio ges:
- tillsammans med en statin (en typ av läkemedel för behandling av högt kolesterol), och ibland tillsammans med ytterligare kolesterolsänkande behandling(ar) om den högsta statindosen inte fungerar tillräckligt bra, eller
- ensamt eller tillsammans med andra kolesterolsänkande läkemedel, när statiner inte kan användas eller när patienten inte tål statiner.
Vad du behöver veta innan produkten används
Du ska inte få Leqvio
- om du är allergisk mot inklisiran eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
Varningar och försiktighet
Tala med läkare, apotekspersonal eller sjuksköterska innan du får Leqvio:
- om du får dialys
- om du har en allvarlig leversjukdom
- om du har en allvarlig njursjukdom
Barn och ungdomar
Ge inte detta läkemedel till barn och ungdomar under 18 år. Det finns ingen erfarenhet av att använda läkemedlet i denna åldersgrupp.
Andra läkemedel och Leqvio
Tala om för läkare, apotekspersonal eller sjuksköterska om du använder, nyligen har använt eller kan tänkas använda andra läkemedel.
Graviditet och amning
Om du är gravid eller ammar, tror att du kan vara gravid eller planerar att skaffa barn, rådfråga läkare, apotekspersonal eller sjuksköterska innan du ges detta läkemedel.
Leqvio bör inte användas under graviditet.
Det är ännu inte känt om Leqvio övergår i bröstmjölk hos människa. Din läkare hjälper dig att bestämma om du ska fortsätta amma eller påbörja behandlingen med Leqvio. Din läkare kommer att väga de möjliga fördelarna med behandlingen för dig mot hälsofördelarna och riskerna med amning för ditt barn.
Körförmåga och användning av maskiner
Leqvio förväntas inte påverka förmågan att köra bil eller använda maskiner.
Leqvio innehåller natrium
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per dosenhet d.v.s. är näst intill ”natriumfritt”.
Hur produkten används
Den rekommenderade dosen Leqvio är 284 mg, som ges som en injektion under huden (subkutan injektion). Nästa dos ges efter 3 månader och därefter ges ytterligare doser var 6:e månad.
Innan du börjar med Leqvio ska du ha gått över till kolesterolsänkande kost och troligen tar du även en statin. Du ska fortsätta med den kolesterolsänkande kosten och fortsätta ta statinen hela tiden medan du får Leqvio.
Leqvio är avsett för injektion under huden i buken; alternativa injektionsställen är överarm eller lår. Leqvio kommer att ges till dig av läkare, apotekspersonal eller sjuksköterska (sjukvårdspersonal).
Om du har fått för stor mängd av Leqvio
Du får läkemedlet av läkare, apotekspersonal eller sjuksköterska (sjukvårdspersonal). Det är väldigt osannolikt, men om du skulle få för mycket (en överdos) kommer läkaren eller annan sjukvårdspersonal att kontrollera om du får biverkningar.
Om du har missat en dos Leqvio
Om du har missat ditt besök för att få din Leqvio-injektion, ska du kontakta din läkare, apotekspersonal eller sjuksköterska så snart du kan och boka en ny tid för nästa injektion.
Om du har ytterligare frågor om detta läkemedel, kontakta läkare, apotekspersonal eller sjuksköterska.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Vanliga (kan förekomma hos upp till 1 av 10 personer)
- Reaktioner vid injektionsstället, bland annat smärta, rodnad eller hudutslag.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet. Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på etiketten och kartongen efter ”EXP”. Utgångsdatumet är den sista dagen i angiven månad.
Inga särskilda förvaringsanvisningar. Får ej frysas.
Läkaren, apotekspersonalen eller sjuksköterskan kontrollerar detta läkemedel och kasserar det om det innehåller partiklar.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Läkaren, apotekspersonalen eller sjuksköterskan kasserar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- Den aktiva substansen är inklisiran. Varje förfylld spruta innehåller natriuminklisiran motsvarande 284 mg inklisiran i 1,5 ml lösning. Varje ml innehåller natriuminklisiran motsvarande 189 mg inklisiran.
- Övriga innehållsämnen är vatten för injektionsvätskor, natriumhydroxid (E524) (se avsnitt Vad du behöver veta innan produkten används ”Leqvio innehåller natrium”) och koncentrerad fosforsyra (E338).
Läkemedlets utseende och förpackningsstorlekar
Leqvio 284 mg injektionsvätska, lösning i förfylld spruta är en klar, färglös till ljust gul lösning som är väsentligen fri från partiklar.
Varje förpackning innehåller en förfylld spruta för engångsbruk med automatiskt nålskydd.
Innehavare av godkännande för försäljning
Novartis Europharm Limited
Vista Building
Elm Park, Merrion Road
Dublin 4
Irland
Tillverkare
Novartis Pharmaceutical Manufacturing GmbH
Biochemiestrasse 10
6336 Langkampfen
Österrike
Novartis Pharmaceutical Manufacturing LLC
Verovškova Ulica 57
1000 Ljubljana
Slovenien
Novartis Pharma GmbH
Sophie-Germain-Strasse 10
90443 Nürnberg
Tyskland
Kontakta ombudet för innehavaren av godkännandet för försäljning om du vill veta mer om detta läkemedel:
Suomi/Finland
Novartis Finland Oy
Puh/Tel: +358 (0)10 6133 200
Denna bipacksedel ändrades senast 4.3.2026
Övriga informationskällor
Ytterligare information om detta läkemedel finns på Europeiska läkemedelsmyndighetens webbplats: https://www.ema.europa.eu.
Direktiv för experterna inom hälsovården
Följande uppgifter är endast avsedda för hälso- och sjukvårdspersonal:
Leqvio 284 mg injektionsvätska, lösning i förfylld spruta
Förfylld spruta med automatiskt nålskydd
inklisiran
Sjukvårdspersonal ska läsa produktresumén för fullständig förskrivningsinformation.
Indikation (se avsnitt 4.1 i produktresumén)
Leqvio är avsett för behandling av vuxna med primär hyperkolesterolemi (heterozygot familjär och icke-familjär) eller blandad dyslipidemi, som tillägg till diet:
- i kombination med en statin, eller statin i kombination med annan lipidsänkande behandling, hos patienter som inte når målvärdet för LDL‑kolesterol med högsta tolererade statindos, eller
- ensamt eller i kombination med annan lipidsänkande behandling hos patienter som är statinintoleranta eller när statinbehandling är kontraindicerad.
Dosering (se avsnitt 4.2 i produktresumén)
Den rekommenderade dosen är 284 mg inklisiran administrerat via en enda subkutan injektion: initialt, efter 3 månader och därefter var 6:e månad.
Glömda doser
Om en planerad dos glöms bort i mindre än 3 månader, ska inklisiran administreras och doseringen fortsätta enligt patientens ursprungliga schema.
Om en planerad dos glöms bort i mer än 3 månader, ska ett nytt doseringsschema påbörjas – inklisiran ska återigen administreras initialt, efter 3 månader och därefter var 6:e månad.
Behandlingsbyte från proproteinkonvertas subtilisin/kexin typ 9 (PCSK9)-hämmare i form av monoklonala antikroppar
Inklisiran kan administreras omedelbart efter den sista dosen av en PCSK9‑hämmare (monoklonal antikropp). För att bibehålla sänkningen av lågdensitetslipoprotein-kolesterol (LDL‑kolesterol) bör inklisiran administreras inom 2 veckor efter den sista dosen av en sådan PCSK9‑hämmare.
Särskilda populationer
Äldre
Inga dosjusteringar är nödvändiga för äldre patienter (se avsnitt 5.2 i produktresumén).
Nedsatt leverfunktion
Inga dosjusteringar är nödvändiga för patienter med lätt (Child‑Pugh klass A) eller måttlig (Child‑Pugh klass B) leverfunktionsnedsättning. Data saknas för patienter med gravt nedsatt leverfunktion (Child‑Pugh klass C) (se avsnitt 5.2 i produktresumén). Inklisiran ska användas med försiktighet till patienter med grav leverfunktionsnedsättning.
Nedsatt njurfunktion
Inga dosjusteringar är nödvändiga för patienter med lätt, måttlig eller grav njurfunktionsnedsättning eller för patienter med njursjukdom i slutskedet (se avsnitt 5.2 i produktresumén). Det finns begränsad erfarenhet av inklisiran hos patienter med grav njurfunktionsnedsättning. Inklisiran ska användas med försiktighet till dessa patienter. Se avsnitt 4.4 i produktresumén för försiktighetsåtgärder vid hemodialys.
Pediatrisk population
Säkerhet och effekt för inklisiran för barn under 18 år har ännu inte fastställts. Inga data finns tillgängliga.
Administreringssätt (se avsnitt 4.2 i produktresumén)
Subkutan användning.
Inklisiran är avsett för subkutan injektion i buken; alternativa injektionsställen inkluderar överarm eller lår. Injektioner ska inte ges i områden med aktiv hudsjukdom eller skada såsom solbränna, hudutslag, inflammation eller hudinfektioner.
Varje dos (284 mg) administreras med en förfylld spruta. Varje förfylld spruta är endast avsedd för engångsbruk.
Inklisiran är avsett att administreras av sjukvårdspersonal.
Kontraindikationer (se avsnitt 4.3 i produktresumén)
Överkänslighet mot den aktiva substansen eller mot något hjälpämne.
Varningar och försiktighet (se avsnitt 4.4 i produktresumén)
Hemodialys
Effekten av hemodialys på farmakokinetiken för inklisiran har inte studerats. Eftersom inklisiran elimineras renalt, bör hemodialys inte genomföras förrän tidigast 72 timmar efter dosering med inklisiran.
Förvaring (se avsnitt 6.4 i produktresumén)
Inga särskilda förvaringsanvisningar. Får ej frysas.
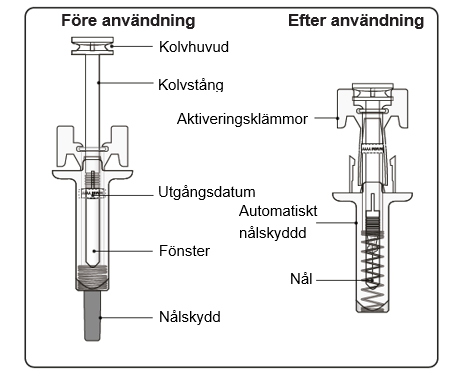
Bruksanvising till Leqvio förfylld spruta med automatiskt nålskydd
Det här avsnittet innehåller information om hur du injicerar Leqvio.
Viktig information som du behöver veta innan du injicerar Leqvio
- Använd inte den förfyllda sprutan om förseglingarna på kartongen eller plasttråget är bruten.
- Ta inte av nålskyddet innan du är redo att injicera.
- Använd inte den förfyllda sprutan om den har tappats på en hård yta eller tappats efter det att nålskyddet har avlägsnats.
- Försök inte återanvända eller ta isär den förfyllda sprutan.
- Den förfyllda sprutan har ett automatiskt nålskydd för att täcka nålen och som aktiveras efter att injektionen är avslutad. Det automatiska nålskyddet hjälper till att förhindra nålsticksskador hos alla som hanterar den förfyllda sprutan efter injektion.
Steg 1. Inspektera den förfyllda sprutan
Du kan eventuellt se luftbubblor i vätska, vilket är normalt. Försök inte ta bort luften.
- Använd inte den förfyllda sprutan om den ser skadad ut eller om något av injektionslösningen har läckt ut ur den förfyllda sprutan.
Steg 2. Ta bort nålskyddet Dra med ett fast grepp av nålskyddet rakt ut från den förfyllda sprutan. Du kan eventuellt se en droppe vätska i ändan av nålen. Det är normalt. Sätt inte på nålskyddet igen. Kasta bort det. Avlägsna inte nålskyddet förrän du är redo att injicera, eftersom för tidigt avlägsnande av nålskyddet i sällsynta fall kan leda till att läkemedlet torkar ut i nålen, vilket kan resultera i att nålen täpps till. | 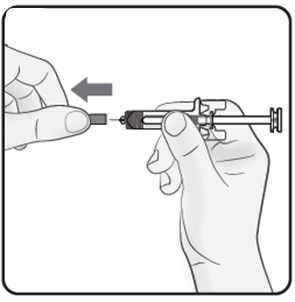 |
Steg 3. För in nålen Nyp försiktigt ihop huden på injektionsstället och behåll huden ihopnypt under hela injektionen. Med den andra handen, för in nålen i huden i en vinkel på cirka 45 grader enligt bilden. | 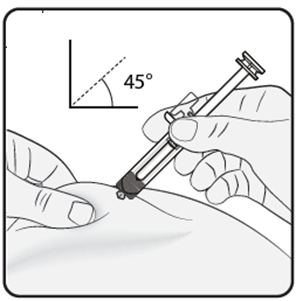 |
Steg 4. Påbörja injektionen Fortsätt hålla huden ihopnypt. Tryck långsamt in kolvstången så långt det går. Detta säkerställer att hela dosen injiceras. Om du vid injicering inte kan trycka ner kolvstången, använd en ny förfylld spruta. | 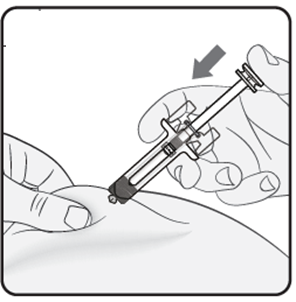 |
Steg 5. Avsluta injektionen Försäkra dig om att kolvhuvudet är mellan aktiveringsklämmorna enligt bilden. Detta säkerställer att det automatiska nålskyddet har aktiverats och täcker nålen efter det att injektionen är avslutad. | 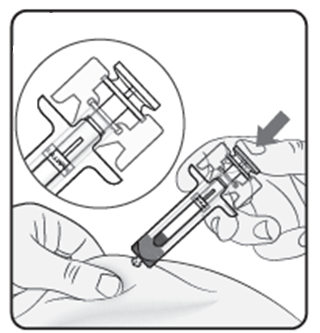 |
Steg 6. Släpp kolvstången Håll kvar den förfyllda sprutan på injektionsstället och släpp långsamt upp kolvstången tills nålen är täckt av det automatiska nålskyddet. Ta bort den förfyllda sprutan från injektionsstället. | 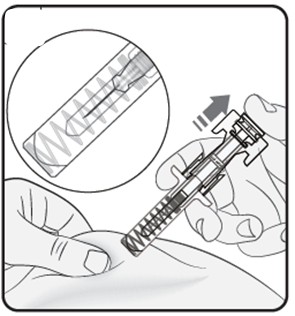 |
Steg 7. Kassera den förfyllda sprutan
Kasta den förfyllda sprutan i enlighet med lokala bestämmelser.