GRAZAX frystorkad sublingual tablett 75000 SQ-T
Tilläggsinformation
GRAZAX 75 000 SQ-T frystorkad sublingual tablett
Standardiserat allergenextrakt från timotej (Phleum pratense)
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar ta detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad Grazax är och vad det används för
2. Vad du behöver veta innan du tar Grazax
3. Hur du tar Grazax
4. Eventuella biverkningar
5. Hur Grazax ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
Grazax innehåller allergenextrakt av gräspollen. Grazax används för att behandla hösnuva (rinit) och ögoninflammation (konjunktivit) orsakad av gräspollenallergi hos vuxna och barn från fem år. Grazax påverkar den allergiska sjukdomen genom att öka immunförsvarets tolerans mot gräspollen.
Vid behandling av barn väljs patienterna ut av läkare som har erfarenhet av att behandla allergiska sjukdomar hos barn.
Läkaren gör en utredning av dina allergiska symtom, och gör ett pricktest eller tar ett blodprov för att bestämma om du ska bli behandlad med Grazax.
Det rekommenderas att du tar första tabletten på läkarens mottagning. Det är en försiktighetsåtgärd för att bedöma hur känslig du är för behandlingen och ger dig möjlighet att diskutera eventuella biverkningar med din läkare.
Grazax förskrivs av läkare med erfarenhet av behandling av allergiska sjukdomar.
Vad du behöver veta innan produkten används
Ta inte Grazax
- om du är allergisk mot något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar)
- om du har en sjukdom som påverkar immunsystemet
- om du har svår astma (enligt läkares bedömning)
- om du har cancer
- om du har en kraftig inflammation i munnen
Varningar och försiktighet
Tala med läkare innan du tar Grazax:
- om du nyligen dragit ut en tand eller genomgått andra ingrepp i munhålan. Gör då ett avbrott i behandlingen med Grazax under 7 dagar för att ge munhålan tid att läka
- om du har allvarlig fiskallergi
- om du tidigare fått en allergisk reaktion i samband med injektion av gräspollenallergen
- om du har astma och en pågående akut infektion i de övre luftvägarna. Behandlingen med Grazax bör avbrytas tillfälligt tills infektionen har avklingat.
Vissa biverkningar kan vara allvarliga och kräver omedelbar medicinsk vård. Se avsnitt Eventuella biverkningar för symtom.
Barn
- om du har tappat en mjölktand: behandling med Grazax ska upphöra i 7 dagar för att ge munhålan tid att läka.
Om något av ovanstående stämmer in på dig skall du tala om det för din läkare innan du börjar med Grazax.
Det finns ingen erfarenhet av behandling med Grazax hos äldre ≥ 65 år.
Andra läkemedel och Grazax
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel, även receptfria sådana.
Om du tar andra läkemedel mot dina allergiska besvär såsom antihistaminer eller kortikosteroider bör din doktor utvärdera användningen av dessa läkemedel.
Grazax med mat och dryck
Ät och drick inget under fem minuter efter tablettintaget.
Graviditet, amning och fertilitet
Det finns för närvarande ingen erfarenhet av behandling med Grazax under graviditet. Behandling med Grazax bör inte inledas under graviditet. Om du blir gravid under behandlingen kontakta din läkare för bedömning om fortsatt behandling är lämplig.
Det finns för närvarande ingen erfarenhet av behandling med Grazax under amning. Grazax förväntas dock inte påverka barn som ammas. Rådgör med din läkare före användning under amning.
Körförmåga och användning av maskiner
Du är själv ansvarig för att bedöma om du är i kondition att framföra motorfordon eller utföra arbete som kräver skärpt uppmärksamhet. En av faktorerna som kan påverka din förmåga i dessa avseenden är användning av läkemedel på grund av deras effekter och/eller biverkningar. Beskrivning av dessa effekter och biverkningar finns i andra avsnitt. Läs därför all information i denna bipacksedel för vägledning. Diskutera med din läkare eller apotekspersonal om du är osäker.
Grazax har ingen eller försumbar effekt på förmågan att framföra fordon och använda maskiner.
Grazax innehåller natrium
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per frystorkad sublingual tablett, d.v.s. är näst intill ”natriumfritt”.
Hur produkten används
Ta alltid detta läkemedel enligt läkarens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
Hur mycket Grazax du ska ta
- Rekommenderad dos är en frystorkad sublingual tablett dagligen.
Hur du tar Grazax
- För bäst effekt ska behandlingen starta minst 4 månader innan gräspollensäsongen förväntas börja. Rekommenderad behandlingstid med Grazax är 3 år.
Den första dosen av Grazax ska tas på läkarmottagningen.
- Det är för att du ska vara under uppsikt av vårdpersonal under cirka en halvtimme efter första tablettintaget.
- Det är en försiktighetsåtgärd för att kontrollera hur känslig du är för läkemedlet.
- Det är även ett tillfälle för dig att diskutera eventuella biverkningar med läkaren.
Fortsätt att ta Grazax varje dag - även om det tar ett tag innan din allergi förbättras.
Om dina allergisymtom inte avtar under den första gräspollensäsongen ska du kontakta läkare för att diskutera den fortsatta behandlingen.
Dina händer måste vara helt torra innan du handskas med tabletterna.
Tabletterna skall tas på följande sätt:
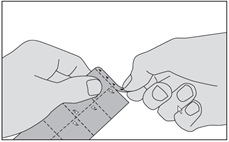
1. Riv av fliken som är markerad med trekanter på toppen av förpackningen.
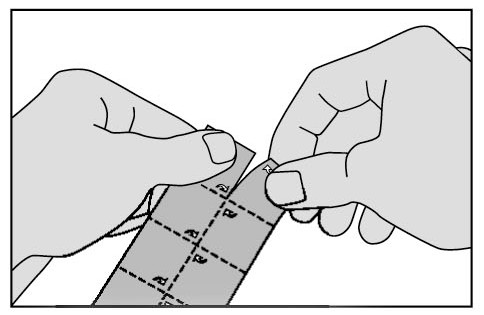
2. Riv av en ruta från förpackningen längs de streckade linjerna.
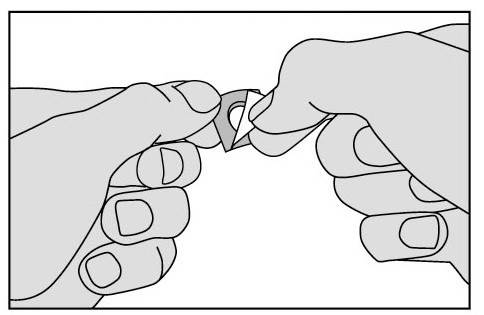
3. Vik tillbaka folien från det markerade hörnet och dra sedan av folien.
- Tryck inte tabletten genom folien - den går lätt sönder.
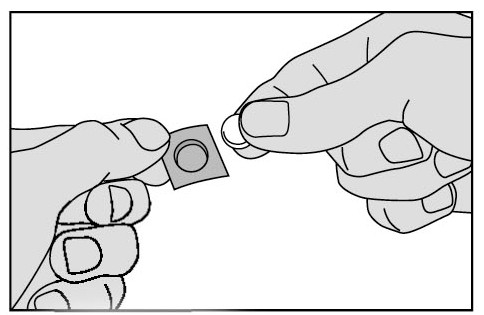
4. Avlägsna försiktigt tabletten från folien och lägg den omedelbart under tungan.
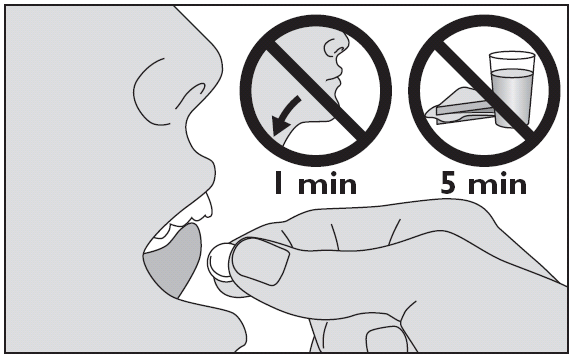
5. Låt tabletten ligga under tungan tills den lösts upp.
- Undvik att svälja under 1 minut.
- Ät eller drick inget under minst 5 minuter efter att du tagit tabletten
Om du har tagit för stor mängd av Grazax
Om du fått i dig för stor mängd läkemedel eller om t.ex. ett barn fått i sig läkemedlet av misstag kontakta läkare, sjukhus eller Giftinformationscentralen (tel. 112 i Sverige, 0800 147 111 i Finland) för bedömning av risken samt rådgivning.
Om du tagit för stor mängd Grazax tabletter kan du få allergiska symtom såsom lokala symtom i mun och hals.
Om du har glömt att ta Grazax
Har du glömt att ta en tablett, kan du ta den senare samma dag. Ta inte dubbel dos för att kompensera för glömd tablett.
Om du slutar att ta Grazax
Om du inte tar det här läkemedlet som ordinerat är det möjligt att du inte får effekt av behandlingen. Om du har ytterligare frågor om detta läkemedel kontakta läkare eller apotekspersonal.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Biverkningarna kan vara en allergisk reaktion på det allergen du behandlas med. Reaktionerna varar i allmänhet minuter till timmar efter intag avtablettenoch avtar oftast spontant inom en vecka efter det att behandlingen påbörjats.
Allvarliga biverkningar:
Sluta att ta Grazax och kontakta omedelbart läkare eller sjukhus om du får något av följande symtom:
- hastigt uppkommen svullnad av ansikte, mun eller hals
- svårigheter att svälja
- svårigheter att andas
- nässelutslag
- förändringar av rösten
- försämring av existerande astma
- svår olustkänsla
Om du får ihållande halsbränna bör du kontakta din läkare.
Andra möjliga biverkningar:
Mycket vanliga (kan förekomma hos fler än 1 av 10 användare):
- svullnad i munnen
- klåda i munnen eller öronen
- irriterande känsla i halsen
Vanliga (kan förekomma hos upp till 1 av 10 användare):
- stickande känsla eller domningar i munnen
- klåda i ögon, läppar eller näsa
- inflammation i ögon eller mun
- andnöd, hosta eller nysningar
- torrhet i halsen
- rinnande näsa
- svullnad av ögon eller läppar
- sår i munnen
- blåsbildning, smärta eller obehag från mun eller hals
- magsmärta, diarré, illamående, kräkningar
- halsbränna
- klåda, utslag eller nässelutslag
- trötthet
- obehag i bröstet
- trånghet i halsen
- rodnad i munnen
- svårigheter att svälja
Mindre vanliga (kan förekomma hos upp till 1 av 100 användare):
- känsla av snabba, kraftiga eller oregelbundna hjärtslag
- smakförändring
- röda eller irriterade ögon
- smärta eller obehag i öronen
- känselbortfall i halsen, smärta vid sväljning
- förstorade halsmandlar
- allvarlig allergisk reaktion
- muntorrhet
- blåsor på läpparna, läppinflammation, sår på läpparna
- förstorade salivkörtlar eller ökad salivproduktion
- inflammation i magen, uppstötningar
- känsla av främmande föremål i halsen
- hudrodnad
- svullnad av ansikte
- inflammation i tungan
- allergisk reaktion
- stickande känsla i huden
- obehag i magen
- svullnad i halsen
- tårflöde
- heshet
- rodnad i halsen
- blåsor i munnen
Sällsynta (kan förekomma hos upp till 1 av 1000 användare):
- sammandragning av nedre luftvägarna
- svullna öron
Ögonirritation, rodnad i halsen, blåsor i munnen, smärta i öronen och svullna öron förekommer oftare hos barn än hos vuxna.
Om du får besvärliga biverkningar, kontakta din läkare som kan avgöra om du behöver ta symtomlindrande allergimediciner, t.ex. antihistaminer.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
Finland
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
00034 FIMEA
Sverige
Läkemedelsverket
Box 26
751 03 Uppsala
www.lakemedelsverket.se
Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatumsom anges på blisterförpackningen och kartongen efter EXP. Utgångsdatumet är den sista dagen i angiven månad.
Inga särskilda förvaringsanvisningar.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
Den aktiva substansen är SQ standardiserat allergenextrakt av pollen från timotej (Phleum pratense).
Aktiviteten per tablett uttrycks i enheten SQ-T*, en tablett innehåller 75 000 SQ-T. Innehåll av allergenet Phl p 5 per tablett är 6 mikrogram.
* [Standardised Quality units Tablet (SQ-T)]- Övriga innehållsämnen är gelatin (från fisk), mannitol och natriumhydroxid.
Läkemedlets utseende och förpackningsstorlekar
Vit till benvit rund frystorkad sublingual tablett med en prägling på ena sidan.
Blisterförpackningar av aluminium med avdragbar aluminiumfolie i en ytterkartong. Varje blisterförpackning innehåller 10 frystorkade sublinguala tabletter.
Följande förpackningar finns: 10 (1x10), 30 (3x10), 90 (9x10) eller 100 (10x10) frystorkade sublinguala tabletter.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
Innehavare av godkännande för försäljning
ALK-Abelló A/S
Bøge Allé 6-8
2970 Hørsholm
Danmark
Tillverkare
ALK-Abelló S.A.
Miguel Fleta 19
28037 Madrid
Spanien
Information lämnas av
Finland
ALK-Abelló Nordic A/S, filial i Finland
tfn: 09 5842 2120
e-post: infofi@alk.net
Sverige
ALK Nordic A/S, Danmark Filial
tfn: 0300 – 185 45
e-post: infose@alk.net
Denna bipacksedel ändrades senast 31.10.2025 (i Finland)