FORSTEO injektionsvätska, lösning i förfylld injektionspenna 20 mikrog/80 mikrol
Tilläggsinformation
FORSTEO 20 mikrogram/80 mikroliter, injektionsvätska, lösning, i förfylld injektionspenna
teriparatid
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även
om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare eller apotekspersonal. Detta gäller även eventuella
biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
1. Vad FORSTEO är och vad det används för
2. Vad du behöver veta innan du använder FORSTEO
3. Hur du använder FORSTEO
4. Eventuella biverkningar
5. Hur FORSTEO ska förvaras
6. Förpackningens innehåll och övriga upplysningar
Vad produkten är och vad den används för
FORSTEO innehåller den aktiva substansen teriparatid som används till att göra skelettet starkare och minska risken för benbrott genom att stimulera benbildning.
FORSTEO används för att behandla osteoporos hos vuxna. Osteoporos är en sjukdom, som gör att benen i kroppen blir tunna och sköra. Sjukdomen är särskilt vanlig hos kvinnor efter menopaus, men kan även förekomma bland män. Osteoporos är också vanligt hos patienter som får kortikosteroider.
Vad du behöver veta innan produkten används
Använd inte FORSTEO
- om du är allergisk mot teriparatid eller något annat innehållsämne i detta läkemedel (anges i avsnitt Förpackningens innehåll och övriga upplysningar).
- om du har ökad mängd kalcium i blodet (hyperkalcemi).
- om du har allvarliga problem med njurarna.
- om du vid något tidigare tillfälle fått diagnos på skelettcancer eller annan cancer som spritt sig (metastaserat) till skelettet.
- om du har en viss typ av bensjukdom. Tala om för din läkare om du har en bensjukdom.
- om du har oförklarligt höga värden av alkalisk fosfatas i blodet, som tyder på att du kan ha Paget’s bensjukdom (sjukdom med onormal nedbrytning och uppbyggnad av ben). Rådfråga din läkare om du är osäker.
- om du har fått strålbehandling som involverar benstommen.
- om du är gravid eller ammar.
Varningar och försiktighet
FORSTEO kan ge en ökad mängd av kalcium i blodet eller urinen.
Tala med läkare eller apotekspersonal innan eller under tiden du använder FORSTEO:
• om du ständigt har illamående, kräkningar, förstoppning, låg energi eller muskelsvaghet. Det kan vara tecken på att du har för mycket kalcium i blodet.
• om du lider av njursten eller har haft njursten tidigare.
• om du lider av njurproblem (måttligt försämrad njurfunktion).
En del patienter blir yra eller får en snabb hjärtfrekvens efter de första doserna. Injicera FORSTEO där du snabbt kan sitta eller ligga ned om du blir yr.
Den rekommenderade behandlingstiden på 24 månader bör inte överskridas.
FORSTEO ska inte användas till unga vuxna.
Barn och ungdomar
FORSTEO ska inte användas till barn eller ungdomar (under 18 år).
Andra läkemedel och FORSTEO
Tala om för läkare eller apotekspersonal om du tar, nyligen har tagit eller kan tänkas ta andra läkemedel, eftersom de i enstaka fall kan påverka effekten av varandra (t ex digoxin/digitalis, för behandling av hjärtsjukdom).
Graviditet och amning
Använd inte FORSTEO om du är gravid eller ammar. Om du är en fertil kvinna ska du använda ett säkert preventivmedel under behandling med FORSTEO. Om du blir gravid ska behandlingen med FORSTEO avslutas. Rådfråga din läkare eller apotekspersonal innan du tar något läkemedel.
Körförmåga och användning av maskiner:
Vissa personer kan känna yrsel efter injektion med FORSTEO. Om du känner dig yr, ska du inte köra bil eller använda verktyg eller maskiner förrän du känner dig bättre.
FORSTEO innhåller natrium:
Detta läkemedel innehåller mindre än 1 mmol natrium (23 mg) per dos. Det innebär att det är nästintill ”natriumfritt”.
Hur produkten används
Använd alltid detta läkemedel enligt läkarens anvisningar. Rådfråga din läkare eller apotekspersonal om du är osäker.
Den rekommenderade dosen av är 20 mikrogram, som injiceras under huden i lår eller buk, en gång om dagen. Ta ditt läkemedel vid samma tidpunkt varje dag för att lättare komma ihåg att ta det.
Injicera FORSTEO varje dag under så lång tid som läkaren förskrivit. Den totala behandlingstiden med FORSTEO bör inte överstiga 24 månader. Du bör inte få mer än en 24 månaders behandlingskur under din livstid.
FORSTEO kan tas i samband med måltid.
Läs i bruksanvisningen, som finns i förpackningen, hur pennan ska användas.
Kanyler medföljer inte förpackningen. Becton Dickinsons injektionskanyler för pennor kan användas.
Injicera FORSTEO strax efter det att pennan tagits ut från kylskåpet, som beskrivs i bruksanvisningen. Lägg tillbaka pennan i kylskåpet omedelbart efter användningen. Använd en ny kanyl vid varje injektion och kasta den efter användningen. Förvara inte pennan med kanylen påsatt. Dela aldrig din FORSTEOpenna med andra.
Din läkare kan ordinera tillägg av kalcium och D-vitamin. Hur mycket av dessa läkemedel du ska ta varje dag bestäms av läkaren.
FORSTEO kan tas oberoende av måltid.
Om du har använt för stor mängd av FORSTEO
Om du av misstag använt mer FORSTEO än du borde, kontakta din läkare eller farmaceut.
För stor dos kan ge illamående, kräkningar, yrsel och huvudvärk.
Om du har glömt att ta FORSTEO eller inte kan ta det vid vanlig tidpunkt, ta injektionen så snart som möjligt samma dag. Ta inte dubbel dos för att kompensera den uteblivna dosen. Ta inte mer än en injektion samma dag även om du missat en dos. Försök inte kompensera den uteblivna dosen.
Om du slutar använda FORSTEO
Om du överväger att avsluta FORSTEO-behandlingen, bör du tala med din läkare. Din läkare kommer att rådgöra med dig och avgöra hur länge du bör fortsätta med FORSTEO.
Om du har ytterligare frågor om detta läkemedel, kontakta läkare eller apotekspersonal.
Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla behöver inte få dem.
De vanligaste biverkningarna är smärta i armar och ben (frekvensen är mycket vanlig, kan påverka fler än 1 av 10 personer) och illamånende, huvudvärk och yrsel (frekvensen är vanlig).
Om du blir yr efter injektionen, sätt eller lägg dig ner tills du känner dig bättre. Om du inte blir bättre ska läkare tillkallas innan behandlingen fortsätts. Fall av svimning har rapporterats i samband med användning av teriparatid.
Om du känner obehag såsom hudrodnad, smärta, svullnad, klåda, blåmärken eller mindre blödning vid injektionsstället (frekvensen är vanlig). Detta brukar oftast försvinna inom några dagar eller veckor.
Annars bör läkare kontaktas så snart som möjligt.
Några patienter har fått allergiska reaktioner kort efter injektionen, såsom andnöd, ansiktssvullnad, utslag och bröstsmärta (frekvensen är sällsynt). I sällsynta fall kan allvarliga och potentiellt livshotande allergiska reaktioner inklusive anafylaxi inträffa.
Andra biverkningar är:
Vanliga: kan påverka upp till 1 av 10 personer
• ökade kolesterolnivåer i blodet
• depression
• neuralgisk (nerv-) smärta i benen
• svaghetskänsla
• oregelbundna hjärtslag
• andfåddhet
• ökad svettning
• muskelkramper
• nedsatt energi
• trötthet
• bröstsmärta
• lågt blodtryck
• halsbränna (smärta eller brännande känsla nedanför bröstbenet)
• illamående (kräkningar)
• bråck i matstrupen
• lågt hemoglobin eller lågt antal röda blodkroppar (anemi).
Mindre vanliga: kan påverka upp till 1 av 100 personer
• ökad hjärtfrekvens
• onormalt hjärtljud
• andfåddhet
• hemorrojder
• urinläckage
• ökat behov att tömma blåsan
• viktökning
• njurstenar
• smärtor i muskler och smärtor i leder. Några patienter har fått så svåra kramper eller smärtor i ryggen, att de fått behandlas på sjukhus
• ökning av kalciummängden i blodet
• ökning av urinsyremängden i blodet
• ökning av ett enzym som heter alkalisk fosfatas.
Sällsynta: kan förekomma hos upp till 1 av 1 000 personer
• nedsatt njurfunktion, inkluderande njursvikt
• svullnad, främst i händer, fötter och ben.
Rapportering av biverkningar
Om du får biverkningar, tala med läkare eller sjuksköterska. Detta gäller även biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet. Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
FI-00034 Fimea
Hur produkten ska förvaras
Förvaras utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på kartongen efter Utg.dat. och på injektionspennan efter EXP.
Utgångsdatum är den sista dagen i angiven månad.
Förvaras i kylskåp (2 °C – 8 °C) både före och under användning. FORSTEO kan användas upp till 28 dagar efter första injektionen, så länge som pennan förvaras i kylskåp (2 °C till 8 °C).
FORSTEO får ej frysas. Undvik att placera pennorna nära frysdelen i kylskåpet för att förhindra att de fryser. Använd inte FORSTEO om det är eller har varit fryst.
Efter 28 dagar ska pennan kasseras, även om den inte är helt tom.
FORSTEO innehåller en klar och färglös lösning. Använd inte FORSTEO om fasta partiklar har bildats i lösningen eller om lösningen är grumlig eller färgad.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man gör med läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
- Den aktiva substansen är teriparatid. En ml injektionsvätska innehåller 250 mikrogram teriparatid.
- Övriga innehållsämnen är koncentrerad ättiksyra, natriumacetat (vattenfri), mannitol, metakresol och vatten för injektionsvätskor. Dessutom kan saltsyra och/eller natriumhydroxid ha tillsatts för pH-justering.
Läkemedlets utseende och förpackningsstorlekar
FORSTEO är en färglös och klar lösning. Den tillhandahålls i en ampull innesluten i en förfylld penna för engångsbruk. Varje penna innehåller 2,4 ml lösning som räcker till 28 doser. Förpackningen innehåller antingen en penna eller tre pennor. Eventuellt kommer inte alla förpackningsstorlekar att tillhandahållas.
Innehavare av godkännande för försäljning
Eli Lilly Nederland B.V., Orteliuslaan 1000, 3528 BD Utrecht, Nederländerna
Tillverkare
Tillverkare: Lilly France S.A.S., Rue du Colonel Lilly, F-67640 Fegersheim, Frankrike
Kontakta ombudet för innehavaren av godkännandet för försäljning om du vill veta mer om detta läkemedel.
Suomi/Finland
Oy Eli Lilly Finland Ab
Puh/Tel: + 358-(0) 9 85 45 250
Denna bipacksedel godkändes senast 2.1.2026
Ytterligare information om detta läkemedel finns på Europeiska läkemedelsmyndighetens webbplats
https://www.ema.europa.eu/.
Denna bipacksedel finns på samtliga EU-/EES-språk på Europeiska läkemedelsmyndighetens webbplats.
Direktiv för användaren
Forsteo
FORSTEO 20 mikrogram (μg) / 80 mikroliter injektionsvätska, lösning i förfylld penna
Användaranvisningar
Läs igenom hela avsnittet Användaranvisningar innan du börjar använda din nya penna. Följ instruktionerna noggrant.
Läs även bipacksedeln som finns i förpackningen.
Pennan innehåller läkemedel för 28 dagar.
| Pennans delar* | ||||
| Gul skalm | ||||
| Svart injektions-knapp |  |  | ||
| Rött band Blå pennkropp Ampull med läkemedel | Vit skyddshatt | |||
 |  |  | 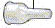 | |
| Pappersflik | Kanyl | Litet kanylskydd | Stort kanylskydd | |
| * Kanyler medföljer inte. Becton, Dickinson pennkanyler kan användas. Fråga din läkare/sköterska vilken kanylstorlek som är lämplig för dig. | ||||
Tvätta alltid händerna före varje injektion. Förbered injektionsstället som din
läkare/sköterska instruerat dig.
| 1 Dra av den vita skyddshatten | 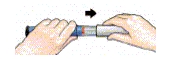 |
| 2 Sätt på en ny kanyl |  | 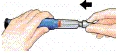 | 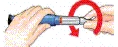 | Stort kanylskydd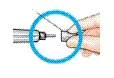 |
| Riv av pappersfliken. | Sätt på kanylen rakt mot ampullen. | Skruva på kanylen tills den sitter fast ordentligt. | Dra av det stora kanylskyddet och spara det. |
| 3 Ställ in dosen |  | 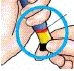 | Rött band | Litet kanyl- skydd | 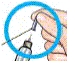 |
Dra ut den svarta Om du inte kan dra | Kontrollera att det röda bandet syns. | Dra av det lilla kanylskyddet och kasta det. |
| 4 Injicera dosen | 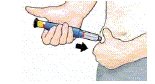 | 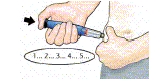 |
| Ta ett försiktigt tag om huden i låret eller magen och för kanylen rakt in i huden. | Tryck in den svarta injektionsknappen tills det tar stopp. Håll in den och räkna l å n g s a m t till 5. Dra sedan ut kanylen ur huden. |
| VIKTIGT | ||||
| 5 Bekräfta dosen | 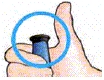 | När du har injicerat dosen: Så snart du har dragit ut kanylen ur huden, kontrollera att den svarta injektionsknappen är helt intryckt. Om den gula skalmen inte syns har du gjort rätt när du injicerat. | 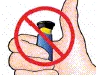 | Du ska INTE se något av den gula skalmen. Om du gör det efter det att du har injicerat, ta inte en till dos samma dag. I stället MÅSTE du återställa FORSTEO-pennan (läs under Felsökning, Problem A). |
| 6 Ta av kanylen | Stort kanylskydd | 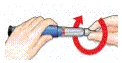 | 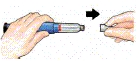 | 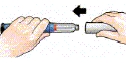 |
| Sätt på det stora kanylskyddet på kanylen. | Skruva av kanylen helt genom att vrida runt det stora kanylskyddet ordentligt 3- 5 varv. | Dra av kanylen och kasta den som din läkare/sköterska instruerat dig. | Sätt på den vita skyddshatten. Lägg pennan i kylskåpet omedelbart efter användningen. |
Anvisningarna angående hantering av kanyler ersätter inte lokala regler.
 | Forsteo FORSTEO, 20 mikrogram (μg) / 80 mikroliter injektionsvätska, lösning i förfylld penna |
| Felsökning | |||
| Problem A. Den gula skalmen syns fortfarande efter 1 tryck på den svarta injektionsknappen. Hur återställer jag min FORSTEO-penna? |  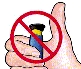 | Åtgärd För att återställa pennan, följ nedanstående steg. | |
| Du kan förhindra att detta problem uppstår genom att alltid använda en NY kanyl vid varje injektion, och l å n g s a m t räkna till 5 medan du trycker in den svarta injektionsknappen helt. | |||
| B. Hur vet jag att min FORSTEO-penna fungerar? |  | FORSTEO-pennan är utformad så att du ska få en full dos varje gång du använder den, om du följer Användaranvisningarna. När den svarta injektionsknappen är helt intryckt betyder det att en full dos FORSTEO har injicerats. Kom ihåg att sätta på en ny kanyl varje gång du ska injicera, för att vara säker på att pennan fungerar korrekt. | |
| C. Jag ser en luftbubbla i lösningen. |  | En liten luftbubbla påverkar inte dosen och är heller inte skadlig. Du kan fortsätta att ta din dos som vanligt. | |
| D. Jag kan inte få av kanylen. |  | 1) Sätt på det stora kanylskyddet på kanylen. 2) Använd det stora kanylskyddet när du ska skruva av kanylen. 3) Skruva av kanylen helt genom att vrida runt det stora kanylskyddet ordentligt 3-5 varv. 4) Om du fortfarande inte kan få av kanylen, be någon hjälpa dig. | |
| E. Vad ska jag göra om jag inte kan dra ut den svarta injektionsknappen? |  | Byt till en ny FORSTEO-penna och ta din dos som din läkare/sköterska instruerat dig. Det betyder att du nu har använt allt läkemedel som kan injiceras, även om du fortfarande kan se att det är lite lösning kvar i ampullen. | |
Rengöring och förvaring Rengöring av din FORSTEO-penna
Förvaring av FORSTEO-pennan
|
Kassering av kanyler och pennor
|
Annan viktig information
|
Tillverkad av Lilly France, F-67640 Fegersheim, Frankrike för Eli Lilly and Company.
Denna manual uppdaterades senast 2.1.2026