SONOVUE injektiokuiva-aine ja liuotin, dispersiota varten 8 mikrol/ml
SonoVue 8 μL/ml, injektiokuiva-aine ja liuotin, dispersiota varten
Rikkiheksafluoridi
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin sinulle annetaan tätä lääkettä, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä seloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai apteekkihenkilökunnan puoleen.
- Tämä lääke on määrätty vain sinulle eikä sitä tule antaa muiden käyttöön. Se voi aiheuttaa haittaa muille, vaikka heillä olisikin samanlaiset oireet kuin sinulla.
- Jos havaitset haittavaikutuksia, käänny lääkärin tai apteekkihenkilökunnan puoleen. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
- Mitä SonoVue on ja mihin sitä käytetään
- Mitä sinun on tiedettävä, ennen kuin sinulle annetaan SonoVueta
- Miten SonoVueta annetaan
- Mahdolliset haittavaikutukset
- SonoVuen säilyttäminen
- Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
SonoVue on tarkoitettu vain diagnostiseen käyttöön.
SonoVue on ultraäänikuvausaine, joka sisältää pienenpieniä rikkiheksafluoridi-kaasua sisältäviä kuplia.
Jos olet aikuinen, SonoVue auttaa saamaan parempia ultraäänikuvia sydämestä, verisuonistosta ja/tai maksan tai rinnan kudoksista.
SonoVue auttaa saamaan parempia kuvia lasten virtsateistä.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä käytä SonoVueta:
- jos olet allerginen rikkiheksafluoridille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa),
- jos sinulla tiedetään olevan veren oikovirtaus sydämen oikealta puolelta vasemmalle puolelle,
- jos sinulla on voimakkaasti kohonnut keuhkovaltimon verenpaine (keuhkovaltimon verenpaine > 90 mmHg),
- jos sinulla on kontrolloimaton verenpaine,
- jos sinulla on aikuisten hengenahdistusoireyhtymä (vaikea sairaus, jossa keuhkoissa on laajalle levinnyt tulehdustila),
- jos sinulle on sanottu, että et saa käyttää dobutamiinia (sydäntä stimuloiva lääke) vaikean sydänsairautesi vuoksi.
Varoitukset ja varotoimet
Kerro lääkärillesi, jos sinulla on edeltävän 2 vuorokauden kuluessa ollut:
- usein esiintyviä ja/tai toistuvia angina pectoris- tai rintakipuja, etenkin, jos sinulla on aiemmin todettu sydänsairaus,
- tuoreita muutoksia EKG:ssa.
Kerro lääkärille ennen kuin sinulle annetaan SonoVue-valmistetta, jos:
- sinulla on äskettäin ollut sydäninfarkti tai sinulle on äskettäin tehty sepelvaltimoleikkaus,
- sinulla on angina pectoris tai rintakipuja tai vaikea sydänsairaus,
- sinulla on vaikeita rytmihäiriöitä,
- sydänsairautesi on vaikeutunut äskettäin,
- sinulla on akuutti sydämen sisäkalvon tulehdus (endokardiitti),
- sinulla on keinoläppä sydämessä,
- sinulla on akuutti yleistynyt tulehdustila tai infektio,
- sinulla tiedetään olevan veren hyytymishäiriö,
- sinulla on vaikea munuais- tai maksasairaus.
Jos sinulle annetaan SonoVueta yhdessä sellaisen lääkkeen, liikunnan tai laitteen kanssa, joka kiihdyttää sydämen toimintaa, jotta nähdään, kuinka sydän toimii rasituksessa, sydämesi toimintaa, verenpainetta ja sydämen sykettä seurataan.
SonoVue sisältää makrogolia, joka on myös polyetyleeniglykolina (PEG) tunnettu aineosa. Vaikeita allergisia reaktioita on ilmoitettu. Vakavien reaktioiden riski saattaa olla suurentunut potilailla, jotka ovat saaneet aiemmin allergisen reaktion (allergisia reaktioita) polyetyleeniglykolista. Kerro lääkärille, jos olet saanut aiempia allergisia reaktioita polyetyleeniglykolia sisältävistä tuotteista.
Potilaan tarkka seuranta vähintään 30 minuutin ajan SonoVue-valmisteen annon jälkeen on tarpeen vakavien allergisten reaktioiden riskin tarkkailemiseksi.
Lapset ja nuoret
Alle 18-vuotiaille potilaille SonoVue-valmistetta voidaan käyttää vain virtsateiden ultraäänikuvauksessa.
Muut lääkevalmisteet ja SonoVue
Kerro lääkärille, jos parhaillaan käytät tai olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä.
Erityisesti kerro lääkärille, jos käytät beetasalpaajia (lääkkeitä, joita käytetään sydänsairauksien ja verenpainetaudin hoitoon sekä silmätippoina glaukooman hoitoon).
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä neuvoa ennen kuin tätä lääkettä annetaan sinulle.
SonoVuen kulkeutumisesta äidinmaitoon ei ole tietoa. Imetys täytyy kuitenkin lopettaa 2–3 tunniksi ultraäänitutkimuksen jälkeen.
Ajaminen ja koneiden käyttö
SonoVue ei vaikuta ajokykyyn tai koneiden käyttökykyyn.
SonoVue sisältää natriumia
Tämä lääkevalmiste sisältää alle 1 mmol (23 mg) natriumia per annos eli sen on olennaisesti natriumiton.
Miten valmistetta käytetään
Lääketieteen tai hoitoalan ammattilainen, joka on perehtynyt tämänlaisiin tutkimuksiin, antaa sinulle SonoVue-injektion.
Aikuisten sydämen, verisuonten ja/tai maksan ja rinnan kudosten ultraäänikuvaus: laskimoon annettava annos lasketaan sen perusteella, mitä osaa elimistöstä tutkitaan. Suositeltu annos on 2 ml tai 2,4 ml potilasta kohden. Tämä annos voidaan uusia tarvittaessa niin, että suurin annos on yhteensä 4,8 ml.
Lasten virtsateiden ultraäänikuvauksessa suositeltu annos potilasta kohden on 1 ml, joka annetaan virtsarakkoon seuraavasti:
Rakon tyhjentämisen jälkeen rakkoon valutetaan suolaliuosta ohuen putken avulla. Sitten SonoVue valutetaan saman putken avulla rakkoon, minkä jälkeen rakon täyttämistä jatketaan suolaliuoksella. Rakon täyttäminen ja tyhjentäminen suolaliuoksella voidaan toistaa tarvittaessa.
Jos sinulla on vakava keuhko- tai sydänsairaus, sinua tarkkaillaan huolellisesti tutkimuksen ajan ja vähintään 30 minuutin ajan SonoVue-injektion jälkeen.
Jos sinulle annetaan enemmän SonoVueta kuin pitäisi
Koska lääkäri antaa sinulle SonoVue-injektion, yliannostus ei ole todennäköinen. Jos yliannostus tapahtuu, lääkäri toimii asianmukaisesti.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Useimmat haittavaikutukset ovat harvinaisia eivätkä ne tavallisesti ole vakavia. Kuitenkin osa potilaista voi saada vakavia hoitoa vaativia haittavaikutuksia.
Kerro heti lääkärillesi, jos havaitset joitain seuraavista haittavaikutuksista, joihin voit tarvita hoitoa:
kasvojen, huulten, suun tai kurkun turvotus, joka saattaa vaikeuttaa hengittämistä tai nielemistä; ihottuma; käsien, jalkojen tai nilkkojen turvotus.
Seuraavia haittavaikutuksia on ilmoitettu SonoVuen käytön yhteydessä:
Melko harvinaiset haittavaikutukset (voi esiintyä enintään 1 henkilöllä 100:sta):
- päänsärky,
- puutuminen,
- huimaus,
- outo maku suussa,
- punoitus,
- epämukava tunne rinnassa,
- pahoinvointi,
- vatsakipu,
- ihottuma,
- kuumuuden tunne,
- paikalliset reaktiot injektiokohdassa kuten kipu tai epätavallinen tunto.
Harvinaiset (voi esiintyä enintään 1 henkilöllä 1000:sta):
- näön hämärtyminen,
- matala verenpaine,
- kutina,
- selkäkipu,
- kipu yleisesti,
- rintakipu,
- väsymys,
- vakava tai vähemmän vakava allerginen reaktio (johon liittyy ihon punoitus, sykkeen ja verenpaineen lasku, hengästyminen, tajuttomuus, sydänpysähdys/sydämen toiminnan ja hengityksen pysähtyminen tai muu vakava reaktio johon liittyy hengitysvaikeuksia ja huimausta).
Yleisyys tuntematon (saatavilla oleva tieto ei riitä yleisyyden arviointiin):
- niskaan tai vasempaan käsivarteen säteilevä rintakipu, joka voi olla merkki mahdollisesti vakavasta allergiareaktiosta nimeltään Kounisin oireyhtymä,
- heikotus,
- joissakin yliherkkyystapauksissa sepelvaltimotautia sairastavilla potilailla raportoitiin sydänlihaksen hapenpuutetta tai sydänpysähdys,
- oksentelu.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai, apteekkihenkilökunnalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (ks. yhteystiedot alla).
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä etiketissä mainitun viimeisen käyttöpäivämäärän jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Tämä lääkevalmiste ei vaadi erityisiä säilytysolosuhteita.
SonoVue-dispersio tulee annostella sinulle kuuden tunnin kuluessa sen valmistamisesta.
Pakkauksen sisältö ja muuta tietoa
Mitä SonoVue sisältää
- Vaikuttava aine on rikkiheksafluoridi, joka on hienojakoisena dispersiona.
- Muut aineet ovat makrogoli 4000, distearoyylifosfatidyylikoliini, dipalmitoyylifosfatidyyliglyserolinatrium ja palmitiinihappo.
Lasinen ruisku sisältää 9 mg/ml (0,9 %) natriumkloridi-injektionestettä.
Lääkevalmisteen kuvaus ja pakkauskoko
SonoVue-pakkaus sisältää injektiokuiva-aineen lasipullossa, liuottimen lasiruiskussa sekä siirtolaitteen.
Myyntiluvan haltija ja valmistaja
Myyntiluvan haltija
Bracco International B.V.
Argonstraat 3
6422 PH Heerlen
Alankomaat
Valmistaja
Bracco Imaging S.p.A
Via Ribes 5, Bioindustry Park
Colleretto Giacosa - 10010 (TO)
Italia
Tämä pakkausseloste on tarkistettu viimeksi 18.3.2026
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivuilta http://www.ema.europa.eu.
Ohjeet terveydenhuollon ammattilaiselle
Dispersio pitää ravistaa uudelleen ennen ruiskuun vetämistä, jos SonoVueta ei käytetä heti sekoittamisen jälkeen.
Valmiste on tarkoitettu käytettäväksi vain yhteen tutkimukseen. Käyttämättä jäänyt neste on hävitettävä tutkimuksen päätyttyä.
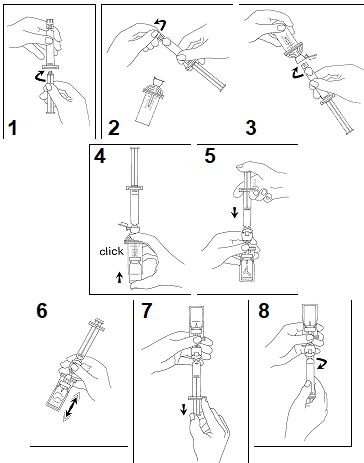
Ohjeet käyttökuntoon saattamiseksi:
- Kiinnitä mäntä ruiskuun kiertämällä sitä myötäpäivään.
- Avaa Mini-Spike-siirtosysteemipakkaus ja poista ruiskusta korkki.
- Avaa siirtosysteemin korkki ja liitä ruisku siirtosysteemiin kiertämällä sitä myötäpäivään.
- Poista suojalevy injektiopullosta. Työnnä injektiopullo siirtosysteemin läpinäkyvään putkeen ja paina voimakkaasti, jotta injektiopullo kiinnittyy paikalleen.
- Tyhjennä ruiskun sisältö injektiopulloon painamalla mäntää.
- Ravista voimakkaasti 20 sekuntia sekoittaaksesi koko injektiopullon sisällön ja saadaksesi valkoisen, tasalaatuisen, maitomaisen liuoksen.
- Käännä systeemi ylösalaisin ja vedä SonoVue varovasti ruiskuun.
- Irrota ruisku siirtosysteemistä.
Käyttökuntoon saattamisen jälkeen SonoVue on homogeeninen, valkoinen, maitomainen dispersio.
Älä käytä, jos valmistettu liuos on kirkas ja/tai suspensiossa näkyy kiinteitä injektiokuiva-ainehiukkasia.
SonoVue-dispersio pitää käyttää kuuden tunnin kuluessa sen valmistamisesta.
Lääkkeitä ei tule heittää viemäriin eikä hävittää talousjätteiden mukana. Kysy käyttämättömien lääkkeiden hävittämisestä apteekista. Näin menetellen suojelet luontoa.