APRETUDE injektioneste, depotsuspensio 600 mg
Apretude 600 mg injektioneste, depotsuspensio
kabotegraviiri
Lisäseuranta
▼ Tähän lääkevalmisteeseen kohdistuu lisäseuranta. Tällä tavalla voidaan havaita nopeasti turvallisuutta koskevaa uutta tietoa. Voit auttaa ilmoittamalla kaikista mahdollisesti saamistasi haittavaikutuksista. Ks. kohdan Mahdolliset haittavaikutukset lopusta, miten haittavaikutuksista ilmoitetaan.
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin aloitat tämän lääkkeen ottamisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin tai sairaanhoitajan puoleen.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
1. Mitä Apretude on ja mihin sitä käytetään
2. Mitä sinun on tiedettävä, ennen kuin saat Apretudea
3. Miten Apretude annetaan
4. Mahdolliset haittavaikutukset
5. Apretuden säilyttäminen
6. Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Apretuden vaikuttava aine on kabotegraviiri. Kabotegraviiri kuuluu integraasinestäjiksi (INI) kutsuttujen retroviruslääkkeiden ryhmään.
Apretudea käytetään HIV‑1‑tartunnan ehkäisyyn aikuisilla ja nuorilla, joiden paino on vähintään 35 kg ja joilla on suurentunut tartuntariski. Tällaista hoitoa kutsutaan altistusta edeltäväksi estohoidoksi eli prep‑hoidoksi (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä). Sitä käytetään yhdistettynä turvaseksikäytäntöihin, kuten kondomin käyttöön.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä käytä Apretudea:
- jos sinulla on esiintynyt aiemmin vaikeaa ihottumaa, ihon kuoriutumista, rakkuloita ja/tai suun haavaumia.
- jos olet allerginen kabotegraviirille tai tämän lääkkeen jollekin muulle aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa).
- jos olet HIV‑positiivinen tai et tiedä, oletko HIV‑positiivinen. Apretude voi pienentää HIV‑tartunnan riskiä vain ennen kuin tartunta on tapahtunut. Sinun on käytävä HIV‑testissä varmistaaksesi, että olet HIV‑negatiivinen, ennen kuin aloitat Apretuden käytön.
- jos käytät jotakin seuraavista lääkkeistä:
- karbamatsepiini, okskarbatsepiini, fenytoiini, fenobarbitaali (epilepsian hoitoon ja epilepsiakohtausten ehkäisyyn).
- rifampisiini tai rifapentiini (eräiden bakteeri‑infektioiden kuten tuberkuloosin hoitoon).
Nämä lääkkeet heikentävät Apretuden tehoa vähentämällä sen määrää veressä.
- Kerro lääkärille, jos arvelet näiden kohtien koskevan sinua tai jos et ole varma asiasta.
Varoitukset ja varotoimet
Pelkkä Apretuden käyttö ei välttämättä suojaa HIV‑tartunnalta.
HIV‑infektio tarttuu seksikontaktissa HIV‑positiivisen henkilön kanssa tai HI‑virusta sisältävästä verestä. Vaikka Apretude pienentää tartuntariskiä, voit silti saada HIV‑tartunnan käyttäessäsi tätä lääkettä.
Pienennä HIV‑tartunnan riskiä myös seuraavilla tavoilla:
- Käy sukupuolitautitesteissä lääkärin ohjeen mukaisesti. Muut sukupuolitaudit saattavat lisätä HIV‑tartunnan riskiä.
- Käytä kondomia suuseksissä ja yhdynnässä.
- Älä käytä yhteisiä tai käytettyjä neuloja tai muita suonensisäisten huumeiden pistämisvälineitä.
- Älä käytä yhteisiä hygieniavälineitä, joissa voi olla verta tai muita eritteitä (esimerkiksi partaterät ja hammasharjat).
Keskustele lääkärin kanssa muista tavoista, joilla voit pienentää HIV‑tartunnan riskiä.
Pienennä HIV‑tartunnan riskiä:
Tälle lääkkeelle voi kehittyä resistenssi, jos saat HIV‑tartunnan. Se tarkoittaa, että lääke ei ehkäise HIV‑tartuntaa. Jotta tämä riski olisi mahdollisimman pieni ja jotta lääke estäisi HIV‑tartunnan, on tärkeää, että:
- käyt sovituilla käynneillä saadaksesi Apretude‑pistoksesi. Keskustele lääkärin kanssa, jos aiot lopettaa pistosten ottamisen, koska se voi suurentaa riskiäsi saada HIV‑tartunta. Jos lopetat valmisteen käytön tai Apretude‑pistoksesi myöhästyy, sinun on käytettävä muita lääkkeitä tai varotoimia HIV‑riskisi pienentämiseen ja mahdollisen virusresistenssin kehittymisen estämiseen.
- käyt HIV‑testissä lääkärin ohjeen mukaan. Testissä on käytävä säännöllisesti, jotta voidaan varmistaa, että olet HIV‑1‑negatiivinen käyttäessäsi Apretudea.
- kerrot lääkärille heti, jos epäilet mahdollisesti saaneesi HIV‑tartunnan (tartunta voi muistuttaa tavallista flunssaa). Lääkäri voi määrätä lisätestejä varmistaakseen, että olet edelleen HIV‑negatiivinen.
Apretude‑pistos on pitkävaikutteinen lääke
Jos lopetat Apretude‑pistosten ottamisen, kabotegraviiria pysyy elimistössäsi jopa vuoden ajan viimeisen pistoksen jälkeen. Sitä ei kuitenkaan ole tarpeeksi, jotta se suojaisi tartunnalta.
On tärkeää, että käyt sovituilla vastaanottokäynneillä saamassa Apretude‑pistoksesi. Keskustele lääkärin kanssa, jos suunnittelet prep‑hoidon lopettamista.
Kun lopetat Apretude‑pistosten ottamisen, sinun on mahdollisesti käytettävä muita lääkkeitä tai muita turvaseksivarotoimia pienentääksesi HIV‑tartunnan riskiä.
Maksavaivat
Kerro lääkärillesi, jos sinulla on jokin maksavaiva. Tarkempi seuranta saattaa olla tarpeen. (Ks. myös kohta Mahdolliset haittavaikutukset, Melko harvinaiset haittavaikutukset.)
Nuoret
Lääkäri keskustelee kanssasi mielenterveyteesi liittyvistä asioista ennen kuin käytät Apretudea sekä Apretuden käytön aikana. Kerro lääkärille, jos sinulla on mielenterveysongelmia, koska saatat tarvita tarkempaa seurantaa (ks. myös kohta Mahdolliset haittavaikutukset).
Vaikeat iho reaktiot
Vakavia ihoreaktioita, Stevens-Johnsonin oireyhtymää ja toksista epidermaalista nekrolyysia, on raportoitu hyvin harvoin Apretuden käytön yhteydessä. Lopeta Apretuden käyttö ja hakeudu välittömästi lääkäriin jos havaitset mitään oireita, jotka liittyvät näihin vakavin iho-oireisiin
- Lue tiedot tämän pakkausselosteen kohdasta Mahdolliset haittavaikutukset. (”Mahdolliset haittavaikutukset”).
Allerginen reaktio
Apretude sisältää kabotegraviiria, joka on integraasinestäjä. Integraasinestäjät, myös kabotegraviiri, voivat aiheuttaa vakavan allergisen reaktion, ns. yliherkkyysreaktion. Sinun on tärkeää tietää, millaisiin oireisiin ja löydöksiin on kiinnitettävä huomiota, kun saat Apretudea.
- Lue tiedot kohdasta ”Mahdolliset haittavaikutukset” tämän pakkausselosteen kohdasta Mahdolliset haittavaikutukset.
Lapset ja nuoret
Tätä lääkettä ei saa antaa alle 35 kg painaville lapsille tai nuorille, koska sitä ei ole tutkittu tällaisilla henkilöillä.
Muut lääkevalmisteet ja Apretude
Kerro lääkärille, jos parhaillaan käytät, olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä, myös lääkkeitä, joita lääkäri ei ole määrännyt.
Jotkin lääkkeet saattavat vaikuttaa Apretuden tehoon tai suurentaa haittavaikutusten todennäköisyyttä. Apretude voi myös vaikuttaa joidenkin muiden lääkkeiden tehoon.
Apretudea ei saa antaa joidenkin muiden lääkkeiden kanssa, koska ne voivat vaikuttaa Apretuden tehoon (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä, ”Älä käytä Apretudea”). Näitä ovat mm.:
- karbamatsepiini, okskarbatsepiini, fenytoiini, fenobarbitaali (epilepsian hoitoon ja epilepsiakohtausten ehkäisyyn).
- rifampisiini tai rifapentiini (eräiden bakteeri‑infektioiden kuten tuberkuloosin hoitoon).
Kerro lääkärille, jos käytät jotakin seuraavista:
- rifabutiini (joidenkin bakteeri‑infektioiden kuten tuberkuloosin hoitoon). Saatat tarvita Apretude‑pistoksia tavallista useammin.
Kerro lääkärille tai apteekkihenkilökunnalle, jos käytät tätä lääkettä. Lääkäri saattaa järjestää sinulle ylimääräisiä kontrollikäyntejä.
Raskaus ja imetys
Jos olet raskaana tai imetät, epäilet olevasi raskaana tai jos suunnittelet lapsen hankkimista, kysy lääkäriltä neuvoa ennen kuin sinulle annetaan tätä lääkettä.
Raskaus
Apretuden käyttöä ei suositella raskauden aikana. Apretuden vaikutusta raskauteen ei tunneta. Keskustele lääkärin kanssa, jos saatat tulla raskaaksi, jos suunnittelet lapsen hankkimista tai jos tulet raskaaksi. Älä lopeta Apretuden antamista varten sovittuja käyntejä keskustelematta lääkärin kanssa. Lääkäri arvioi Apretuden aloittamisesta/jatkamisesta saamasi hyödyn ja mahdolliset sikiölle aiheutuvat riskit.
Imetys
Ei tiedetä, erittyvätkö Apretuden sisältämät aineet rintamaitoon. Kabotegraviiria saattaa kuitenkin kulkeutua rintamaitoon jopa 12 kuukauden ajan viimeisen Apretude‑pistoksen jälkeen. Jos imetät tai aiot imettää, kysy asiasta lääkäriltä. Lääkäri arvioi imetyksestä sinulle ja lapsellesi koituvat hyödyt ja riskit.
Ajaminen ja koneiden käyttö
Apretude voi aiheuttaa huimausta tai muita haittavaikutuksia, jotka voivat huonontaa tarkkaavuuttasi.
- Älä aja äläkä käytä koneita, ellet ole varma, ettei tarkkaavuutesi ole heikentynyt.
Miten valmistetta käytetään
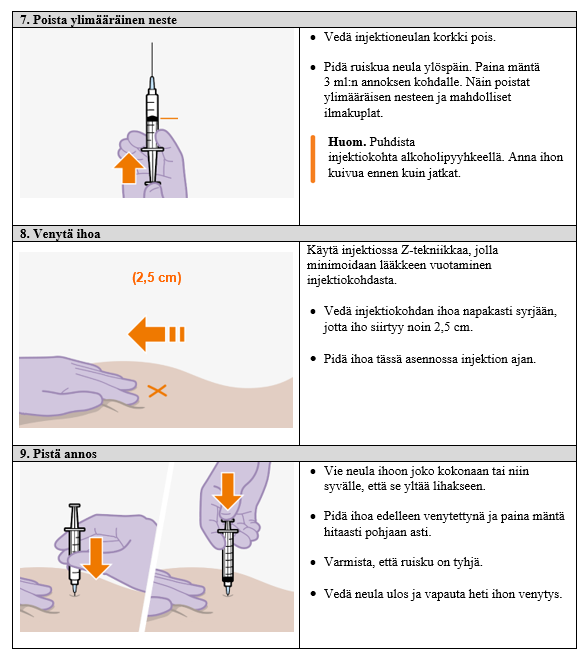
Lääke annetaan 600 mg:n pistoksena. Sairaanhoitaja tai lääkäri pistää Apretuden pakaralihakseesi.
HIV‑testisi on oltava negatiivinen ennen kuin sinulle annetaan Apretudea.
Saat toisen annoksen Apretudea yhden kuukauden kuluttua ensimmäisestä. Toisen annoksen jälkeen saat yhden Apretude‑pistoksen kahden kuukauden välein.
Ennen Apretude‑pistoshoidon aloittamista on mahdollista sopia lääkärin kanssa, että käytät ensin kabotegraviiritabletteja (tätä sanotaan peroraaliseksi eli suun kautta otettavaksi aloitushoidoksi). Aloitushoidon avulla sinä ja lääkärisi voitte arvioida pistoshoidon sopivuutta sinulle.
Jos aloitat ensin tablettihoidon:
- sinun on otettava yksi 30 mg:n Apretude‑tabletti kerran vuorokaudessa noin yhden kuukauden ajan
- sinun on saatava ensimmäinen pistos viimeisen tabletin ottopäivänä tai enintään kolmen vuorokauden kuluessa siitä
- tämän jälkeen saat pistoksen 2 kuukauden välein.
Pistosaikataulu, kun lääke annetaan 2 kuukauden välein
| Ajankohta |
Lääke |
| Ensimmäinen ja toinen pistos, 1 kuukauden välein |
Apretude 600 mg |
| Kolmas ja sitä seuraavat pistokset, 2 kuukauden välein |
Apretude 600 mg |
Jos saat enemmän Apretude‑injektionestettä kuin sinun pitäisi
Lääkäri tai hoitaja antaa tämän lääkkeen sinulle, joten on hyvin epätodennäköistä, että saisit liian suuren annoksen. Jos pelkäät saaneesi liian suuren annoksen, kerro lääkärille tai sairaanhoitajalle, niin sinua hoidetaan tarpeen mukaan.
Jos Apretude‑pistos jää väliin
Ota heti yhteys lääkäriin ja sovi uusi käyntiaika.
On tärkeää käydä sovituilla käynneillä, jotta saat pistoksesi ja HIV‑tartunnan riskiä voidaan pienentää (ks. kohta Mitä sinun on tiedettävä ennen valmisteen käyttöä). Keskustele lääkärin kanssa, jos suunnittelet lopettavasi Apretuden käytön.
Keskustele lääkärin kanssa, jos arvelet, että et voi ottaa Apretude‑pistostasi tavanomaisena ajankohtana. Lääkäri saattaa suositella, että käytät sen sijasta kabotegraviiritabletteja, kunnes pystyt taas ottamaan Apretude‑pistoksen.
Älä lopeta Apretude‑pistosten ottamista kysymättä ensin neuvoa lääkäriltä.
Ota Apretude‑pistoksia niin kauan kuin lääkäri määrää. Älä lopeta hoitoa, ellei lääkäri kehota sinua tekemään niin. Jos lopetat Apretuden käytön ja sinulla on edelleen HIV‑tartunnan riski, lääkärin on aloitettava sinulle toinen prep‑lääkehoito kahden kuukauden kuluessa viimeisestä Apretude‑pistoksesta.
Jos sinulla on kysymyksiä tämän lääkkeen käytöstä, käänny lääkärin tai apteekkihenkilökunnan puoleen.
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Lopeta Apretuden käyttö ja ota välittömästi yhteyttä lääkäriin jos huomaat seuraavia oireita:
- punertavia, ei kohollaan olevia, maalitaulua muistuttavia tai rengasmaisia läiskiä vartalon iholla, joissa on usein keskellä rakkuloita, ihon kuoriutumista, haavaumia suussa, kurkussa, nenässä, sukuelinten alueella ja silmissä. Nämä vakavat ihottumat voi alkaa kuumeella tai flunssan kaltaisilla oireilla (Stevens-Johnsonin oireyhtymä, toksinen epidermaalinen nekrolyysi). Nämä vakavat ihoreaktiot ovat hyvin harvinaisia (voi esiintyä enintään 1:llä ihmisellä 10 000:sta).
Allergiset reaktiot
Apretude sisältää kabotegraviiria, joka on integraasinestäjä. Integraasinestäjät, myös kabotegraviiri, voivat aiheuttaa vakavan allergisen reaktion, ns. yliherkkyysreaktion.
Jos saat jonkin seuraavista oireista:
- ihottuma
- kuume
- energian puute (uupumus)
- turvotus, joskus kasvojen tai nielun turpoaminen (angioedeema), joka aiheuttaa hengitysvaikeuksia
- lihas‑ tai nivelsärky.
Hakeudu heti lääkäriin. Lääkäri saattaa määrätä maksa‑ tai munuaistutkimuksia tai verikokeita, ja Apretude‑hoito saatetaan lopettaa.
Hyvin yleiset haittavaikutukset (voi esiintyä yli 1 käyttäjällä 10:stä)
- päänsärky
- ripuli
- pistoskohdan reaktiot
- hyvin yleiset: kipu (joka voi harvinaisissa tapauksissa aiheuttaa tilapäisiä vaikeuksia kävelyssä) ja epämukavuus, kova massa (kovettuma) tai kyhmy
- yleiset: punoitus, kutina, turvotus, kuumotus, tunnottomuus tai mustelmanmuodostus (värimuutoksia tai verenpurkauma ihon alla)
- melko harvinaiset: märkäpesäke
- kuumuuden tunne (kuume)
- verikokeissa näkyvät maksan toiminnan muutokset (transaminaasiarvojen suureneminen).
Yleiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 10:stä)
- masennus
- ahdistuneisuus
- poikkeavat unet
- nukkumisvaikeudet (unettomuus)
- huimaus
- pahoinvointi
- oksentelu
- vatsakipu
- ilmavaivat
- ihottuma
- lihaskipu
- energian puute (uupumus)
- yleinen huonovointisuus
Melko harvinaiset haittavaikutukset (voi esiintyä enintään 1 käyttäjällä 100:sta)
- itsemurhayritys
- itsemurha‑ajatukset (erityisesti henkilöillä, joilla on aikaisemmin ollut masennusta tai mielenterveysongelmia)
- allergiset reaktiot (yliherkkyys)
- nokkosihottuma
- turvotus (angioedeema), joskus kasvojen tai nielun turpoaminen, joka voi vaikeuttaa hengittämistä
- uneliaisuus
- painon nousu
- pyörrytys pistoksen aikana tai sen jälkeen (vasovagaaliset reaktiot). Tämä voi johtaa pyörtymiseen.
- maksavaurio (maksatoksisuus). Merkkejä voivat olla ihon ja silmänvalkuaisten kellastuminen, ruokahaluttomuus, kutina, vatsan aristus, vaaleat ulosteet tai epätavallisen tumma virtsa.
- verikokeissa näkyvä veren bilirubiiniarvon suureneminen. Bilirubiini on veren punasolujen hajoamistuote.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
00034 FIMEA
Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä etiketissä ja kotelossa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Lääkäri tai sairaanhoitaja vastaa tämän lääkkeen oikeasta säilyttämisestä.
Ei saa jäätyä.
Pakkauksen sisältö ja muuta tietoa
Mitä Apretude sisältää
Vaikuttava aine on kabotegraviiri.
Yksi 3 ml:n injektiopullo sisältää 600 mg kabotegraviiria.
Muut aineet ovat:
Mannitoli (E421)
Polysorbaatti 20 (E432)
Makrogoli (E1521)
Injektionesteisiin käytettävä vesi
Lääkevalmisteen kuvaus ja pakkauskoko (‑koot)
Kabotegraviiri on valkoinen tai hennon vaaleanpunainen suspensio, joka on pakattu ruskeaan, lasiseen injektiopulloon. Injektiopullossa on kumitulppa ja alumiinisinetti, jossa on muovinen nostokorkki.
Myyntiluvan haltija
ViiV Healthcare BV
Van Asch van Wijckstraat 55H
3811 LP Amersfoort
Alankomaat
Valmistaja
GlaxoSmithKline Manufacturing S.p.A.
Strada Provinciale Asolana 90
Torrile
PR
43056
Italia
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
Suomi/Finland
GlaxoSmithKline Oy
Puh/Tel: + 358 (0)10 30 30 30
Tämä pakkausseloste on tarkistettu viimeksi 12/2024
Muut tiedonlähteet
Lisätietoa tästä lääkevalmisteesta on saatavilla Euroopan lääkeviraston verkkosivulla https://www.ema.europa.eu .
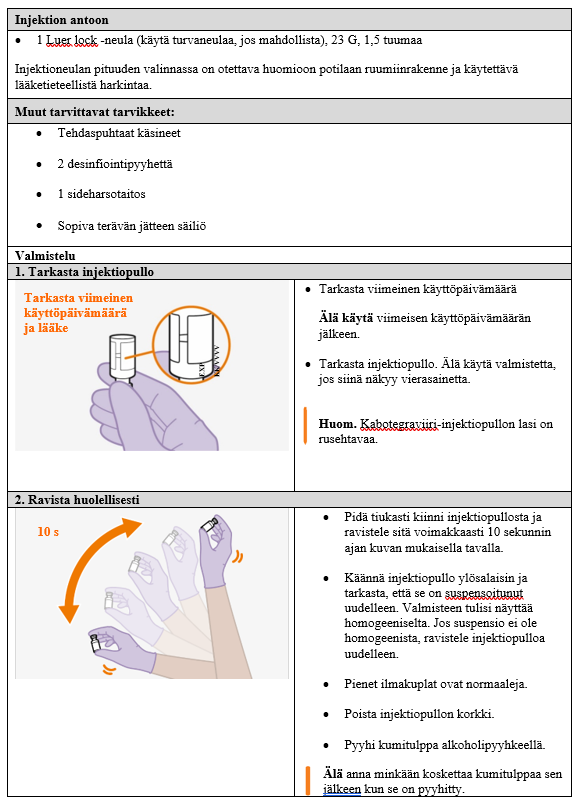
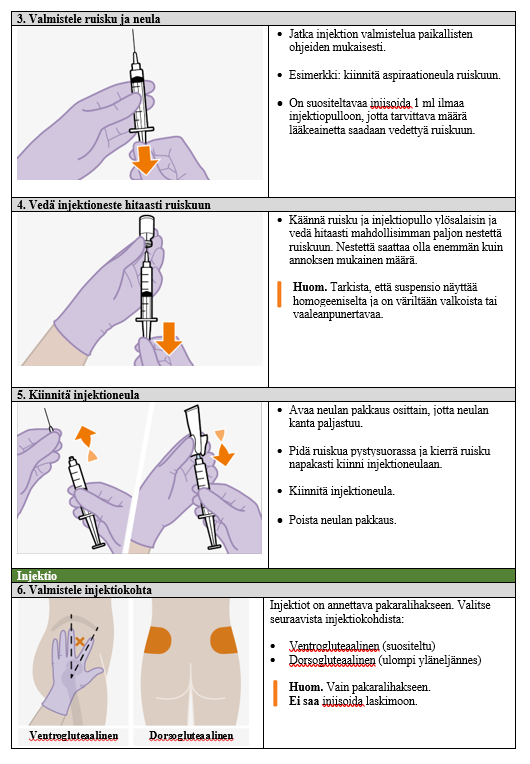
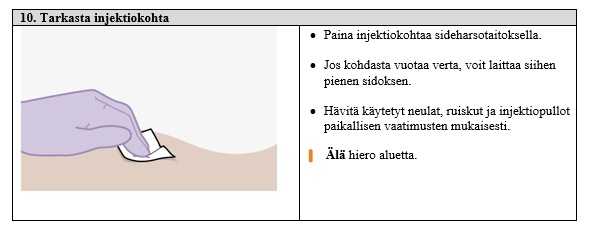
Ohjeet terveydenhuollon ammattilaiselle