Pakkausseloste
DOXYBACTIN VET tabletti 200 mg
ELÄINLÄÄKEVALMISTEEN NIMI
Doxybactin vet 200 mg tabletit koirille
doksisykliini
VAIKUTTAVAT JA MUUT AINEET
1 tabletti sisältää:
Vaikuttava aine:
200 mg doksisykliiniä doksisykliinihyklaattina
Keltainen, pyöreä ja kupera maustettu tabletti, jossa on ruskeita pilkkuja ja toisella puolella ristinmuotoinen jakouurre. Tabletit voidaan jakaa samankokoisiin puolikkaisiin tai neljänneksiin.
KÄYTTÖAIHEET
Seuraavien, doksisykliinille herkkien bakteerien aiheuttamien tautien hoito:
Riniitti (nenän limakalvon tulehdus), jonka aiheuttaja on Bordetella bronchiseptica tai Pasteurella spp.;
Bronkopneumonia (keuhkotulehdus), jonka aiheuttaja on Bordetella spp. Tai Pasteurella spp.;
Interstitiaalinen nefriitti (munuaistulehdus), jonka aiheuttaja on Leptospira spp.
VASTA-AIHEET
Ei saa käyttää tapauksissa, joissa esiintyy yliherkkyyttä tetrasykliineille tai apuaineille.
HAITTAVAIKUTUKSET
Doksisykliinihoidon haittavaikutuksina on hyvin harvoin raportoitu ruoansulatuskanavan oireita, kuten oksentelua, ripulia ja ruokatorventulehdusta.
Erittäin nuorilla eläimillä voi hyvin harvoin esiintyä hampaiden värjäytymistä tetrasykliinin sitoutuessa kalsiumfosfaattiin.
Voimakkaalle päivänvalolle altistumisen seurauksena voi hyvin harvoin ilmetä yliherkkyysreaktioita, valoherkkyyttä ja poikkeustapauksissa valoihottumaa.
Nuorilla eläimillä esiintyy hyvin harvoin muiden tetrasykliinien käytön yhteydessä luuston kasvun hidastumista (joka korjautuu hoidon lopettamisen jälkeen) ja sitä saattaa esiintyä myös doksisykliinin käytön yhteydessä.
Haittavaikutusten esiintyvyys määritellään seuraavasti:
- hyvin yleinen (useampi kuin 1/10 hoidettua eläintä saa haittavaikutuksen)
- yleinen (useampi kuin 1 mutta alle 10/100 hoidettua eläintä)
- melko harvinainen (useampi kuin 1 mutta alle 10 / 1 000 hoidettua eläintä)
- harvinainen (useampi kuin 1 mutta alle 10 / 10 000 hoidettua eläintä)
- hyvin harvinainen (alle 1 / 10 000 hoidettua eläintä, mukaan lukien yksittäiset ilmoitukset).
Jos havaitset haittavaikutuksia, myös sellaisia joita ei ole mainittu tässä pakkausselosteessa, tai olet sitä mieltä että lääke ei ole tehonnut, ilmoita asiasta eläinlääkärillesi.
KOHDE-ELÄINLAJI
Koira
ANNOSTUS, ANTOREITIT JA ANTOTAVAT KOHDE-ELÄINLAJEITTAIN
Suun kautta.
Suositeltu annos koirille on 10 mg doksisykliiniä elopainokiloa kohti vuorokaudessa. Useimmissa rutiinitapauksissa vaste ilmenee, kun hoito on kestänyt 5-7 vuorokautta. Hoitoa tulee jatkaa 2-3 vuorokautta akuutin infektion kliinisen paranemisen jälkeen. Krooniset ja uusiutuvat tulehdukset saattavat vaatia pitemmän, korkeintaan 14 vuorokauden hoitojakson. Leptospiroosin aiheuttamaa munuaistulehdusta sairastaville koirille suositellaan 14 vuorokauden hoitojaksoa. Oikean annoksen takaamiseksi eläimen paino on määritettävä mahdollisimman tarkasti. Näin voidaan välttää aliannostelua.
Seuraava taulukko on tarkoitettu valmisteen annostelun avuksi, kun tarkoitus on antaa ohjeannos eli 10 mg elopainokiloa kohti kerran vuorokaudessa.
| Kehon paino | Annos mg | Doxybactin vet 50 mg | Doxybactin vet 200 mg | Doxybactin vet 400 mg | ||
| 0,75 kg – 1,25 kg | 12,5 | - | - | |||
| >1,25 kg – 2,5 kg | 25 | - | - | |||
| >2,5 kg – 3,75 kg | 37,5 | - | - | |||
| >3,75 kg – 5 kg | 50 | - | - | |||
| >5 kg – 6,25 kg | 62,5 | - | - | |||
| >6,25 kg – 7,5 kg | 75 | - | - | |||
| >7,5 kg – 10 kg | 100 | - | - | |||
| >10 kg – 12,5 kg | 125 | - | - | |||
| >12,5 kg – 15 kg | 150 | - | ||||
| >15 kg – 20 kg | 200 | - | - | |||
| >20 kg – 25 kg | 250 | JA | - | |||
| >25 kg – 30 kg | 300 | - | - | |||
| >30 kg – 35 kg | 350 | - | - | |||
| >35 kg – 40 kg | 400 | - | - | |||
| >40 kg – 45 kg | 450 | JA | ||||
| >45 kg – 50 kg | 500 | - | JA | |||
| >50 kg – 60 kg | 600 | - | JA | |||
| >60 kg – 70 kg | 700 | - | JA | |||
| >70 kg – 80 kg | 800 | - | - | |||
![]() = ¼ tablettia
= ¼ tablettia ![]() = ½ tablettia
= ½ tablettia ![]() = ¾ tablettia
= ¾ tablettia ![]() = 1 tabletti
= 1 tabletti
ANNOSTUSOHJEET
Tabletit on annettava ruoan kanssa (katso kohta Erityisvaroitukset). Tarkan annostelun takaamiseksi tabletit voidaan jakaa samankokoisiin puolikkaisiin tai neljänneksiin. Aseta tabletti tasaiselle pinnalle siten, että sen jakouurteellinen puoli on ylöspäin ja kupera (pyöreä) puoli pintaa vasten.
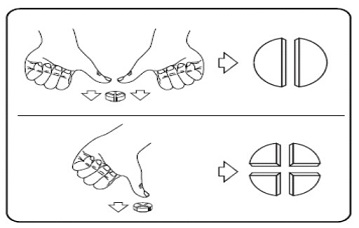
Samankokoiset puolikkaat: paina peukaloilla tabletin molempia sivuja.
Samankokoiset neljännekset: paina peukalolla tabletin keskeltä.
VAROAIKA
Ei oleellinen.
SÄILYTYSOLOSUHTEET
Ei lasten näkyville eikä ulottuville.
Säilytä alle 30 °C.
Älä käytä tätä eläinlääkevalmistetta pakkauksessa mainitun viimeisen käyttöpäivämäärän (EXP) jälkeen.
Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Jaettujen tablettien kestoaika: 3 vuorokautta
ERITYISVAROITUKSET
Eläimiä koskevat erityiset varotoimet:
Valmistetta on käytettävä varoen eläimille, joilla on dysfagia (nielemishäiriö) tai tauti, johon liittyy oksentelua, sillä doksisykliinihyklaattitablettien käyttö voi aiheuttaa ruokatorven haavaumia. Ruokatorven ärsytyksen ja muiden ruoansulatuskanavaan kohdistuvien haittavaikutusten todennäköisyyden pienentämiseksi valmiste on annettava ruoan kanssa.
Erityistä varovaisuutta on noudatettava käytettäessä valmistetta eläimillä, joilla on maksasairaus, sillä joillakin eläimillä on havaittu maksaentsyymien kohoamista doksisykliinihoidon jälkeen.
Valmisteen käytössä nuorilla eläimillä on noudatettava varovaisuutta, sillä tetrasykliinien ryhmään kuuluvat lääkkeet voivat aiheuttaa hampaiden pysyvää värjäytymistä, jos niitä käytetään hampaiden kehittymisvaiheen aikana. Ihmislääketieteen kirjallisuudessa on kuitenkin viitteitä siitä, että doksisykliini ei aiheuta tällaisia haittoja yhtä todennäköisesti kuin muut tetrasykliinit, koska se sitoo kalsiumia vähemmässä määrin.
Valmisteen käytön pitää perustua kohdepatogeenien tunnistamiseen ja herkkyystestaukseen. Jos tämä ei ole mahdollista, hoidon pitää perustua epidemiologiseen tietoon ja tietoon kohdepatogeenien herkkyydestä paikallisella/alueellisella tasolla. Valmistetta on käytettävä mikrobilääkkeitä koskevien virallisten, kansallisten ja alueellisten ohjeiden mukaisesti. Valmisteen käyttö muuten kuin valmisteyhteenvedon sisältämiä ohjeita noudattaen voi lisätä doksisykliinille vastustuskykyisten bakteerikantojen määrää ja heikentää muiden tetrasykliinien hoitotehoa mahdollisen ristiresistenssin takia.
Koska tabletit ovat maustettuja, säilytä tabletit poissa eläinten ulottuvilta tahattoman nielemisen välttämiseksi.
Erityiset varotoimenpiteet, joita eläinlääkevalmistetta antavan henkilön on noudatettava:
Tetrasykliinit voivat aiheuttaa yliherkkyysreaktioita (allergisia reaktioita).
Henkilöiden, jotka ovat yliherkkiä tetrasykliineille, tulee välttää kosketusta eläinlääkevalmisteen kanssa.
Jos sinulle kehittyy altistuksen seurauksena oireita, kuten ihottumaa, käänny välittömästi lääkärin puoleen ja näytä hänelle pakkausseloste.
Doksisykliini voi aiheuttaa haittoja ruoansulatuskanavassa, jos sitä niellään vahingossa, ja etenkin jos lapset nielevät sitä vahingossa. Jotta kukaan ei pääse vahingossa nielemään valmistetta (koskee etenkin lapsia), tablettien käyttämättä jääneet osat on asetettava takaisin läpipainopakkauksen tyhjään kohtaan ja läpipainopakkaus on pantava takaisin pahvirasiaan. Jos vahingossa nielet (tai etenkin jos lapsi vahingossa nielee) valmistetta, käänny lääkärin puoleen.
Pese kädet käytön jälkeen.
Tiineys ja imetys
Eläinlääkevalmisteen turvallisuutta tiineyden ja imetyksen aikana ei ole selvitetty. Tetrasykliinien ryhmään kuuluvat lääkkeet voivat hidastaa sikiön luuston kasvua (korjaantuu kokonaan) ) ja aiheuttaa maitohampaiden värjäytymistä. Ihmislääketieteen kirjallisuuden perusteella voidaan kuitenkin päätellä, että doksisykliini ei aiheuta tällaisia haittoja yhtä todennäköisesti kuin muut tetrasykliinit. Voidaan käyttää ainoastaan hoitavan eläinlääkärin tekemän hyöty-haitta-arvion perusteella.
Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset
Älä anna valmistetta samaan aikaan bakteereita tappavien antibioottien, kuten penisilliinien tai kefalosporiinien, kanssa. Oraalisia imeytysaineita ja multivalentteja kationeja sisältäviä aineita, kuten antasideja ja rautasuoloja, ei saa käyttää doksisykliinin antoa edeltävien kolmen tunnin eikä sitä seuraavien kolmen tunnin aikana. Epilepsialääkkeiden, kuten fenobarbitaalin ja fenytoiinin, samanaikainen käyttö lyhentää doksisykliinin puoliintumisaikaa.
Yliannostus (oireet, hätätoimenpiteet, vastalääkkeet):
Yliannostustapauksessa ei ole odotettavissa muita kuin haittavaikutuksia käsittelevässä kohdassa kuvattuja haittavaikutuksia.
ERITYISET VAROTOIMET KÄYTTÄMÄTTÖMÄN VALMISTEEN TAI JÄTEMATERIAALIN HÄVITTÄMISEKSI
Lääkkeitä ei saa heittää viemäriin eikä hävittää talousjätteiden mukana.
Kysy käyttämättömien lääkkeiden hävittämisestä eläinlääkäriltäsi tai apteekista.
Nämä toimenpiteet on tarkoitettu ympäristön suojelemiseksi.
PÄIVÄMÄÄRÄ, JOLLOIN PAKKAUSSELOSTE ON VIIMEKSI HYVÄKSYTTY
29.11.2022.
MUUT TIEDOT
Alumiini-PVC/PE/PVDC-läpipainopakkaus
Pahvirasia, joka sisältää 1, 2, 3 tai 10 läpipainopakkausta, joissa on kussakin 10 tablettia.
Pahvirasia, joka sisältää 10 erillistä pahvirasiaa, joista jokainen sisältää 1 läpipainopakkauksen, joka sisältää 10 tablettia.
Kaikkia pakkauskokoja ei välttämättä ole markkinoilla.
 Jakouurteellinen tabletti
Jakouurteellinen tabletti
MYYNTILUVAN HALTIJAN NIMI JA OSOITE SEKÄ ERÄN VAPAUTTAMISESTA VASTAAVAN VALMISTAJAN NIMI JA OSOITE EUROOPAN TALOUSALUEELLA, JOS ERI
Myyntiluvan haltija:
Dechra Regulatory B.V.
Handelsweg 25
5531 AE Bladel
Alankomaat
Erän vapauttamisesta vastaava valmistaja:
Lelypharma B.V.
Zuiveringsweg 42
8243 PZ Lelystad
Alankomaat
Genera Inc.
Svetonedeljska cesta 2
Kalinovica
10436 Rakov Potok
Kroatia
Painetussa pakkaussetelissä mainitaan ainoastaan tuotteen testauksen ja erien vapauttamisen sijaintipaikka.