CEFABACTIN VET tabletti 1000 mg
ELÄINLÄÄKEVALMISTEEN NIMI
Cefabactin vet 1000 mg tabletit koiralle
VAIKUTTAVAT JA MUUT AINEET
Yksi tabletti sisältää:
Vaikuttava aine:
Kefaleksiini (kefaleksiinimonohydraattina) 1000 mg
Vaaleanruskea ruskeapilkullinen tabletti, joka on muodoltaan pyöreä ja kupera ja jonka toisella puolella on ristin muotoinen jakouurre. Tabletissa on makuainetta.
Tabletin voi jakaa 2 tai 4 yhtä suureen osaan.
KÄYTTÖAIHEET
Seuraavien sairauksien hoitoon:
- hengitystieinfektiot, erityisesti bronkopneumonia, jonka aiheuttajia ovat Staphylococcus aureus, Streptococcus-lajit, Escherichia coli tai Klebsiella-lajit
- virtsatieinfektiot, joiden aiheuttajia ovat Escherichia coli, Proteus-lajit tai Staphylococcus-lajit
- ihoinfektiot, joiden aiheuttajia ovat Staphylococcus-lajit.
VASTA-AIHEET
Ei saa käyttää tapauksissa, joissa esiintyy yliherkkyyttä vaikuttavalle aineelle, muille kefalosporiineille, muille beetalaktaamiryhmän aineille tai apuaineille.
Ei saa käyttää tapauksissa, joissa kefalosporiini- tai penisilliiniresistenssi on tiedossa.
Ei saa käyttää kaneille, marsuille, hamstereille eikä gerbiileille.
HAITTAVAIKUTUKSET
Koira:
Harvinainen (1–10 eläintä 10 000 hoidetusta eläimestä): | Yliherkkyysreaktioa |
Hyvin harvinainen (< 1 eläin 10 000 hoidetusta eläimestä, yksittäiset ilmoitukset mukaan luettuina): | Oksentelu b, ripulib, Uneliaisuus |
a Hoito on keskeytettävä.
b Jos haittavaikutusta esiintyy toistuvasti, hoito on keskeytettävä ja hoitavalta eläinlääkäriltä on kysyttävä ohjeita.
Haittatapahtumista ilmoittaminen on tärkeää. Se mahdollistaa eläinlääkkeen turvallisuuden jatkuvan seurannan. Jos havaitset haittavaikutuksia, myös sellaisia, joita ei ole mainittu tässä pakkausselosteessa, tai olet sitä mieltä, että lääke ei ole tehonnut, ilmoita ensisijaisesti asiasta eläinlääkärillesi. Voit ilmoittaa kaikista haittavaikutuksista myös myyntiluvan haltijalle tai myyntiluvan haltijan paikalliselle edustajalle käyttämällä tämän pakkausselosteen lopussa olevia yhteystietoja tai kansallisen ilmoitusjärjestelmän kautta:
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
www-sivusto: https://www.fimea.fi/elainlaakkeet/
KOHDE-ELÄINLAJI
Koira.
ANNOSTUS, ANTOREITIT JA ANTOTAVAT KOHDE-ELÄINLAJEITTAIN
Suun kautta.
Suositeltu annos on 15–30 mg kefaleksiinia painokiloa kohti kahdesti vuorokaudessa vähintään 5 peräkkäisen päivän ajan. Vastaava eläinlääkäri voi määrätä pidemmän hoidon esimerkiksi silloin, kun kyse on virtsatieinfektioista tai bakteerien aiheuttamasta ihotulehduksesta.
Oikean annostuksen varmistamiseksi ja aliannostuksen välttämiseksi eläimen paino on määritettävä mahdollisimman tarkasti.
Seuraava taulukko on tarkoitettu ohjeeksi eläinlääkkeen annosteluun annoksella 15 mg kefaleksiinia painokiloa kohti kahdesti vuorokaudessa.
ANTO KAHDESTI VUOROKAUDESSA
| |||||
| Paino | Annos (mg) | Cefabactin vet 50 mg | Cefabactin vet 250 mg | Cefabactin vet 500 mg | Cefabactin vet 1 000 mg |
| > 0,5–0,8 kg | 12,5 | - | - | - | |
| > 0,8–1,6 kg | 25 | - | - | - | |
| > 1,6–2,5 kg | 37,5 | - | - | - | |
| > 2,5–3,3 kg | 50 | - | - | - | |
| > 3,3–5 kg | 75 | - | - | - | |
| > 5–6,6 kg | 100 | - | - | - | |
| > 6,6–8 kg | 125 | - | - | ||
| > 8–10 kg | 150 | - | - | - | |
| > 10–12,5 kg | 188 | - | - | - | |
| > 12,5–16,6 kg | 250 | - | - | ||
| > 16,6–20 kg | 313 | ||||
| > 20–25 kg | 375 | - | - | - | |
| > 25–29 kg | 438 | - | - | - | |
| > 29–33 kg | 500 | - | |||
| > 33–41 kg | 625 | - | - | - | |
| > 41–50 kg | 750 | - | - | ||
| > 50–58 kg | 875 | - | - | - | |
| > 58–66 kg | 1 000 | - | - | ||
| > 66–83 kg | 1 250 | - | - | - | |
![]() = ¼ tabletti
= ¼ tabletti ![]() = ½ tabletti
= ½ tabletti ![]() = ¾ tabletti
= ¾ tabletti ![]() = 1 tabletti
= 1 tabletti
ANNOSTUSOHJEET
Tabletit voidaan jakaa 2 tai 4 yhtä suureen osaan tarkan annostelun takaamiseksi. Aseta tabletti tasaiselle pinnalle niin, että jakouurre osoittaa ylöspäin.
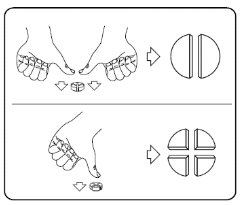
Jos haluat puolittaa tabletin, paina tablettia peukaloilla alaspäin sen kummaltakin reunalta.
Jos haluat jakaa tabletin neljään osaan, paina tablettia peukalolla alaspäin sen keskikohdasta.
VAROAIKA
Ei oleellinen.
SÄILYTYSOLOSUHTEET
Ei lasten näkyville eikä ulottuville.
Ei erityisiä säilytysohjeita.
Jaettujen tablettien kestoaika: 4 vuorokautta.
Älä käytä tätä eläinlääkettä viimeisen käyttöpäivämäärän jälkeen, joka on ilmoitettu ulkopakkauksessa ja läpipainopakkauksessa merkinnän Exp. jälkeen.
Viimeisellä käyttöpäivämäärällä tarkoitetaan kuukauden viimeistä päivää.
ERITYISVAROITUKSET
Erityiset varotoimet, jotka liittyvät turvalliseen käyttöön kohde-eläinlajilla:
Koska kefaleksiinille resistenttien bakteerien esiintyvyydessä on todennäköisesti (ajallista ja maantieteellistä) vaihtelua, suositellaan bakteerinäytteen ottoa ja herkkyysmäärityksen tekemistä.
Eläinlääkettä on käytettävä vain eläimistä eristettyjen bakteerien herkkyysmäärityksen perusteella. Jos tämä ei ole mahdollista, hoidon on pohjauduttava paikalliseen tietoon taudinaiheuttajan herkkyydestä.
Eläinlääkkeen käytössä on noudatettava virallisia, kansallisia ja alueellisia mikrobilääkkeiden käyttöohjeita.
Tämän pakkausselosteen ohjeista poikkeava eläinlääkkeen käyttö saattaa lisätä kefaleksiinille resistenttien bakteerien yleisyyttä ja heikentää muilla beetalaktaamiantibiooteilla tapahtuvan hoidon tehoa mahdollisen ristiresistenssin vuoksi.
Jos eläimellä on krooninen munuaisten vajaatoiminta, annosta tulee pienentää tai annosväliä kasvattaa. Tableteissa on makuainetta. Säilytä tabletteja eläinten ulottumattomissa, etteivät eläimet syö niitä vahingossa.
Erityiset varotoimenpiteet, joita eläinlääkettä eläimille antavan henkilön on noudatettava:
Penisilliinit ja kefalosporiinit voivat aiheuttaa yliherkkyyttä (allergiaa) injisoinnin, hengittämisen, nielemisen tai ihokosketuksen seurauksena. Yliherkkyys penisilliinille voi aiheuttaa ristireaktion kefalosporiinille ja päinvastoin. Allergiset reaktiot näille aineille voivat joskus olla vakavia. Älä käsittele tätä eläinlääkettä, jos tiedät olevasi herkistynyt sille tai jos sinua on kehotettu välttämään kosketusta tällaisten aineiden kanssa.
Käsittele tätä eläinlääkettä hyvin varovaisesti, jotta et altistuisi sille, ja huolehdi kaikista suositelluista varotoimista. Jos sinulle kehittyy altistuksen jälkeen oireita, kuten ihottumaa, käänny lääkärin puoleen ja näytä hänelle tämä varoitus. Kasvojen, huulten tai silmien alueen turvotus taikka hengitysvaikeudet ovat vakavampia oireita ja vaativat kiireellistä lääkärinhoitoa.
Jaetut tai käyttämättömät tabletit on palautettava avoimeen läpipainotaskuun ja asetettava takaisin ulkopakkaukseen, jotta lapset eivät pääse vahingossa nielemään eläinlääkettä.
Jos vahingossa nielet valmistetta, käänny välittömästi lääkärin puoleen ja näytä hänelle pakkausseloste tai myyntipäällys.
Pese kädet käytön jälkeen.
Tiineys ja laktaatio:
Laboratoriotutkimuksissa rotilla ja hiirillä ei ole löydetty näyttöä sikiölle haitallisista vaikutuksista.
Eläinlääkkeen turvallisuutta koiran tiineyden ja laktaation aikana ei ole selvitetty. Voidaan käyttää ainoastaan hoitavan eläinlääkärin hyöty-riskiarvion perusteella.
Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset:
Tehon varmistamiseksi eläinlääkevalmistetta ei saa käyttää yhdessä bakteriostaattisten (bakteerien kasvua ja lisääntymistä estävien) antibioottien (makrolidit, sulfonamidit ja tetrasykliinit) kanssa.
Ensimmäisen polven kefalosporiinien samanaikainen käyttö aminoglykosidiantibioottien tai joidenkin virtsaneritystä lisäävien lääkeaineiden, kuten furosemidin, kanssa saattaa lisätä munuaisvaurion riskiä.
Yliannostus:
Muita kuin kohdassa Haittatapahtumat mainittuja haittavaikutuksia ei tunneta.
Yliannostustapauksessa hoidon on oltava oireenmukaista.
ERITYISET VAROTOIMET KÄYTTÄMÄTTÖMÄN VALMISTEEN TAI JÄTEMATERIAALIN HÄVITTÄMISEKSI
Lääkkeitä ei saa kaataa viemäriin eikä hävittää talousjätteiden mukana.
Eläinlääkkeiden tai niiden käytöstä syntyvien jätemateriaalien hävittämisessä käytetään paikallisia palauttamisjärjestelyjä sekä kyseessä olevaan eläinlääkkeeseen sovellettavia kansallisia keräysjärjestelmiä. Näiden toimenpiteiden avulla voidaan suojella ympäristöä.
Kysy käyttämättömien lääkkeiden hävittämisestä eläinlääkäriltäsi tai apteekista.
PÄIVÄMÄÄRÄ, JOLLOIN PAKKAUSSELOSTE ON VIIMEKSI HYVÄKSYTTY
10.12.2025
Tätä eläinlääkettä koskevaa yksityiskohtaista tietoa on saatavilla unionin valmistetietokannassa (https://medicines.health.europa.eu/veterinary).
MYYNTILUVAN HALTIJAN NIMI JA OSOITE SEKÄ ERÄN VAPAUTTAMISESTA VASTAAVAN VALMISTAJAN NIMI JA OSOITE EUROOPAN TALOUSALUEELLA, JOS ERI
Myyntiluvan haltija:
Le Vet. Beheer B.V.
Wilgenweg 7
3421 TV Oudewater
Alankomaat
Erän vapauttamisesta vastaava valmistaja:
LelyPharma B.V.
Zuiveringweg 42
8243 PZ Lelystad
Alankomaat
Paikalliset edustajat ja yhteystiedot epäillyistä haittatapahtumista ilmoittamista varten:
Dechra Veterinary Products Oy
Yliopistonkatu 31
20100 Turku
Suomi
Puh.: +358 (0)22510500