OCTAPLEX infuusiokuiva-aine ja liuotin, liuosta varten 500 IU, 1000 IU
Octaplex 500 IU infuusiokuiva-aine ja liuotin, liuosta varten
Octaplex 1000 IU infuusiokuiva-aine ja liuotin, liuosta varten
Ihmisen protrombiinikompleksi
Yleisiä ohjeita
Lue tämä pakkausseloste huolellisesti ennen kuin aloitat tämän lääkkeen käyttämisen, sillä se sisältää sinulle tärkeitä tietoja.
- Säilytä tämä pakkausseloste. Voit tarvita sitä myöhemmin.
- Jos sinulla on kysyttävää, käänny lääkärin, apteekkihenkilökunnan tai sairaanhoitajan puoleen.
- Tämä lääke on määrätty vain sinulle eikä sitä pidä antaa muiden käyttöön. Se voi aiheuttaa haittaa muille, vaikka heillä olisikin samanlaiset oireet kuin sinulla.
- Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Ks. kohta Mahdolliset haittavaikutukset.
Tässä pakkausselosteessa kerrotaan
- Mitä Octaplex on ja mihin sitä käytetään
- Mitä sinun on tiedettävä, ennen kuin käytät Octaplex-valmistetta
- Miten Octaplex‑valmistetta käytetään
- Mahdolliset haittavaikutukset
- Octaplex-valmisteen säilyttäminen
- Pakkauksen sisältö ja muuta tietoa
Mitä valmiste on ja mihin sitä käytetään
Octaplex kuuluu sellaiseen lääkeryhmään, jota sanotaan hyytymistekijöiksi. Se sisältää K-vitamiinista riippuvaisia ihmisen veren hyytymistekijöitä II, VII, IX ja X.
Octaplex-valmistetta käytetään verenvuodon hoitoon ja ehkäisyyn seuraavissa tapauksissa:
- Kun verenvuodon aiheuttaa joku K-vitamiiniantagonistiksi nimitetty lääke (kuten varfariini).
Nämä lääkkeet estävät K-vitamiinin vaikutuksen ja aiheuttavat elimistössä K-vitamiinista riippuvaisten hyytymistekijöiden II ja X puutosta. Octaplex-valmistetta käytetään, kun puutos täytyy saada nopeasti korjatuksi. - Jos potilaalla on syntymästään asti jonkun K-vitamiinista riippuvaisen hyytymistekijän puutos.
Octaplex-valmistetta käytetään, kun saatavana ei ole juuri tarvittavaa hyytymistekijää puhdistettuna.
Mitä sinun on tiedettävä ennen valmisteen käyttöä
Älä käytä Octaplex-valmistetta
- jos olet allerginen jollekin valmisteen aineelle (lueteltu kohdassa Pakkauksen sisältö ja muuta tietoa).
- jos olet allerginen hepariinille tai se on aiemmin vähentänyt verihiutaleittesi määrää.
- jos sinulla on IgA:n puutostila ja sinulle on kehittynyt IgA:n vasta-aineita.
Varoitukset ja varotoimet
- Kysy neuvoa hyytymishäiriöiden hoitoon erikoistuneelta lääkäriltä, jos tarvitset Octaplex-valmistetta.
- Jos sairastat hankinnaista K-vitamiinista riippuvaisen hyytymistekijän puutosta (joka saattaa johtua esimerkiksi K-vitamiiniantagonistilääkkeiden käytöstä), tätä valmistetta on syytä käyttää vain, jos puutoksen nopea korjaus on tarpeen, kuten suuren verenvuodon tai päivystysleikkauksen yhteydessä. Muissa tapauksissa riittää usein, että potilaalle annetaan K-vitamiinia ja/tai K‑vitamiiniantagonistilääkkeen annosta pienennetään.
- Jos käytät K-vitamiiniantagonistilääkettä (kuten varfariinia), sinulle saattaa tulla verihyytymiä tavallista helpommin. Siinä tapauksessa Octaplex-valmisteen käyttö saattaa lisätä verihyytymien riskiä.
- Jos sinulla on ollut syntymästäsi lähtien K-vitamiinista riippuvaisen hyytymistekijän puutosta, on parasta käyttää nimenomaan tarvitsemaasi hyytymistekijää, jos sitä on saatavilla.
- Allergisen tai anafylaktisen reaktion sattuessa lääkäri keskeyttää infuusion heti ja antaa tarvittavan hoidon.
- Octaplex-valmistetta käytettäessä (erityisesti jos sitä käytetään säännöllisesti) on vaarana disseminoitunut intravaskulaarinen koagulaatio (vakava sairaus, jossa muodostuu verihyytymiä ympäri kehoa). Potilaan tilaa on seurattava tarkasti näihin viittaavien merkkien ja oireiden varalta.
Tämä on erityisen tärkeää, jos sinulla on sepelvaltimotauti tai maksasairaus, jos sinulle aiotaan tehdä leikkaus tai jos Octaplex-valmistetta annetaan aivan pienelle vauvalle. - Octaplex-valmisteen käytöstä vastasyntyneiden K-vitamiininpuutoksesta johtuvan verenvuodon hoidossa synnytyksen yhteydessä ei ole tietoa.
Virusturvallisuus
- Kun ihmisverestä tai ‑plasmasta valmistetaan lääkkeitä, tehdään tiettyjä toimenpiteitä, joiden tarkoituksena on tartuntojen välttäminen. Esimerkiksi veren ja plasman luovuttajat valitaan huolellisesti, jottei mukaan pääsisi tartunnankantajia, ja jokainen luovutuserä ja yhdistetty plasmaerä tarkistetaan virusten ja infektioiden varalta. Lisäksi verelle ja plasmalle tehdään toimenpiteitä, joiden avulla viruksia pystytään tekemään toimintakyvyttömiksi tai poistamaan. Silti ihmisen verestä tai plasmasta tehtyjä lääkevalmisteita käytettäessä tartunnan vaaraa ei pystytä sulkemaan kokonaan pois. Tämä pätee myös tuntemattomiin ja uusiin viruksiin ja muuntyyppisiin tartuntoihin.
- Käytettyjen toimenpiteiden katsotaan tehoavan vaipallisiin viruksiin, joita ovat esimerkiksi immuunikatovirus (HIV), hepatiitti B -virus (HBV) ja hepatiitti C -virus (HCV). Niistä saattaa olla jonkin verran hyötyä myös hepatiitti A -viruksen (HAV) ja parvovirus B19:n kaltaisia vaipattomia viruksia vastaan. Parvovirus B19 ‑infektio voi olla vakava, jos potilas on raskaana (sikiön infektio) tai sairastaa immuunijärjestelmän vajaatoimintaa tai tietynlaista anemiaa (kuten sirppisoluanemiaa tai hemolyyttistä anemiaa).
- Valmisteen nimi ja eränumero on syytä kirjata joka kerta, kun saat Octaplex-annoksen, että käytetty erä on jäljitettävissä.
- Asianmukaiset rokotukset (hepatiitti A:ta ja B:tä vastaan) ovat paikallaan, jos saat säännöllisesti tai toistuvasti ihmisen plasmasta tehtyjä protrombiinikompleksivalmisteita.
Lapset ja nuoret
Tietoja ei ole saatavilla Octaplex-valmisteen käytöstä lapsille ja nuorille.
Muut lääkevalmisteet ja Octaplex
Octaplex-valmistetta ei saa sekoittaa yhteen muiden lääkeaineiden kanssa.
Octaplex estää K-vitamiiniantagonistilääkkeiden (kuten varfariinin) vaikutukset, mutta yhteisvaikutuksia muiden lääkkeiden kanssa ei tunneta.
Octaplex saattaa vaikuttaa hepariinille herkkien hyytymistestien tuloksiin.
Kerro lääkärille tai apteekkihenkilökunnalle, jos parhaillaan käytät tai olet äskettäin käyttänyt tai saatat käyttää muita lääkkeitä.
Raskaus ja imetys
Octaplex-valmistetta tulisi käyttää raskauden ja imetyksen aikana vain, mikäli käyttö on ehdottomasti tarpeen. Kysy lääkäriltä tai apteekista neuvoa ennen minkään lääkkeen käyttöä.
Ajaminen ja koneiden käyttö
Octaplex-valmisteen vaikutusta ajokykyyn ja koneiden käyttökykyyn ei tiedetä.
Tärkeää tietoa Octaplex-valmisteen sisältämistä aineista
Hepariini saattaa aiheuttaa allergisia reaktioita ja vähentää verihiutaleiden määrää, mikä voi vaikuttaa veren hyytymiseen. Potilaiden, joilla on ollut hepariinin aiheuttamia allergisia reaktioita, pitää välttää hepariinia sisältävien lääkkeiden käyttöä.
- Tämä lääkevalmiste sisältää natriumia (ruokasuolan toinen ainesosa) 75–125 mg per 500 IU:n injektiopullo tai 150–200 mg per 1000 IU:n injektiopullo. Tämä vastaa 3,8–6,3 % tai 7,5–12,5 % suositellusta natriumin enimmäisvuorokausiannoksesta aikuiselle.
Miten valmistetta käytetään
Hoito on aloitettava hyytymishäiriöiden hoitoon perehtyneen lääkärin valvonnassa.
- Kuiva-aine liuotetaan ensin veteen.
- Liuos annetaan laskimoon.
Tarvittava Octaplex-annos ja hoidon kesto riippuvat seuraavista seikoista:
- kuinka vakava sairautesi on,
- missä ja kuinka vakava verenvuoto on, sekä
- minkälainen terveydentilasi on.
Jos käytät enemmän Octaplex-valmistetta kuin sinun pitäisi
Yliannostuksen sattuessa seuraavien riski on tavallista suurempi:
- hyytymiseen liittyvät komplikaatiot (kuten sydäninfarkti tai hyytymät laskimoissa tai keuhkoissa)
- disseminoitunut intravaskulaarinen koagulaatio (vakava sairaus, jossa hyytymiä muodostuu ympäri kehoa).
Mahdolliset haittavaikutukset
Kuten kaikki lääkkeet, tämäkin lääke voi aiheuttaa haittavaikutuksia. Kaikki eivät kuitenkaan niitä saa.
Yleiset (yli 1 potilaalla sadasta)
Verisuonien tukokset.
Melko harvinaiset (alle 1 potilaalla sadasta)
Ahdistuneisuus, kohonnut verenpaine, astman kaltaiset oireet, veriyskä, nenäverenvuoto, injektiokohdan kuumotus, tukos laitteessa.
Harvinaiset (alle 1 potilaalla tuhannesta)
Allergistyyppisiä reaktioita voi esiintyä. Maksakoetulosten (transaminaasiarvojen) tilapäistä kohoamista on havaittu harvinaisissa tapauksissa.
Octaplex-valmisteella korvaushoitona hoidetuille potilaille saattaa kehittyä neutraloivia vasta-aineita (inhibiittoreita) jotakin valmisteen sisältämää hyytymistekijää vastaan. Jos vasta-aineita syntyy, korvaushoito ei tehoa kovin hyvin.
Hyvin harvinaiset (alle 1 potilaalla kymmenestätuhannesta)
Lämmönnousua (kuumetta) on esiintynyt.
Kun potilaalle annetaan tätä lääkettä, verihyytymien riski lisääntyy.
Tuntematon (koska saatavissa oleva tieto ei riitä arviointiin)
Vakava allerginen reaktio ja sokki, yliherkkyys, vapina, sydämenpysähdys, sydämen tiheälyöntisyys, verenkierron romahtaminen, epänormaalin matala verenpaine, kohonnut verenpaine, hengenahdistus, hengitysvajaus, pahoinvointi, nokkosihottuma, ihotulehdus, vilunväristykset.
Valmiste sisältää hepariinia. Hepariini saattaa aiheuttaa äkillisen vähenemisen verihiutaleiden määrässä. Tätä allergista reaktiota kutsutaan nimellä ”hepariinista johtuva trombosytopenia tyyppi II”. Harvinaisissa tapauksissa verihiutaleiden määrän väheneminen saattaa ilmetä 6-14 päivän kuluessa potilailla, jotka eivät ole aiemmin saaneet allergista reaktiota hepariinista. Hepariinille yliherkkien potilaiden reaktio saattaa ilmetä muutaman tunnin kuluessa hoidon aloittamisesta.
Octaplexin käyttö on välittömästi lopetettava, jos allerginen reaktio ilmenee. Näillä potilailla ei voi jatkossakaan käyttää hepariinia sisältäviä valmisteita.
Virustartuntojen torjunnasta on lisätietoa kohdassa Mitä sinun on tiedettävä ennen valmisteen käyttöä.
Haittavaikutuksista ilmoittaminen
Jos havaitset haittavaikutuksia, kerro niistä lääkärille, apteekkihenkilökunnalle tai sairaanhoitajalle. Tämä koskee myös sellaisia mahdollisia haittavaikutuksia, joita ei ole mainittu tässä pakkausselosteessa. Voit ilmoittaa haittavaikutuksista myös suoraan (katso tarkemmat tiedot jäljempänä). Ilmoittamalla haittavaikutuksista voit auttaa saamaan enemmän tietoa tämän lääkevalmisteen turvallisuudesta.
www-sivusto: www.fimea.fi
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
Lääkkeiden haittavaikutusrekisteri
PL 55
FI-00034 Fimea
Valmisteen säilyttäminen
Ei lasten ulottuville eikä näkyville.
Älä käytä tätä lääkettä pakkauksessa mainitun viimeisen käyttöpäivämäärän jälkeen. Viimeinen käyttöpäivämäärä tarkoittaa kuukauden viimeistä päivää.
Säilytä alle 25 °C. Ei saa jäätyä. Säilytä alkuperäispakkauksessa. Herkkä valolle.
Kuiva-aine liuotetaan vasta juuri ennen injektiota. Liuoksen on osoitettu säilyvän stabiilina enintään 8 tunnin ajan 25 °C lämpötilassa. Kontaminaation ehkäisemiseksi liuos on kuitenkin hyvä käyttää välittömästi ja yhdellä kerralla.
Pakkauksen sisältö ja muuta tietoa
Mitä Octaplex sisältää yhdessä injektiopullollisessa liuosta, joka on tehty käyttövalmiiksi lisäämällä 20 ml (500 IU) tai 40 ml (1000 IU) liuotinta
Vaikuttavat aineet ovat:
| Aine | Octaplex määrä / 500 IU:n injektiopullo | Octaplex määrä / 1000 IU:n injektiopullo | Octaplex määrä/ml käyttövalmista liuosta |
| Proteiinien kokonaismäärä: | 260–820 mg | 520–1640 mg | 13–41 mg/ml |
| Vaikuttavat aineet | |||
| Ihmisen hyytymistekijä II | 280–760 IU | 560–1520 IU | 14–38 IU/ml |
| Ihmisen hyytymistekijä VII | 180–480 IU | 360–960 IU | 9–24 IU/ml |
| Ihmisen hyytymistekijä IX | 500 IU | 1000 IU | 25 IU/ml |
| Ihmisen hyytymistekijä X | 360–600 IU | 720–1200 IU | 18–30 IU/ml |
| Muut vaikuttavat aineet | |||
| C-proteiini | 260–620 IU | 520–1240 IU | 13–31 IU/ml |
| S-proteiini | 240–640 IU | 480–1280 IU | 12–32 IU/ml |
Tuotteen spesifinen aktiivisuus on ≥ 0,6 IU/mg tekijän IX spesifisenä aktiivisuutena ilmaistuna.
Muut aineet ovat:
hepariini, trinatriumsitraattidihydraati, injektionesteisiin käytettävä vesi.
Lääkevalmisteen kuvaus ja pakkauskoko
Octaplex-pakkauksessa on infuusiokuiva-ainetta ja liuotinta liuosta varten. Kuiva-aine on hygroskooppinen, valkoinen tai hieman värillinen, irtonainen jauhe tai mureneva massa lasisessa injektiopullossa. Liuotin on injektionesteisiin käytettävä vesi lasisessa injektiopullossa. Käyttövalmis liuos on kirkas tai hieman samea ja se voi olla värillinen.
Octaplex myydään kartonkilaatikossa, jossa on
- yksi pullollinen infuusiokuiva-ainetta liuosta varten
- yksi pullollinen liuotinta, injektionesteisiin käytettävää vettä
- yksi Nextaro-siirtopakkaus.
Myyntiluvan haltija ja valmistaja
Myyntiluvan haltija:
Octapharma AB
S-112 75 Stockholm
Ruotsi
Valmistaja:
Octapharma Pharmazeutika Produktionsges.m.b.H.
Oberlaaer Str. 235
1100 Vienna
Itävalta
tai
Octapharma Lingolsheim S.A.S.
72 Rue du Maréchal Foch
67380 Lingolsheim
Ranska
Lisätietoja tästä lääkevalmisteesta antaa myyntiluvan haltijan paikallinen edustaja:
Octapharma AB
Rajatorpantie 41 C
01640 Vantaa
Suomi
Tällä lääkevalmisteella on myyntilupa Euroopan talousalueeseen kuuluvissa jäsenvaltioissa seuraavilla kauppanimillä:
Itävalta, Belgia, Bulgaria, Kroatia, Kypros, Tanska, Viro, Suomi, Ranska, Saksa, Unkari, Islanti, Irlanti, Latvia, Liettua, Luxemburg, Malta, Hollanti, Norja, Puola, Portugali, Slovenia, Slovakia, Espanja, Iso-Britannia: Octaplex
Tsekki, Ruotsi: Ocplex
Italia, Romania: Pronativ
Tämä pakkausseloste on tarkistettu viimeksi 26.6.2024.
Ohjeet terveydenhuollon ammattilaiselle
Kohdassa Miten valmistetta käytetään on yleisiä ohjeita Octaplexin käytöstä.
Seuraavat tiedot on tarkoitettu vain terveydenhuollon ammattilaisille:
Hoito-ohjeet
Lue kaikki ohjeet, ja noudata niitä tarkasti!
Seuraavat toimenpiteet on tehtävä steriilisti!
Tuote liukenee nopeasti huoneenlämmössä kirkkaaksi tai hieman sameaksi liuokseksi. Älä käytä liuosta, jos se on läpinäkymätöntä tai siinä on sakkaa. Tarkista ennen annostelua silmämääräisesti, että liuos ei sisällä hiukkasia eikä ole värjäytynyt.
Käyttövalmis liuos täytyy käyttää heti.
Käyttämätön valmiste tai jäte on hävitettävä paikallisten vaatimusten mukaisesti.
Annos
Verenvuoto ja vuodon ehkäisy K-vitamiiniantagonistihoidon aikana:
Annos riippuu hoitoa edeltävästä INR-arvosta (international normalized ratio) ja painosta. Seuraavassa taulukossa on mainittu likimääräiset annokset (yksikköä käyttövalmista liuosta painokiloa kohti).
| Hoitoa edeltävä INR | 2 – < 4 | 4 – 6 | > 6 |
|---|---|---|---|
| Octaplex-annos (tekijä IX -yksikköä†) / painokilo | 25 | 35 | 50 |
| † Yksiköillä viitataan kansainvälisiin yksikköihin. | |||
Annos perustuu enintään 100 kg:n painoon. Jos potilaan paino on yli 100 kg, suurin sallittu kerta-annos (IU tekijää IX) ei siis saa olla yli 2 500 IU INR-arvolla 2 – < 4, 3 500 IU INR-arvolla 4 – 6 ja 5 000 IU INR-arvolla > 6.
Koska nämä suositukset perustuvat kokeellisiin havaintoihin, ja toipuminen ja vaikutuksen kesto saattavat vaihdella, INR-arvoa on seurattava hoidon aikana.
Verenvuoto ja perioperatiivinen vuodon ehkäisy potilailla, joilla on synnynnäinen K-vitamiinista riippuvaisten hyytymistekijöiden II ja X puute, silloin kun spesifistä hyytymistekijävalmistetta ei ole saatavilla:
Laskettu hoitoannos perustuu siihen kokeelliseen havaintoon, että noin 1 IU tekijää II lisää tekijän II aktiivisuutta plasmassa 0,02 IU/ml ja 1 IU tekijää X tekijän X aktiivisuutta vastaavasti 0,017 IU/ml.
Tarvittava yksikkömäärä = paino (kg) x haluttu hyytymistekijän X aktiivisuuden lisäys (IU/ml) x 60, missä 60 (ml/kg) on arvioidun korjautumisen korjauskerroin.
Tarvittava tekijän II annostus:
Tarvittava yksikkömäärä = paino (kg) x haluttu hyytymistekijän II aktiivisuuden lisäys (IU/ml) x 50.
Jos tiedetään, paljonko kyseisen potilaan arvo on aiemmin korjautunut, laskelmat on tehtävä sen perusteella.
Liuotusohjeet:
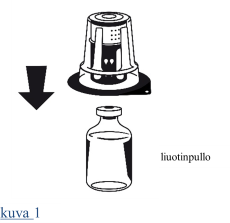 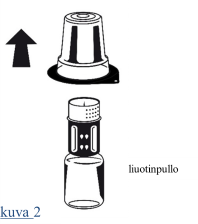 | 1. Anna suljetuissa injektiopulloissa olevien liuottimen (injektionesteisiin käytettävä vesi) ja infuusiokuiva-aineen tarvittaessa lämmetä huoneenlämpöisiksi. Tämä lämpötila tulee ylläpitää liuottamisen ajan. 2. Irrota kuiva-ainepullosta ja liuotinpullosta niiden irti napsautettavat korkit, ja desinfioi kummankin pullon kumitulpat asianmukaisesti. 3. Avaa Nextaro-pakkaus vetämällä suljin auki. Aseta liuotinpullo tasaiselle alustalle ja pidä siitä tukevasti kiinni. Poistamatta Nextaro-adapteria ulkopakkauksestaan aseta sen sininen osa liuotinpulloa vasten ja paina tiukasti, kunnes kuulet napsahduksen (kuva 1). Kiinnityksen yhteydessä osia ei saa kiertää! Pidä kiinni liuotinpullosta ja poista varovaisesti Nextaro-laitteen pakkaus. Huolehdi siitä, että Nextaro jää kunnolla kiinni liuotinpulloon (kuva 2). |
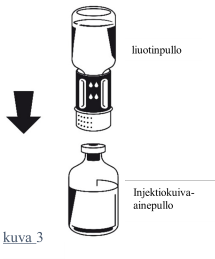 | 4. Aseta kuiva-ainepullo tasaiselle alustalle ja pidä siitä tukevasti kiinni. Käännä liuotinpullo, johon Nextaro on kiinnitetty, ylösalaisin. Aseta Nextaro-liittimen valkoinen osa kuiva-ainepulloa (jauhe) vasten ja paina lujasti, kunnes kuulet napsahduksen (kuva 3). Kiinnityksen yhteydessä osia ei saa kiertää! Liuotin valuu automaattisesti kuiva-ainepulloon. |
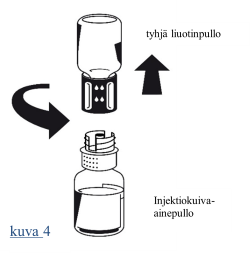 | 5. Pidä molemmat injektiopullot edelleen kiinni toisissaan ja pyöritä kuiva-ainepulloa varovasti, kunnes valmiste on liuennut. Hävitä tyhjä liuotinainepullo ja siinä oleva Nextaro‑adapterin sininen osa. |
Jos kuiva-aine ei liukene kokonaan tai muodostuu sakkaa, älä käytä valmistetta.
Infuusio-ohjeet:
Varotoimenpiteenä potilaalta mitataan pulssi ennen infuusiota ja sen aikana. Jos pulssi nopeutuu selvästi, infuusiota täytyy hidastaa tai se täytyy keskeyttää.
- Kiinnitä yksi 20 ml:n (500 IU) tai 40 ml:n (1 000 IU) ruisku Nextaro-adapterin luer lock -portin valkoiseen osaan. Käännä pullo ylösalaisin ja vedä liuos ruiskuun. Kun liuos on siirretty, pidä ruiskun männästä tukevasti kiinni (ruisku edelleen ylösalaisin) ja irrota ruisku Nextaro-adapterista. Hävitä Nextaro sekä tyhjä injektiopullo.
- Desinfioi aiottu injektiokohta asianmukaisesti.
- Ruiskuta liuos hitaasti laskimoon infuusionopeudella 0,12 ml/kg/min (noin 3 yksikköä/kg/min); enimmäisnopeus on 8 ml/min (noin 210 yksikköä/min). Infuusio annetaan aseptisesti.
Ruiskuun ei saa päästä verta, jottei muodostuisi fibriinihyytymiä. Nextaro on tarkoitettu kertakäyttöön.