METROBACTIN VET tabletti 250 mg
ELÄINLÄÄKEVALMISTEEN NIMI
Metrobactin vet 250 mg tabletit koiralle ja kissalle
VAIKUTTAVAT JA MUUT AINEET
Yksi tabletti sisältää:
Vaikuttava aine:
Metronidatsoli 250 mg
Vaaleanruskea, ruskeapilkullinen, pyöreä ja kupera maustettu tabletti, jonka toisella puolella on ristinmuotoinen jakouurre.
Tabletin voi jakaa kahteen tai neljään yhtä suureen osaan.
KÄYTTÖAIHEET
Giardia spp:n ja Clostridium spp:n (ts. C. perfringens tai C. difficile) aiheuttamien mahasuolikanavan infektioiden hoito.
Obligatorisesti anaerobisten bakteerien (esim. Clostridium spp.) aiheuttamien virtsa- ja sukupuolielin-, suuontelo-, nielu- ja ihoinfektioiden hoito.
VASTA-AIHEET
Ei saa käyttää tapauksissa, joissa esiintyy maksan maksasairauksia.
Ei saa käyttää tapauksissa, joissa esiintyy yliherkkyyttä vaikuttavalle aineelle tai apuaineille.
HAITTAVAIKUTUKSET
Koira, kissa
Hyvin harvinainen (< 1 eläin 10 000 hoidetusta eläimestä, yksittäiset ilmoitukset mukaan luettuina): | Neurologiset oireet Oksentelu Maksatoksisuus Veren neutrofiili-solujen niukkuus (Neutropenia) |
Haittatapahtumista ilmoittaminen on tärkeää. Se mahdollistaa eläinlääkkeen turvallisuuden jatkuvan seurannan. Jos havaitset haittavaikutuksia, myös sellaisia, joita ei ole mainittu tässä pakkausselosteessa, tai olet sitä mieltä, että lääke ei ole tehonnut, ilmoita ensisijaisesti asiasta eläinlääkärillesi. Voit ilmoittaa kaikista haittavaikutuksista myös myyntiluvan haltijalle tai myyntiluvan haltijan paikalliselle edustajalle käyttämällä tämän pakkausselosteen lopussa olevia yhteystietoja tai kansallisen ilmoitusjärjestelmän kautta:
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
www-sivusto: https://www.fimea.fi/elainlaakkeet/
KOHDE-ELÄINLAJI
Koira, kissa


ANNOSTUS, ANTOREITIT JA ANTOTAVAT KOHDE-ELÄINLAJEITTAIN
Suun kautta.
Metronidatsolin suositeltu annos on 50 mg/kg/vrk 5−7 vuorokauden ajan. Vuorokausiannos voidaan jakaa kahteen yhtä suureen annokseen vuorokaudessa (ts. 25 mg/kg kahdesti vuorokaudessa).
Oikean annoksen varmistamiseksi eläimen paino on määritettävä mahdollisimman tarkasti.
ANNOSTUSOHJEET
Tabletin voi jakaa kahteen tai neljään yhtä suureen osaan tarkkaa annostelua varten. Aseta tabletti tasaiselle alustalle jakouurrepuoli ylöspäin ja kupera (pyöreä) puoli alaspäin.
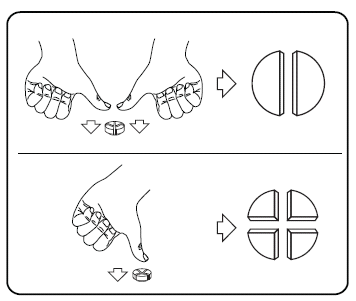
Puolikkaat: paina peukaloillasi tabletin molempia puolia.
Neljännekset: paina peukalollasi tabletin keskeltä.
VAROAIKA
Ei oleellinen.
SÄILYTYSOLOSUHTEET
Ei lasten näkyville eikä ulottuville.
Ei erityisiä säilytysohjeita.
Älä käytä tätä eläinlääkettä viimeisen käyttöpäivämäärän jälkeen, joka on ilmoitettu ulkopakkauksessa ja läpipainopakkauksessa merkinnän Exp. jälkeen.
Viimeisellä käyttöpäivämäärällä tarkoitetaan kuukauden viimeistä päivää.
Jaettujen tablettien kestoaika: 3 vuorokautta.
ERITYISVAROITUKSET
Erityiset varotoimet, jotka liittyvät turvalliseen käyttöön kohde-eläinlajilla:
Koska metronidatsolille vastustuskykyisten bakteerien esiintymisessä on todennäköisesti (ajallisia, maantieteellisiä) vaihteluita, suositellaan bakteriologisen näytteen ottoa ja herkkyysmääritystä.
Mikäli mahdollista, eläinlääkettä tulisi käyttää ainoastaan herkkyysmäärityksen perusteella.
Eläinlääkkeen käytössä on noudatettava mikrobilääkehoidon tarkoituksenmukaista käyttöä koskevia virallisia, kansallisia ja paikallisia ohjeita.
Tabletit ovat maustettuja. Säilytä tabletit eläinten ulottumattomissa tablettien tahattoman nielemisen välttämiseksi. Hermostollisia oireita saattaa ilmetä erityisesti pitkäaikaisessa metronidatsolihoidossa.
Erityiset varotoimenpiteet, joita eläinlääkettä eläimille antavan henkilön on noudatettava:
Metronidatsoli voi aiheuttaa yliherkkyysreaktioita. Henkilöiden, jotka ovat yliherkkiä metronidatsolille, tulee välttää kosketusta eläinlääkkeen kanssa.
Metronidatsolilla on vahvistettu olevan mutaatioita aiheuttavia ja perimämyrkyllisiä ominaisuuksia sekä laboratorioeläimillä että ihmisillä. Metronidatsolin on vahvistettu olevan syöpää aiheuttava laboratorioeläimille, ja sillä saattaa olla syöpää aiheuttavia vaikutuksia ihmisille. Metronidatsolin kyvystä aiheuttaa syöpää ihmisille ei kuitenkaan ole riittävästi näyttöä.
Metronidatsoli voi vahingoittaa sikiötä.
Vältä vahingossa tapahtuvaa nielemistä ja kosketusta iholle tai limakalvoille, mukaan lukien kosketus kädestä suuhun. Käytä näiden välttämiseksi läpäisemättömiä käsineitä eläinlääkettä käsitellessäsi ja/tai antaessasi sitä suoraan eläimen suuhun.
Älä anna hoidetun koiran nuolla ketään heti lääkkeen annon jälkeen. Jos valmistetta joutuu iholle, pese ihoalue huolellisesti. Valmisteen tahattoman nielemisen välttämiseksi ja etenkin sen välttämiseksi, että lapsi nielee valmistetta, käyttämättömät tabletin osat pitää laittaa takaisin avattuun läpipainopakkaukseen, joka laitetaan takaisin ulkokoteloon ja säilytetään turvallisessa paikassa poissa lasten näkyviltä ja ulottuvilta. Käyttämättä jäävät tabletin osat pitää käyttää seuraavalla antokerralla.
Jos vahingossa nielet valmistetta, käänny välittömästi lääkärin puoleen ja näytä hänelle pakkausseloste tai myyntipäällys.
Jos vahingossa nielet valmistetta, käänny välittömästi lääkärin puoleen ja näytä hänelle pakkausseloste tai myyntipäällys. Pese kädet huolellisesti käytön jälkeen.
Tiineys:
Laboratorioeläimillä tehtyjen tutkimusten tulokset ovat olleet ristiriitaisia metronidatsolin teratogeenisten/alkiotoksisten vaikutusten osalta. Sen vuoksi tämän eläinlääkkeen käyttöä ei suositella tiineyden aikana.
Laktaatio:
Metronidatsoli erittyy maitoon, minkä vuoksi käyttöä ei suositella laktaation aikana.
Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset:
Metronidatsolilla saattaa olla muiden lääkkeiden, kuten fenytoiinin, siklosporiinin tai varfariinin, maksassa tapahtuvaa hajoamista estävä vaikutus.
Simetidiini saattaa hidastaa metronidatsolin metaboliaa maksassa, mikä suurentaa metronidatsolin pitoisuutta seerumissa.
Fenobarbitaali saattaa nopeuttaa metronidatsolin metaboliaa maksassa, mikä alentaa metronidatsolin pitoisuutta seerumissa.
Yliannostus:
Suositeltua suuremmat annokset ja pidempi hoito kesto lisäävät haittavaikutusten todennäköisyyttä. Hermostollisten oireiden ilmetessä hoito on keskeytettävä ja potilaalle on annettava oireenmukaista hoitoa.
ERITYISET VAROTOIMET KÄYTTÄMÄTTÖMÄN VALMISTEEN TAI JÄTEMATERIAALIN HÄVITTÄMISEKSI
Lääkkeitä ei saa kaataa viemäriin eikä hävittää talousjätteiden mukana.
Eläinlääkkeiden tai niiden käytöstä syntyvien jätemateriaalien hävittämisessä käytetään paikallisia palauttamisjärjestelyjä sekä kyseessä olevaan eläinlääkkeeseen sovellettavia kansallisia keräysjärjestelmiä. Näiden toimenpiteiden avulla voidaan suojella ympäristöä.
Kysy käyttämättömien lääkkeiden hävittämisestä eläinlääkäriltäsi tai apteekista.
PÄIVÄMÄÄRÄ, JOLLOIN PAKKAUSSELOSTE ON VIIMEKSI HYVÄKSYTTY
10.12.2025
Tätä eläinlääkettä koskevaa yksityiskohtaista tietoa on saatavilla unionin valmistetietokannassa (https://medicines.health.europa.eu/veterinary).
MUUT TIEDOT
Jaettava tabletti
MYYNTILUVAN HALTIJAN NIMI JA OSOITE SEKÄ ERÄN VAPAUTTAMISESTA VASTAAVAN VALMISTAJAN NIMI JA OSOITE EUROOPAN TALOUSALUEELLA, JOS ERI
Myyntiluvan haltija:
Dechra Regulatory B.V.
Handelsweg 25
5531 AE Bladel
Alankomaat
Erän vapauttamisesta vastaava valmistaja:
LelyPharma B.V.
Zuiveringsweg 42
8243 PZ Lelystad
Alankomaat
Genera d.d.
Svetonedeljska cesta 2,
10436 Rakov Potok
Kroatia
Paikalliset edustajat ja yhteystiedot epäillyistä haittatapahtumista ilmoittamista varten:
Dechra Veterinary Products Oy
Yliopistonkatu 31
20100 Turku
Suomi
Puh.: +358 (0)22510500
Lisätietoja tästä eläinlääkkeestä saa myyntiluvan haltijan paikalliselta edustajalta.