TRALIEVE VET purutabletti 20 mg
ELÄINLÄÄKEVALMISTEEN NIMI
Tralieve vet 20 mg purutabletit koiralle
VAIKUTTAVAT JA MUUT AINEET
Yksi tabletti sisältää:
Vaikuttava aine:
Tramadoli 17,6 mg
(vastaa 20 mg tramadolihydrokloridia)
Vaaleanruskea, ruskeatäpläinen, pyöreä ja kupera 7 mm:n maustettu tabletti, jonka toisella puolella on ristinmuotoinen jakouurre.
Tabletin voi jakaa kahteen tai neljään yhtä suureen osaan.
KÄYTTÖAIHEET
Lievän akuutin ja kroonisen pehmytkudosten ja tuki- ja liikuntaelimistön kivun vähentämiseen.
VASTA-AIHEET
Ei saa antaa yhdessä trisyklisten masennuslääkkeiden, monoamiinioksidaasin (MAO:n) estäjien eikä serotoniinin takaisinoton estäjien kanssa.
Ei saa käyttää tapauksissa, joissa esiintyy yliherkkyyttä tramadolille tai apuaineille.
Ei saa käyttää eläimille, joilla on epilepsia.
HAITTAVAIKUTUKSET
Koira:
Yleinen (1–10 eläintä 100 hoidetusta eläimestä): | Sedaatioa,b, uneliaisuusb |
Melko harvinainen 1–10 eläintä 1 000 hoidetusta eläimestä): | Pahoinvointi, oksentelu |
Harvinainen (1–10 eläintä 10 000 hoidetusta eläimestä): | Yliherkkyysreaktioc |
Hyvin harvinainen (< 1 eläin 10 000 hoidetusta eläimestä, yksittäiset ilmoitukset mukaan luettuina): | Kouristuksetd |
a Lievää.
b Varsinkin jos on annettu suurempia annoksia.
c Hoito on lopetettava.
d Koirilla, joilla on alhainen kouristuskynnys.
Haittatapahtumista ilmoittaminen on tärkeää. Se mahdollistaa eläinlääkkeen turvallisuuden jatkuvan seurannan. Jos havaitset haittavaikutuksia, myös sellaisia, joita ei ole mainittu tässä pakkausselosteessa, tai olet sitä mieltä, että lääke ei ole tehonnut, ilmoita ensisijaisesti asiasta eläinlääkärillesi. Voit ilmoittaa kaikista haittavaikutuksista myös myyntiluvan haltijalle tai myyntiluvan haltijan paikalliselle edustajalle käyttämällä tämän pakkausselosteen lopussa olevia yhteystietoja tai kansallisen ilmoitusjärjestelmän kautta:
Lääkealan turvallisuus- ja kehittämiskeskus Fimea
www-sivusto: https://www.fimea.fi/elainlaakkeet/
KOHDE-ELÄINLAJI
Koira.
ANNOSTUS, ANTOREITIT JA ANTOTAVAT KOHDE-ELÄINLAJEITTAIN
Suun kautta.
Suositeltu annos on 2-4 mg tramadolihydrokloridia painokiloa kohti 8 tunnin välein tai kivun voimakkuuden perusteella tarpeen mukaan.
Lyhyin sallittu antoväli on 6 tuntia. Suositeltu päivittäinen maksimiannos on 16 mg/kg. Koska yksilöllinen vaste tramadolille vaihtelee ja riippuu osittain annostuksesta, potilaan iästä, yksilöllistä kipuherkkyyseroista sekä yleistilasta, optimaalinen annostusohjelma on suunniteltava yksilöllisesti yllä esitetyn annoksen ja toistuvasti annettavan hoidon aikavälien perusteella. Eläinlääkärin on tutkittava koira säännöllisesti ja arvioitava tällöin, tarvitaanko lisää kivunlievitystä. Lisälievitystä kipuun voidaan antaa suurentamalla tramadoliannosta kunnes päivittäinen maksimiannos on saavutettu ja/tai käyttämällä monimuotoista (multimodaalista) kivunlievitystä, jossa hoitoon lisätään muita sopivia kipulääkkeitä. Jotta seuraavaa antokertaa varten jäisi mahdollisimman vähän osiin jaettuja tabletteja, on käytettävä vahvuuksiltaan sopivimpia tabletteja.
Huomaa, että tämä antotaulukko on tarkoitettu ohjeeksi annettaessa eläinlääkettä annoshaitarin suurimmalla annoksella: 4 mg/painokilo. Taulukossa kerrotaan, montako tablettia tarvitaan, kun tramadolihydrokloridia halutaan antaa 4 mg/painokilo.
| Painokilo | Tramadoli 20 mg |
|---|---|
| 1,25 kg | |
| 2,5 kg | |
| 3,75 kg | |
| 5 kg | |
| 6,25 kg | |
| 7,5 kg | |
| 10 kg | |
| 15 kg |
![]() = ¼ tablettia
= ¼ tablettia ![]() = ½ tablettia
= ½ tablettia ![]() = ¾ tablettia
= ¾ tablettia ![]() = 1 tablettia
= 1 tablettia
ANNOSTUSOHJEET
Tabletin voi jakaa kahteen tai neljään yhtä suureen osaan tarkan annostelun varmistamiseksi. Aseta tabletti tasaiselle alustalle jakouurteellinen puoli ylöspäin ja kupera (pyöreä) puoli alustaa vasten.
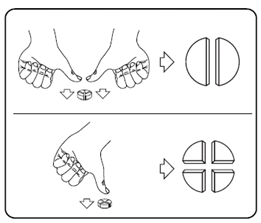
Puolikkaat: paina peukalolla tabletin molempia sivuja.
Neljännekset: paina peukalolla tabletin keskeltä.
VAROAIKA
Ei oleellinen.
SÄILYTYSOLOSUHTEET
Ei lasten näkyville eikä ulottuville.
Osiin jaettujen tablettien kestoaika sisäpakkauksen ensimmäisen avaamisen jälkeen: 3 vuorokautta.
Älä säilytä yli 30 °C.
Säilytä alkuperäispakkauksessa. Herkkä kosteudelle.
Älä käytä tätä eläinlääkettä viimeisen käyttöpäivämäärän jälkeen, joka on ilmoitettu pahvikotelossa merkinnän Exp jälkeen.
Viimeisellä käyttöpäivämäärällä tarkoitetaan kuukauden viimeistä päivää.
ERITYISVAROITUKSET
Erityisvaroitukset:
Tramadolihydrokloridin analgeettiset vaikutukset voivat vaihdella. Tämän ajatellaan johtuvan lääkkeen aineenvaihdunnan yksilöllisistä eroista ensisijaisen vaikuttavan metaboliitin, O-desmetyylitramadolin, osalta. Joillakin koirilla (hoitoon vastaamattomat) tämä voi johtaa siihen, että eläinlääke ei saa aikaan kivunlievitystä. Krooniseen kipuun on harkittava monimuotoista kivunlievitystä. Eläinlääkärin on tarkkailtava koiraa säännöllisesti riittävän kivunlievityksen varmistamiseksi. Jos kipu on uusiutuvaa tai kivunlievitys riittämätöntä, kivunhoito-ohjelma on ehkä suunniteltava uudelleen.
Erityiset varotoimet, jotka liittyvät turvalliseen käyttöön kohde-eläinlajilla:
Käytä varoen munuaisten tai maksan vajaatoimintaa sairastaville koirille. Maksan vajaatoimintaa sairastavilla koirilla tramadolin metabolia vaikuttaviksi metaboliiteiksi voi vähentyä, mikä voi heikentää eläinlääkkeen tehoa. Yksi tramadolin vaikuttavista metaboliiteista erittyy munuaisten kautta, minkä vuoksi munuaisten vajaatoimintaa sairastavilla koirilla annostusohjelmaa voidaan joutua muuttamaan. Munuaisten ja maksan toimintaa on tarkkailtava tätä eläinlääkettä käytettäessä. Pitkäaikaisen kivunlievityshoidon lopettaminen on tehtävä asteittain aina kun mahdollista.
Erityiset varotoimenpiteet, joita eläinlääkettä eläimille antavan henkilön on noudatettava:
Henkilöiden, jotka ovat yliherkkiä tramadolille tai jollekin apuaineelle, tulee välttää kosketusta eläinlääkkeen kanssa.
Jos valmistetta on vahingossa nielty, tramadoli voi aiheuttaa sedaatiota, pahoinvointia ja heitehuimausta, varsinkin lasten ollessa kyseessä. Vahingossa tapahtuvan nielemisen estämiseksi (varsinkin lapsen kohdalla) käyttämättä jäänyt tabletti on asetettava takaisin avatussa läpipainopakkauksessa olevaan syvennykseensä. Pakkaus laitetaan sitten takaisin pahvikoteloon ja säilytetään turvallisessa paikassa, johon lapset eivät näe eivätkä ulotu, sillä jos pienet lapset nielevät vahingossa tabletteja, ne ovat vaaraksi lasten terveydelle. Jos vahingossa nielet valmistetta, varsinkin lasten ollessa kyseessä, käänny lääkärin puoleen ja näytä hänelle pakkausseloste tai myyntipäällys. Jos aikuinen on niellyt valmistetta vahingossa: ÄLÄ AJA AUTOA, koska sedaatiota voi ilmetä.
Pese kädet käytön jälkeen.
Tiineys:
Laboratoriotutkimuksissa (hiiri ja/tai rotta ja kani) ei ole löydetty näyttöä epämuodostumia aiheuttavista, sikiötoksisista tai emolle toksisista vaikutuksista. Voidaan käyttää ainoastaan hoitavan eläinlääkärin hyöty-riskiarvion perusteella.
Laktaatio:
Laboratoriotutkimuksissa (hiiri ja/tai rotta ja kani) ei ole löydetty näyttöä jälkeläisten peri- ja postnataaliseen kehitykseen kohdistuvista haittavaikutuksista. Voidaan käyttää ainoastaan hoitavan eläinlääkärin hyöty-riskiarvion perusteella.
Hedelmällisyys:
Laboratoriotutkimuksissa (hiiri ja/tai rotta ja kani) tramadolin käyttö terapeuttisilla annoksilla ei vaikuttanut haitallisesti urosten eikä naaraiden lisääntymiskykyyn ja hedelmällisyyteen. Voidaan käyttää ainoastaan hoitavan eläinlääkärin hyöty-riskiarvion perusteella.
Yhteisvaikutukset muiden lääkevalmisteiden kanssa sekä muut yhteisvaikutukset:
Tämän eläinlääkkeen samanaikainen anto keskushermoston toimintaa lamaavien lääkkeiden kanssa saattaa voimistaa keskushermostoa ja hengitystä lamaavia vaikutuksia.
Tramadoli saattaa lisätä kouristuskynnystä alentavien lääkkeiden vaikutusta.
Lääkkeillä, jotka estävät CYP450-välitteistä metaboliaa (esim. simetidiini ja erytromysiini) tai indusoivat sitä (esim. karbamatsepiini), saattaa olla vaikutusta tramadolin analgeettiseen vaikutukseen. Näiden yhteisvaikutusten kliinistä merkitystä ei ole tutkittu koirilla.
Tramadolin käyttö yhdessä agonisti/antagonistin (esim. bufenorfiini, butorfanoli) kanssa ei ole suositeltava, koska puhtaan agonistin kipua lievittävä vaikutus voi sellaisissa olosuhteissa teoriassa vähentyä.
Katso myös kohta ”Vasta-aiheet”.
Yliannostus:
Tramadolia käytettäessä sattuvissa myrkytystapauksissa voi esiintyä oireita, jotka ovat samanlaisia kuin muita keskushermostoon vaikuttavia kipulääkkeitä (opioideja) käytettäessä havaittavat oireet. Näitä ovat erityisesti seuraavat: mioosi (mustuaisten supistuminen), oksentelu, sydän- ja verenkiertoelimistön kollapsi, tajunnantason häiriöt (voivat vaihdella koomaan asti), kouristukset ja hengityslama (voi vaihdella hengityspysähdykseen asti).
Yleiset ensiaputoimet: pidä hengitystie avoimena, tue sydämen ja hengityselinten toimintaa oireista riippuen. Oksennuttamista mahan tyhjentämiseksi voidaan käyttää, paitsi jos eläimellä ilmenee tajunnantason alenemista; tällöin voidaan harkita mahahuuhtelua. Hengityslaman vastalääke on naloksoni. Naloksoni ei kuitenkaan välttämättä ole hyödyllinen kaikissa tramadolin yliannostustapauksissa, sillä se saattaa peruuttaa joitakin tramadolin muista vaikutuksista vain osittain. Kouristustapauksissa on annettava diatsepaamia.
ERITYISET VAROTOIMET KÄYTTÄMÄTTÖMÄN VALMISTEEN TAI JÄTEMATERIAALIN HÄVITTÄMISEKSI
Lääkkeitä ei saa kaataa viemäriin eikä hävittää talousjätteiden mukana.
Eläinlääkkeiden tai niiden käytöstä syntyvien jätemateriaalien hävittämisessä käytetään paikallisia palauttamisjärjestelyjä sekä kyseessä olevaan eläinlääkkeeseen sovellettavia kansallisia keräysjärjestelmiä. Näiden toimenpiteiden avulla voidaan suojella ympäristöä.
Kysy käyttämättömien lääkkeiden hävittämisestä eläinlääkäriltäsi tai apteekista.
PÄIVÄMÄÄRÄ, JOLLOIN PAKKAUSSELOSTE ON VIIMEKSI HYVÄKSYTTY
10.12.2025
Tätä eläinlääkettä koskevaa yksityiskohtaista tietoa on saatavilla unionin valmistetietokannassa (https://medicines.health.europa.eu/veterinary).
MUUT TIEDOT
Osiin jaettava tabletti
MYYNTILUVAN HALTIJAN NIMI JA OSOITE SEKÄ ERÄN VAPAUTTAMISESTA VASTAAVAN VALMISTAJAN NIMI JA OSOITE EUROOPAN TALOUSALUEELLA, JOS ERI
Myyntiluvan haltija:
Dechra Regulatory B.V.
Handelsweg 25
5531 AE Bladel
Alankomaat
Erän vapauttamisesta vastaava valmistaja:
Lelypharma B.V.
Zuiveringweg 42
8243 PZ Lelystad
Alankomaat
Genera d.d.
Svetonedeljska cesta 2
10436 Rakov Potok
Kroatia
Paikalliset edustajat ja yhteystiedot epäillyistä haittatapahtumista ilmoittamista varten:
Dechra Veterinary Products Oy
Yliopistonkatu 31
20100 Turku
Suomi
Puh.: +358 (0)22510500